Kuinka ravinto ja elintavat vaikuttavat MS-taudin etenemiseen? Osa 2
Tulehdusten vaikutus neurodegeneratiivisiin tapahtumiin assosioituu vahvasti kaikkiin MS-taudin muotoihin. Aktiiviset leesiot liittyvät yleensä inflammaatioon. Tästä syystä MS-hoitojen kohdentaminen tulehduksellisiin tekijöihin on aiheellista. (Frischer et al., 2009; Lassmann, 2013, Kutzelnigg and Lassmann, 2014). Inflammaatio ja sen merkitys MS-taudissa jatkaa edellisen artikkelin aloittamaa syvempää tutustumista MS-tautiin vaikuttaviin tekijöihin.
MS on ongelmallinen sairaus. Tautiin vahvasti assosioituvia geenivariantteja tunnetaan 100-200. Näistä useimmat osallistuvat immuunijärjestelmän toimintaan. Monitekijäiseen tautiin vaikuttaa vaihtelevien ympäristö- ja geenitekijöiden lisäksi myös eräät aineenvaihduntaan kytkeytyvät tekijät. (Ascherio, 2013)
Ravinnolla on kiistattomia vaikutuksia terveyteen. Jotkin ravintoaineet altistavat lihomiselle, matala-asteiselle tulehdukselle ja sairastumiselle, mutta toiset ehkäisevät tulehduksia, ylläpitävät kehon normaalia aineenvaihduntaa ja terveyttä.
Ravintoaineet osallistuvat solujen ja suoliston mikrobiomin kautta aineenvaihduntaan tulehduksellisissa taudeissa, kuten MS-taudissa. Ravintoaineet voivat siis hillitä tai pahentaa tulehdusreaktioita. Jatketaan tässä artikkelissa Paolo Riccion ja Rocco Rossanon laajan ravintoa ja tulehdustekijöitä käsittelevän tutkimuskatsauksen avaamista.
Inflammaatio ja sen merkitys MS-taudissa
- Ravinnon määrä ja laatu vaikuttavat mm. entsyymien, transkriptiotekijöiden sekä solun tuman reseptorien toiminnan kautta aineenvaihduntaan. Ravintoaineet myös ohjaavat soluja joko anaboliseen tai kataboliseen aineenvaihduntaan sekä säätelevät tulehduksellisia ja immunologisia vasteita elimistössä. (Desvergne et al., 2006).
- Ravinto ja elintavat osallistuvat monella tavalla suolistoflooran hyvinvointiin. Ihminen on eräänlainen metaorganismi, joka elää mutualistisessa taikka symbiottisessa suhteessa kehon mikrobiomin kanssa.Mikrobiomi muodostuu biljoonista mikrobeista (1014), jotka voivat edustaa satoja tai jopa yli tuhatta bakteerilajia. Mikrobiomin merkitystä korostaa lisäksi se, että kehossa mikrobien soluja on arvioiden mukaan kymmenkertainen määrä kehon omiin soluihin nähden.Tämä monimutkainen ekosysteemi on keskeinen osa ihmistä, ja se vaikuttaa sekä aineenvaihdunnan että immuunijärjestelmän kautta elimistön toimintaan.
Osallistuva mikrobiomi
Keho toimii mutualistisessa tai symbioottisessa suhteessa mikrobiomin hyvien mikrobien kanssa. Mutualismilla tarkoitetaan biologiassa kahden osapuolen välistä fysiologista suhdetta, joka on kummallekin myönteinen.
Eubioosi ja dysbioosi
Suolistoflooralla on useita tärkeitä immunologisia ja metabolisia tehtäviä; se mm. suojelee elimistöä enteropatogeeneiltä ja osallistuu moniin immuunijärjestelmän normaaleihin toimintoihin.
Suolisto on ihmisen suurin immunologinen elin ja monilla sairauksilla on yhteys ruoansulatuksen ja suoliston toimintaan. Eubioottinen suoliston mikrobiomi on terve ja tasapainoinen.
Terve ja tasapainoinen, eubioottinen mikrobiomi voi muuttua oireilevaksi, dysbioottiseksi mikrobiomiksi, jos patogeenisten mikrobikantojen määrä pääsee lisääntymään ja horjuttamaan suoliston mikrobien herkkää tasapainoa. Dysbioosilla tarkoitetaan suoliston bakteerikannan haitallisia muutoksia. (Chassaing and Gewirtz, 2014)
Dysbioosi voi aiheuttaa monenlaisia oireita, kuten:
- Vatsan turvotus
- Aivosumu
- Akne
- Ripuli
- Ummetus
- Ihon kutina
- Heikot kynnet
- Väsymys
- Ahdistus
- Painonnousu
Dysbioosin aiheuttamiin oireisiin vaikuttaa se, mitkä suoliston bakteerikannat ovat epätasapainossa. Tutkimuksissa on havaittu, että suolistoflooran dysbioosi assosioituu mm. tulehduksellisiin suolistosairauksiin (IBD), ärtyneen suolen oireyhtymään (IBS), allergioihin, astmaan, sydän- ja verisuonitauteihin, metaboliseen oireyhtymään, autoimmuunitauteihin ja ylipainoon.
Dysbioosiin vaikuttavia tekijöitä
Suolistofloora on herkästi haavoittuva mikrobien ekosysteemi. Dysbioosi voi kehittyä suolistoon mm. antibioottien käytön, stressin ja epäterveellisen, paljon sokeria, valkoisia jauhoja, huonoja rasvoja, alkoholia sekä punaista lihaa sisältävän ruokavalion seurauksena.
Toisaalta dysbioosia voi ehkäistä ruokavalion avulla. Runsaskuituinen, pro- ja prebiootteja sisältävä, kasvisvoittoinen hapatettuja ruokia sisältävä ruokavalio ylläpitää suolistoflooran hyvinvointia. Suolistoflooran kannalta hyviä ravintoaineita ovat:
- Juurekset
- Tummanvihreät lehtikasvit, kuten pinaatti
- Sipulit
- Palkokasvit
- Kaalit
- Hapatetut ruoat (hapankaali, suolakurkut, kimchi, jogurtti, viili ja piimä)
- Täysjyväviljat
Ravinnon vaikutukset suolistoflooran tasapainoon perustuvat siihen, että eri ravintoaineet ruokkivat erilaisia mikrobipopulaatioita suolistossa. Ruokavalio voi johtaa yhtä hyvin elimistölle hyödyllisten tai haitallisten bakteerikantojen lisääntymiseen ja siten vaikuttaa suolistoflooran tasapainoon.
Yksipuolinen ravinto yksipuolistaa myös suoliston mikrobiomia ja heikentää siten immuunijärjestelmän toimintaa.
Runsaasti prosessoituja ravintoaineita, sokereita, huonoja rasvoja, punaista lihaa ja alkoholia sisältävä dysbioosia edistävä ravinto altistaa suoliston inflammaatiolle. Suoliston tulehdukset ja immuuunijärjestelmän toiminnan muutokset kasvattavat systeemisen inflammaation ja kroonisten tulehdussairauksien riskiä.
Suoliston hyvät mikrobit hyödyntävät ruoansulatuskanavassa sulamatonta kuitua ja vapauttavat elimistöön ihmiselle tärkeitä lyhytketjuisia rasvahappoja. Lyhytketjuiset rasvahapot vahvistavat suolen pintakerroksia, hillitsevät tulehduksia sekä säätelevät kylläisyyttä ja rasvan kertymistä kehoon.
FODMAP
Aina suolistobakteereita hyödyttävä sinänsä terveellinen ravinto ei toimi toivotulla tavalla. Ärtyvän suolen oireyhtymää (IBS) sairastavilla huonosti ohutsuolesta imeytyvät lyhytketjuiset ns. FODMAP-hiilihydraatit voivat aiheuttaa oireita, kuten turvotusta, vatsakipuja ja ilmavaivoja.
FODMAP-nimitys tulee hiilihydraattien englanninkielisistä nimistä fermentable oligo-, di- and monosaccharides and polyols. FODMAP-hiilihydraatteja ovat fruktaanit, galaktaanit, raffinoosit, fruktoosi, laktoosi ja polyolit eli sokerialkoholit.
FODMAP-hiilihydraattien on todettu aiheuttavan vaikeita oireita suurimmalle osalle IBS:stä kärsivistä. Osalla ärtyvän suolen oireyhtymän oireita voi aiheuttaa FODMAP-hiilihydraattien sijaan stressi ja muut elintavat.
Metabolia: Ravintoaineet vaikuttavat aineenvaihduntaan ja soluihin sekä säätelevät tulehdusreaktiota
Aineenvaihdunta on kaksisuuntainen biologinen prosessi. Ravinto pilkotaan ruoansulatuskanavassa imeytyvään muotoon eli ravinnon perusmolekyyleiksi (aminohapot, rasvahapot, sokerit, suojaravinteet ja vesi), joita elimistö voi käyttää energiaravinteina sekä elimistön uusiutumisen ja veren, lihasten, luiden, entsyymien, hormonien ja ruoansulatusnesteiden tarvitsemina rakennusaineina.
Aineenvaihdunta jaetaan kahteen toimintamekanismiin: anaboliseen ja kataboliseen aineenvaihduntaan.
Anaboliset reaktiot ovat energiaa kuluttavia reaktioita, joissa yksinkertaisista lähtöaineista valmistetaan monimutkaisempia yhdisteitä. Kataboliset reaktiot ovat energiaa tuottavia reaktioita, joissa suuret molekyylit pilkotaan yksinkertaisemmiksi yhdisteiksi. Ravintoaineiden pilkkomisen seurauksena energiaravinteista (hiilihydraatit, rasvat ja proteiinit) vapautetaan energiaa elimistön käyttöön.
Esimerkiksi:
Anabolisissa reaktioissa yksinkertaisista lähtöaineista rakennetaan monimutkaisempia makromolekyylejä:
Solun rakennuspalikat Solurakenteen suuremmat yksiköt
Sokerit – – > Polysakkaridit
Rasvahapot – – > Rasvat, lipidit, solukalvot
Aminohapot – – > Proteiinit
Nukleotidit – – > NukleiinihappoAnaboliset reaktiot kuluttavat energiaa ATP:n tai NADH:n (ja NADPH:n) muodossa.
ATP – – > ADP + Pi
NADH + H+ – – > NAD+Aineenvaihdunnan proteiinisynteesi kuluttaa runsaasti energiaa. Myös glukoosia muodostava glukoneogeneesi kuluttaa enemmän energiaa kuin mitä se tuottaa glukoosina solujen glykolyysissä ja soluhengityksessä.
Anabolinen ja katabolinen aineenvaihdunta vuorottelevat elimistössä päivittäisten rutiinien lisäksi myös iän ja elämäntilanteen mukaan. Fyysinen harjoittelu ja sairaudesta toipuminen kallistavat aineenvaihduntaa anaboliseksi, jolloin aineenvaihdunta rakentaa esimerkiksi lihaskudosta tai korjaa sairauden aiheuttamia vaurioita. Myös kasvavien lasten aineenvaihdunta painottuu anabolisen metabolian puolelle.
Minulla ja uskoakseni monella MS-tautia sairastavalla aineenvaihdunta on katabolisessa tilassa. Se osaltaan selittää lihaskatoa.
Aineenvaihduntaan vaikuttavia tekijöitä
Aineenvaihduntaan vaikuttaa useita tekijöitä, kuten ravinnon määrä ja laatu, makroravinteet, ravinnon sisältämät suojaravinteet (vitamiinit ja mineraalit), stressi, nestetasapaino, maksan, suoliston ja haiman terveys, geenit, hormonit, insuliinisensitiivisyys, leptiinisensitiivisyys, liikunta, ja uni jne.
Entsyymit ja transkriptiotekijät
Kuinka ravintomolekyylit vaikuttavat solujen metaboliaan? Tämän ymmärtämiseksi täytyy määritellä kataboliaan ja anaboliaan vaikuttavien entsyymien ja transkriptiotekijöiden merkitys.

Yksinkertaistettu kaavio osoittaa miten luonnolliset ravintotekijät säätelevät solumetaboliaa oksidatiiviseen aineenvaihduntaan (vasemmalla), biosynteesiin (oikealla) ja NF-kB-välitteiseen inflammaatioon (alla keskellä) sitoutumalla tumareseptoreihin, transkriptiotekijöihin sekä vuorovaikutteisiin entsyymeihin. Kuvan lähde: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4342365/
Agonisti ja antagonisti
Agonisti eli ”reseptorinaktivoija” on kemiallinen yhdiste, joka rakenteensa perusteella eli ligandina ja elimistön viestimolekyylien tavoin aktivoi kohdereseptoriaan ja käynnistää siihen kytkeytyvän solun fysiologisen signaalinvälitysmekanismin.
Agonistin vaikutus voidaan kumota agonistin kanssa samaan reseptoriin sitoutuvalla antagonistilla eli reseptorinsalpaajalla.
Tumareseptori
Tumareseptorit sijaitsevat joko tumassa DNA:han kiinnittyneinä tai solun sytoplasmassa. Ne aktivoituvat solukalvon läpäisevän, hydrofobisen viestimolekyylin sitouduttua niihin.
Tällaisia viestimolekyylejä ovat mm. monet hormonit (tyroksiini, estradioli, testosteroni, kortisoli, retinoli ja D-vitamiini), jotka reseptoriinsa sitouduttuaan vaikuttavat suoraan solun geeniekspressioon.
Kaikkien tumareseptorien rakenteeseen kuuluu:
- Transkriptiota säätelevä alue
- DNA:han sitoutuva alue
- Ligandia sitova alue.
Transkriptio
Transkriptio on biologinen prosessi, jossa DNA-templaatin avulla valmistetaan yhdelle DNA-juosteelle komplementaarinen RNA-molekyyli. Transkriptiossa RNA-polymeraasi kopioi DNA:ssa olevaa geneettistä koodia RNA:ksi. Se on proteiinisynteesin ensimmäinen vaihe.
Transkriptiossa syntyy myös lähetti-RNA-, ribosomaalinen-RNA- ja siirtäjä-RNA-molekyylejä. Lähetti-RNA:ta käytetään proteiinisynteesin mallina translaatiossa, siirtäjä-RNA:t kuljettavat aminohappoja translaatiossa käytettäväksi ja ribosomaalinen RNA muodostaa yhdessä ribosomaalisten proteiinien kanssa ribosomeja, jotka toimivat translaatiossa moottoreina.
RNA-polymeraasi
RNA-polymeraasi on entsyymi, joka aukaisee kaksijuosteista DNA:ta lyhyeltä matkalta ja liittää nukleotidejä toisen DNA-juosteen (templaatin) pariksi muodostuvaan RNA-molekyyliin.
Templaattina toimivaa DNA-juostetta kutsutaan (-)-juosteeksi ja koodaavaa juostetta (+)-juosteeksi (koodaavassa juosteessa siis sama emäsjärjestys kuin muodostuvassa RNA-molekyylissä).
Toisin kuin DNA-polymeraasi, RNA-polymeraasi ei tarvitse aluketta, vaan voi aloittaa RNA:n synteesin suoraan DNA:n ja nukleotidien (A, U, C, G) avulla. RNA-polymeraasi tarvitsee kuitenkin erityisiä DNA-sekvenssejä, promoottoreita, joiden kohdalle polymeraasi sitoutuu. Lähde: Solunetti
Transkriptiotekijät
Transkriptiotekijät eli transkriptiofaktorit ovat proteiineja, jotka tunnistavat DNA:ssa promoottoreita ja tehostajia ja säätelevät geenin transkriptiota. Transkriptiotekijöiden on tunnistettava ja liityttävä DNA:n aloituskohtaan, ennen kuin RNA-polymeraasi voi liittyä siihen. Transkriptiotekijät jaetaan kolmeen luokkaan:
- Yleiset transkriptiotekijät, jotka ovat transkriptiolle välttämättömiä proteiineja. Yhdessä RNA-polymeraasin kanssa ne muodostavat perustranskriptiokoneiston.
- Ylävirran transkriptiotekijät ovat säätelyn ulkopuolisia proteiineja, jotka kiinnittyvät DNA:han geenin aloituskohdasta ylävirtaan ja säätelevät transkriptiota.
- Indusoivat transkriptiotekijät ovat ylävirran transkriptiofaktoreiden kaltaisia, mutta ne edellyttävät aktivointia tai inhibointia.
Yleisten transkriptiotekijöiden (TFIIA, TFIIB, TFIID, TFIIE, TFIIF) läsnäolo geenien käynnistäjien TATA-alueella on välttämätöntä, jotta transkriptio lähtee alkuun. Sinkkisormet, leusiinivetoketjut, ja heliksi-mutka-heliksin sisältävät proteiinit (engl. homeodomain) ovat tavallisimman tyyppiset transkriptiota säätelevät proteiinit. Lähde: Internetix
Ligandi
Ligandi on molekyyli tai ioni, joka on koordinoitunut keskusioniin ja sitoutunut siihen koordinatiivisella sidoksella. Sidoksen muodostuessa keskusioni toimii Lewisin happona ja ligandit Lewisin emäksinä. Ligandeja kutsutaan yksi-, kaksi-, kolme-, neljä- tai kuusihampaisiksi riippuen siitä kuinka monta elektroniparin luovuttajaksi soveltuvaa luovuttaja-atomia sen rakenteessa on.
Reseptorit voivat olla entsyymejä tai ne voivat aktivoida entsyymejä. Entsyymejä aktivoivien (tai entsyymeinä toimivien) reseptoreiden rakenteessa on ligandia sitovan solun ulkopuolisen osan lisäksi katalyyttinen tai entsyymiä sitova solunsisäinen osa. Entsyymireseptorien ligandina toimii usein kasvutekijä.
Entsyymejä aktivoivat reseptorit ovat toimintansa perusteella
- tyrosiinikinaasireseptorit
- tyrosiinikinaaseja aktivoivat reseptorit
- tyrosiinifosfataasireseptorit
- seriini/treoniinikinaasireseptorit
- guanylaattisyklaasireseptorit
- histidiinikinaasia aktivoivat reseptorit
Entsyymit ja substraatit
Entsyymit ovat biologisia katalyyttejä eli ne nopeuttavat kemiallisia reaktioita. Entsyymit ovat tavallisesti proteiineja, mutta myös RNA-molekyylit voivat olla entsyymejä, jolloin puhutaan ribotsyymeistä.
Monissa proteiinientsyymeissä aktiivinen keskus koostuu muusta kuin aminohapoista, usein aminohappoihin koordinoituneesta yhdestä tai useammasta metalli-ionista. Näitä entsyymiä auttavia ryhmiä kutsutaan kofaktoreiksi ja tavallisimpia ovat kupari-, rauta- ja sinkki-ionit. Jos kofaktori on orgaaninen molekyyli, puhutaan koentsyymistä.
Molekyyliä, johon entsyymin toiminta kohdistuu, kutsutaan substraatiksi. Entsyymien katalyyttinen toiminta perustuu niiden kykyyn alentaa substraattiin kohdistuvan reaktion aktivaatioenergiaa. Tämä tapahtuu siten, että entsyymi pakottaa substraatin kohti siirtymätilaa muodostamalla sen kanssa heikkoja vuorovaikutuksia. Heikkojen vuorovaikutusten ja siirtymätilan uusien sidosten syntyminen vapauttaa energiaa, jka sysää katalysoitavan reaktion liikkeelle nopeammin.
Ilman entsyymejä kemialliset reaktiot tapahtuisivat soluissa liian hitaasti, eikä elämä olisi mahdollista. Entsyymit nopeuttavat reaktioita vähintään tuhatkertaisesti, joskus jopa 1017-kertaisesti. Nopeimmat entsyymit muuttavat jopa 40 miljoonaa molekyyliä reaktiotuotteiksi yhdessä sekunnissa.
Alla lista tulehduksia säätelevistä agonisteista (+) ja antagonisteista (-) sekä eräistä tavallisista lääkkeistä, entsyymeistä, tumareseptoreista ja transkriptiotekijöistä.
Useimmissa tapauksissa agonistit hillitsevät ja antagonistit edistävät inflammaatioita. Joissain tapauksissa tilanne näyttää kuitenkin olevan päinvastainen. Tämä on melko sekavaa, mutta ehkä tästä jonkinlaisen yleiskuvan saa:
AMPK
AMP-aktivoitu proteiinikinaasi. Proteiinikinaasit ovat kinaasientsyymeitä, joiden substraatti on proteiini. Kinaasit ovat tärkeä tekijä solunsisäisessä viestinnässä. Fosfaattiryhmän siirtämällä proteiinikinaasit tyypillisesti aktivoivat tai deaktivoivat substraattinsa. Yksi proteiinikinaasi voi fosforyloida useita substraattimolekyylejä.
AMPK (5-adenosiinimonofosfaatti-aktivoitu proteiinikinaasi) osallistuu solujen energiatasapainon säätelyyn. AMPK:ta esiintyy mm. maksa-, aivo- ja lihaskudoksissa.
(+) Agonistit – Inflammaatiota vähentävät tekijät
- Kaloreiden rajoittaminen; vähäenerginen ravinto.
- Liikunta
- AMP: Adenosiinimonofosfaatti eli adenyylihappo on nukleotidi. Se muodostuu adenosiinikukleosidistä ja siihen liittyneestä fosfaattiryhmästä. Adenosiinimonofosfaatilla on tärkeä rooli aineenvaihdunnassa. se aktivoi useita tärkeitä reaktioita esimerkiksi glykolyysissä, glykogenolyysissä ja rasvahappojen hapettamisessa.
- Greliini: Growth hormone release inducing, eli KH-reliini tai GH-reliini on pääasiassa mahalaukun limakalvolta erittyvä 28 aminohapon mudostama peptidihormoni, joka lisää kasvuhormonin eritystä aivolisäkkeestä. Sen lisäksi greliini stimuloi ruokahalua ja nopeuttaa mahalaukun tyhjenemistä. Greliini vaikuttaa kasvuun aiheuttamalla ruokahalun lisäyksen kautta elimistöön kasvun mahdollistavan anabolisen tilan.
- Alfa-lipoiinihappo: LA; Antioksidantti ja koentsyymi hapetus-pelkistysreaktiossa. Lipoiinihappo on yleinen lisäravinne, joka tutkimuksissa on alentanut MS-tautia sairastavien tulehdusreaktioita.
- Adiponektiini: Rasvasolujen erittämä hormoni, jonka vähäinen määrä veressä korreloi monien sairauksien kanssa.
- Flavonoidit: Kasveissa esiintyviä yhdisteitä, jotka vaikuttavat makuun, väriin, koostumukseen ja säilyvyyteen sekä toimivat antioksidantteina. Flavonoidit voivat vaikuttaa veren hyytymiseen ja ehkäistä syöpiä. Flavonoideja tunnetaan yli 4000.
- Nonflavonoidit: Polyfenoleita, jotka hyödyttävät erityisesti suoliston hyviä mikrobeja.
- Metformiini: Metformiini on suun kautta otettava diabeteslääke, joka parantaa solujen insuliinivastetta. Metformiini voi hillitä inflammaatiota, mutta pitkäaikainen käyttö on yhdistetty kohonneisiin homokysteiinitasoihin sekä B12-vitamiinin imeytymisen heikkenemiseen.
- Salisyylaatit: Salisylaatit ovat salisyylihapon suoloja ja estereitä
(−) Antagonistit – Inflammaatiota lisäävät tekijät
- Dysbioottinen eli epätasapainoinen suoliston mikrobiomi.
- Leptiini: Leptiini on rasvakudoksen vereen erittämä kylläisyyshormoni, joka säätelee ruokahalua ja elimistön energiankäyttöä. Leptiini kertoo hypotalamuksen kautta keskushermostolle kehon varastorasvan määrästä. Kun leptiinin määrä lisääntyy, ruokahalu vähenee ja päinvastoin: leptiinin vähäinen määrä aiheuttaa näläntunnetta.Leptiini vaikuttaa aktiivisuuteen yhdessä insuliinin ja melatoniinin kanssa. Se hillitsee ruokahalua ja vaikuttaa tyreotropiinin (TSH) ja kortikotropiinin (ACTH) erittymiseen aivolisäkkeestä, mikä puolestaan vaikuttaa aineenvaihdunnan vilkkauteen.
Sirtuiinit
Ihmisen histonideasetylaaseja kutsutaan sirtuiineiksi ja niillä on seitsemän alatyyppiä. Histonideasetylaasit (HDAC) ovat entsyymejä, jotka toimivat asetyyliryhmän poistajina.
Esimerkiksi SIRT 1 säätelee useita keskeisiä metabolisia prosesseja ja sillä on suuri merkitys myös energia-aineenvaihdunnan säätelyssä. SIRT 1 säätelee mm. mitokondrioiden biogeneesiä sekä energiametaboliaa ja vaikuttaa mm. diabetekseen ja lihavuuteen. SIRT 1 osallistuu myös rasvametaboliaan ja oksidatiivisen stressin säätelyyn. Sitoutumalla NF-kB:en se todennäköisesti säätelee tulehdusvasteita ja kudosten atrofioitumista. SIRT 2 vaikuttaa mm. solun jakautumisen säätelyyn.
(+) Agonistit – Inflammaatiota vähentävät tekijät
- VDR-D: D-vitamiini ja solujen D-vitamiinireseptorit.
- Kaloreiden rajoittaminen; vähän energiaa sisältävä ravinto.
- Alfa-lipoiinihappo (LA): Antioksidantti ja koentsyymi hapetus-pelkistysreaktiossa. Lipoiinihappo on yleinen lisäravinne, joka tutkimuksissa on hillinnyt MS-tautia sairastavien tulehdusreaktioita.
- Resveratroli: Resveratroli on useissa kasveissa esiintyvä fenoliyhdiste, jolla uskotaan olevan terveyttä hyödyttäviä ominaisuuksia, kuten syöpiä, virustauteja, vanhenemista ja tulehdusta ehkäiseviä sekä hermosoluja suojaavia vaikutuksia.Resveratrolia on erityisesti punaisissa ja sinisissä viinirypäleissä sekä viininlehdissä ja karpaloissa, mutta sitä on myös punaviinissä. Erään tutkimuksen mukaan resveratroli suojaa diabetekselta ja ylipainolta aktivoimalla aineenvaihdunnan säätelyyn vaikuttavaa Sirt1-geeniä. Toisessa tutkimuksessa punaviinillä saatiin hiirikokeissa anti-inflammatorisia vaikutuksia, mutta vastaavien hyötyjen saamiseksi punaviinillä, ihmisen pitäisi juoda 400 lasia punaviinia päivässä.Resveratrolin terveysvaikutuksiin kannattaakin suhtautua varauksella. Tutkimus on hyvin keskeneräistä ja resveratrolin pitkäaikaisvaikutuksia ihmiselle ei tunneta.
- Niasiini (B3-vitamiini): Niasiini on yhteisnimitys nikotiiniamidille ja nikotiinihapolle. Niasiinin johdannaiset ovat elintärkeitä solun aineenvaihdunnalle. Puutos aiheuttaa vakavaa puutostautia – pellagraa.Kaikki B-vitamiinit ovat entsyymien tarvitsemien koentsyymien esiasteita. niasiinia tarvitaan etenkin nikotiiniamidiadeniinidinukleotidien (NAD+ ja NADP+) valmistukseen.Niasiinia saa eläuinperäisestä ravinnosta, kuten lihasta, sisäelimistä, kalasta, kananmunista, maitovalmisteista sekä kokojyväviljoista, pähkinöistä ja lehtivihanneksista.
- TRP (Transient receptor potential channel): TRP-kanavat ovat joukko ionikanavareseptoreita. Ionikanavareseptorit ovat perustilassaan suljettuja. Kun reseptoriin sitoutuu ligandi, kanava avautuu ja ionit pääsevät kulkeutumaan muodostuneen vesihuokosen kautta kalvon läpi konsentraatiogradienttinsa suuntaisesti. Tapahtuma on nopea ja lyhytkestoinen (transient).Monet hermovälittäjäaineiden reseptorit ovat ionikanavareseptoreita. Ionikanavareseptorin kautta kulkeutuvat ionit vaikuttavat hermosoluissa sijaitsevien jänniteherkkien kanavien toimintaan ja voivat synnyttää tai ehkäistä aktiopotentiaalin muodostumista. Ionikanavareseptorien vaikutus solujen ionitasapainoon on nopeampaa kuin esimerkiksi G-proteiinien välityksellä aktivoituvien ionikanavien. Lähde: Solunetti
- NAD+: Nikotiiniamidiadeniinidinukleotidi on kaikista elävistä soluista löytyvä kahdesta nukleotidista koostuva koentsyymi. Nikotiiniamidiadeniinidinukleotidi osallistuu hapetus-pelkistysreaktioon siirtämällä elektroneja reaktioiden välillä.NAD+ on hapettava tekijä – eli se vastaanottaa elektroneja muilta molekyyleiltä ja pelkistyy. Reaktiossa syntyy NADH, joka toimii pelkistävänä tekijänä luovuttaen elektroneja vastaanottaville molekyyleille.
(−) Antagonistit – Inflammaatiota lisäävät tekijät
- Alkoholi
- Tupakointi
- Nikotiiniamidi: Tämä on mielenkiintoista. Vaikuttaa siltä, että eräät niasiinien ryhmään kuuluvat B-vitamiinit hillitsevät tai lisäävät inflammaatiota.
PPAR alfa/gamma
PPAR säätelee rasva-aineenvaihduntaa. PPAR-agonistit ovat metabolisen oireyhtymän hoidossa käytettäviä lääkkeitä, jotka kohdistuvat PPAR-reseptoriin (peroxisome proliferator-activated receptor).
Peroksisomit ovat yksinkertaisen lipidikalvon ympäröimiä soluelimiä, joita on melkein kaikissa aitotumallisten soluissa. Peroksisomit osallistuvat tärkeisiin solun aineenvaihdunta- ja signalointitehtäviin.
PPAR-reseptorit ovat joukko tumareseptoriproteiineja, jotka toimivat transkriptiotekijöinä ja säätelevät geenien ilmentymistä (gene expression). Geenin ilmentyminen tarkoittaa geneettisen infromaation lukemista DNA:sta uuden proteiinin valmistuksen yhteydessä.
(+) Agonistit – Inflammaatiota vähentävät tekijät
- Polyfenolit: Polyfenolit ovat kasveissa esiintyviä antioksidantteja. Monet polyfenoleja runsaasti sisältävät ravintoaineet yhdistyvät sekä väestötutkimuksissa että satunnaistetuissa välimuuttujatutkimuksissa hyvään terveyteen. Tällaisia polyfenoleja ovat mm. neitsytoliiviöljy (fenoliset alkoholit: hydroksityrosoli, tyrosoli), omena (kversetiini: flavonoli), soija (genisteiini: isoflavoni), mustikka (antosyaanit, ferula- ja kahvihapot: fenolisia happoja), kahvi (klorogeenihappo: fenolinen happo).
- Sirtuiinit; kahvin sisältämä yhdiste hydroksyyli hydrokinoni (HHQ):”We show that coffee component HHQ has significant apoptotic effect on MDA-MB-231 and MCF-7 cells in vitro, and that ROS generation, change in mitochondrial membrane permeability, upregulation of Bax and Caspase-8 as well as down regulation of PGK1 and PKM2 expression may be important apoptosis-inducing mechanisms. The results suggest that PPARγ ligands may serve as potential therapeutic agents for breast cancer therapy. HHQ was also validated as a ligand for PPARγ by docking procedure.”
- Thiazolidinedione (TZD): TZD aktivoi PPAR-reseptoreita. Vapaat rasvahapot (FFA) ja eikosanoidit ovat reseptorien endogeenisiä (luonnostaan esiintyviä) ligandeja. Aktivoitu reseptori kiinnittyy DNA:han kompleksina, johon kuuluu toinen tumareseptori eli RXR-reseptori (retinoid X receptor). Aktivaatio lisää eräiden spesifien geenien transkriptiota ja vähentää toisten geenien transkriptiota.Keskeinen vaikutus on eräiden spesifien geenien ekspression ja repression säätely, jolloin rasvahappojen varastoiminen rasvasoluihin (adiposyytteihin) tehostuu ja vapaat rasvahapot vähenevät verenkierrosta.Tämän seurauksena solujen energiantuotanto hiilihydraattien ja erityisesti glukoosin oksidaatiosta tehostuu.
- Kannabinoidiagonistit: Kannabinoidireseptoreja esiintyy kaikkialla elimistössä osana endokannabinoidijärjestelmää. Tämä järjestelmä vaikuttaa moniin fysiologisiin mekanismeihin, kuten ruokahaluun, kivun aistimiseen, mielialaan ja muistiin.Kannabinoidiagonistit aktivoivat CB1- ja CB2-reseptoreita ja niitä käytetään lääkkeinä mm. kivun, anoreksian sekä oksentelun ja pahoinvoinnin hoidossa.Kannabinoidiagonisteja ja -antagonisteja käytetään lääkkeinä. Esimerkiksi Sativex, jota käytetään neuropaattisten kipujen lieventämiseen MS-taudissa.
- 15d PGJ2 eli anti-inflammatorinen prostaglandiini. Eikosanoidit ovat solujen välisessä parakriinisessä signaloinnissa toimivia molekyylejä. Eikosanoidit valmistetaan arakidonaatista, monityydyttämättömästä rasvahaposta, jota nisäkkäät tuottavat kasviravinnosta saatavasta linolaatista.Esimerkiksi hermoärsytys voi aiheuttaa sen, että fosfolipaasi alkaa hajottaa fosfolipidejä ja vapauttaa samalla arakidonaattia. sER:n entsyymit muuttavat arakidonaatin prostaglandiinien ja tromboksaanien yhteiseksi esiasteeksi ja edelleen prostaganiideiksi, jotka ovat tulehdusreaktioissa toimivia signalointimolekyylejä. Esimerkiksi ibuprofeenin ja aspiriinin toiminta perustuu näiden sER:llä tapahtuvien reaktioiden estämiseen.”In particular, 15d-PGJ2 is recognized as the endogenous ligand for the intranuclear receptor PPARgamma. This property is responsible for many of the 15d-PGJ2 anti-inflammatory functions. In this review, we summarize the current understanding of 15d-PGJ2 synthesis, biology and main effects both in molecular physiology and pathological states.”
NF-kB
NF-kB (nuclear factor kappa-light-chain-enchancer of activated B cells) on proteiinikompleksi, joka säätelee DNA:n transkriptiota, sytokiinien tuotantoa ja solun elinkaarta. NF-kB löytyy lähes kaikista soluista. Se osallistuu soluvasteisiin mm. sytokiinien, stressin, vapaiden happiradikaalien, raskasmetallien, ultraviolettisäteliyn, hapettuneen LDL-kolesterolin sekä patogeenien stimuloimana.
NF-kB on keskeinen vaikuttaja infektioiden aiheuttamassa immuunivasteessa. Häiriintynyt NF-kB:n toiminta assosioituu syöpiiin, tulehduksellisiin sairauksiin, autoimmuunitauteihin, virusinfektioihin, septiseen shokkiin sekä immuunijärjestelmän kehityshäiriöihin. NF-kB saattaa vaikuttaa myös synaptiseen plastisuuteen sekä muistiin.
NF-kB on merkittävä synnynnäiseen ja adaptiiviseen immuunijärjestelmään liittyviä geenejä säätelevä transkriptiotekijä
Koska NF-kB ohjaa monia inflammaatioon liittyviä geenejä, ei liene yllätys, että NF-kB on erityisen aktiivinen monissa tulehduksellisissa sairauksissa.
”It is important to note though, that elevation of some NF-κB activators, such as osteoprotegerin (OPG), are associated with elevated mortality, especially from cardiovascular diseases. Elevated NF-κB has also been associated with schizophrenia. Recently, NF-κB activation has been suggested as a possible molecular mechanism for the catabolic effects of cigarette smoke in skeletal muscle and sarcopenia.”Lähde: Wikipedia
(+) Agonistit: NF-kB-agonistit assosioituvat inflammaatioon
- Tyydyttyneet (kovat) rasvat ja transrasvat.
- Onkoproteiinit: Onkogeenien koodaamat proteiinit eli onkoproteiinit säätelevät solukasvua ja erikoistumista. NF-kB aktivoi onkoproteiineja, jotka altistavat syövälle. Onkogeenit ovat mutatoituneita geenejä, jotka voivat saada solun muodostamaan kasvaimen. Onkogeenit saavat kasvaimia aiheuttavat ominaisuutensa mutaatioiden kautta.Onkoproteiineja ovat:
– Kasvutekijän kinaasireseptorit, jotka muodostavat autofosforyloivia dimeerejä sopontaanisti ilman ligandia.
– Sytoplasman tyrosiinikinaasit, jotka fosforyloivat ylitehokkaasti. - ROS (Reactive oxygen species): Reaktiiviset happiradikaalit ovat hapesta muodostuvia yhdisteitä, jotka sisältävät parittoman elektronin ja ovat siksi hyvin reaktiivisia. Energiataloudellisesti parittomat elektronit ovat epäedullisia ja yhdiste pyrkii parilliseen elektronimäärään reagoimalla läheisyydessä olevien muiden yhdisteiden kanssa. Happiradikaali vaurioittaa kohtaamansa molekyylin rakennetta ja/tai toimintaa.Happiradikaaleja syntyy erityisesti soluhengityksessä, kun mitokondrioiden elektroninsiirtoketju käytää happea energiantuotannossa. Soluhengitys kuluttaa suurimman osan hengitysilman mukana elimistöön tulevasta hapesta, mutta sivutuotteena prosessista syntyy superoksidianionia sekä pieniä määriä muita happiradikaaleja. Myös hapetus-pelkistysreaktioita katalysoivien oksidoreduktaasien sekä elimistölle haitallisia aineita tuhoavien sytokromi P450-entsyymien toiminta tuottaa jonkin verran reaktiivisia happiradikaaleja.
- TNF-α: Tuumorinekroositekijä alfa on tulehdusreaktion syntyyn vaikuttava välittäjäaine eli sytokiini. TNF-alfa on lähinnä makrofagien erittämä proteiini, joka osallistuu tulehdusreaktion ohella monenlaisiin biologisiin prosesseihin, kuten solunjakautumiseen, solujen erilaistumiseen, apoptoosiin (ohjattuun solukuolemaan), rasva-aineiden metaboliaan ja verihyytymän muodostukseen. TNF-alfalla on havaittu olevan osuutta mm. autoimmuunisairauksissa, insuliiniresistenssissä ja syövässä. TNF-alfan vasta-aine on infliksimabi.” TNF-alfa sekä sen solukalvon läpäisevä TNF-alfareseptori ovat kolmesta osasta kohdistuvia eli trimeerisiä proteiineja. TNF-alfan sitoutuminen solukalvon pinnalla olevaan TNF-alfareseptoriin johtaa reseptorin soluliman puoleisten osien asennon Tällöin soluliman puoleiset osat voivat aktivoida erilaisia viestimekanismeja, jotka johtavat edelleen seriini/treoniinikinaasien aktivoitumiseen. Aktivoituneet seriini/treosiinikinaasit fosforyloivat IκB-kinaasin (IKK), jolloin se aktivoituu. Fosforyloitu IκB-kinaasi liittää IκB-proteiinin kahteen seriinitähteeseen fosfaattia. Tämä fosforylaatio johtaa ubikitiinin liittämiseen IκB-proteiiniin. Proteasomit tunnistavat ubikitinoidun IκB:n ja hajottavat sen. Tällöin IκB:n solulimaan sitoma NFκB-proteiini vapautuu sen otteesta ja kulkeutuu tumaan. Tumassa NFκB yhdessä muiden proteiinien kanssa lisää kohdegeeniensä luentaa eli transkriptiota.” Lähde: Wikipedia
- IL-1b: Interleukiini 1 beeta (IL1β) on sytokiiniproteiini, jota koodaa IL1B geeni. Interleukiini 1 beeta on merkittävä aktivoitujen makrofagien erittämä tulehdusvälittäjäaine. Se osallistuu solujen säätelyyn, kuten lisääntymiseen (proliferaatio), erikoistumiseen ja apoptoosiin.Interleukiinit ovat proteiineja ja peptidejä, jotka auttavat valkosoluja kommunikoimaan. Interleukiineja tuottavat pääasiassa auttaja-T-solut, monosyytit, makrofagit ja endoteelisolut. Interleukiinit edistävät T- ja B-solujen lisääntymistä ja vaikuttavat immuunivasteeseen. Toisaalta interleukiinit edistävät inflammaatiota ja aiheuttavat suurina määrinä kuumeen.Interleukiini 1 (IL-1) on makrofagien, fibrosyyttien ja T-lymfosyyttien tuottama pieni proteiini, jonka tehtävänä on vahvistaa makrofagien kykyä tappaa mikro-organismeja ja aktivoi auttaja-T-lymfosyyttejä. IL-1 vaikuttaa myös elimistön lämmönsäätelykeskukseen, jossa se saa aikaan ruumiinlämmön kohoamisen. Indusoi akuuttia tulehdusta.Interleukiini 1 beeta ja IL-1 antagonistireseptori (IL-1RN) geenin polymorfismit assosioituvat haavaiseen paksusuolen tulehdukseen.
- LPS (Lipopolysaccharides): Lipopolysakkaridit tunnetaan myös polyglykaaneina ja endotoksiineina. Ne ovat suuria lipidistä ja polysakkarideista muodostuvia molekyylejä.Endotoksiinit ovat gramnegatiivisten bakteerien ulkokalvon sisältämiä myrkkyaineita, jotka vapautuvat bakteerin hajotessa. Endotoksiineilla viitataan usein lipopolysakkaridiin (LPS), jonka lipidi A-osa aiheuttaa infektion aikana isäntäelimistössä toksisia reaktioita: kuumetta, valkosolujen ja verihiutaleiden niukkuutta sekä mahdollisesti shokin (endotoksiinishokki).Endotoksiineja ovat myös Bacillus thuringiensis-bakteerin delta-endotoksiinit, jotka ovat kiteisiä proteiineja.
- Virusten aiheuttamat infektiot: Infektiotaudit ovat virusten, bakteerien tai sienten aiheuttamia tulehdustiloja. Infektiotauteja ei aiheuta kylmettyminen, vetoisuus, stressi, valvominen, vitamiinipuute tai huono ruokavalio; infektiotauteja aiheuttavat aina mikrobit.Infektiotaudeille on ominaista tulehdusreaktion syntyminen. Tulehdusreaktioon liittyy valkosolujen ilmaantuminen ja lisääntyminen infektiokohdassa ja verenkierrossa. Valkosolut erittävät tulehdushormoneja, sytokiinejä, jotka saavat aikaan yleisoireina esimerkiksi kuumeen nousun, lihassärkyä ja huonon olon. Oireet eivät niinkään johdu itse mikrobista, vaan sen aiheuttamasta elimistön reaktiosta.Virukset ovat millimetrin tuhannesosan kokoisia proteiineista ja geeneistä muodostuvia rakenteita, jotka esimerkiksi hengitysteihin tai suolistoon tunkeuduttuaan aihauttavat tulehdusreaktion. Virusten infektoimat solut alkavat infektion seurauksena erittää tulehdusvälittäjäaineita, mikä aiheuttaa nuhaa, yskää, ripulia tai oksentelua. Limakalvon soluissa virukset monistuvat ja syntyvät uudet virukset leviävät verenkiertoon ja infektoivat uusia soluja. Antibiootit eivät tehoa viruksiin.Bakteerit ovat yleensä satoja kertoja viruksia suurempia ja muistuttavat rakenteeltaan ihmisen omia soluja. Bakteerit eroavat ihmisen omista kudoksista mm. vahvan, bakteeria suojaavan seinämän perusteella. Monet antibiootit tuhoavat bakteereita tuhoamalla bakteerien vahvan seinän. Tavallisimpia infektioita aiheuttavia bakteereita on alle kymmenen eri lajia. Yleisimmät infektioita aiheuttavat bakteerit ovat: pneumokokki, hemofilus, streptokokki, stafylokokki ja branhamella.
(−) NF-kB-antagonistit hillitsevät inflammaatiota
- Kaloreiden rajoittaminen eli vähäenerginen ravinto
- Polyfenolit
- n-3 PUFA: Monityydyttämättömät (PUFA) omega-3 rasvahapot eli alfalinoleenihappo.
- Butyraatti: Suoliston hyvät mikrobit, kuten bifidobakteerit ja laktobasillit tuottavat kaasua syömällä imeytymättömiä fermentoituvia hiilihydraatteja. Kaasua synnyttävässä prosessissa syntyy suolisto- ja kokonaisterveyttä edistäviä lyhytketjuisia rasvahappoja (SCFA). Näitä ovat asetaatti, propionaatti ja butyraatti. Lyhytketjuisilla rasvahapoilla on havaittu suoliston inflammaatiota, infektioita ja syöpiä ehkäiseviä vaikutuksia. Ne myös auttavat suoliston pintaa uusiutumaan ja pysymään terveenä.
- Sirtuiinit
LXR (Liver X receptor)
LXR on tumareseptori ja transkriptiotekijä. Se muistuttaa läheisesti PPAR-, FXR ja RXR-reseptoreita. LXR-reseptorit osallistuvat kolesterolin, rasvahappojen ja glukoosin homeostaasin säätelyyn.
(+) LXR-Agonisteja
- Omega-6 monityydyttämättömät rasvahapot (PUFA):Omega-6 eli linolihappo on toinen kehon välttämättä tarvitsemista rasvahapoista. Toinen on omega-3 eli alfalinoleenihappo. Elimistö tarvitsee linolihappoa mm. ihon kunnon ylläpitämiseen. Sekä omega-6 että omega-3 rasvoja tarvitaan solukalvojen rakennusaineina sekä eikosanoidien lähtöaineina. Eikosanoidit ovat yhdisteitä, jotka säätelevät elimistössä esimerkiksi verenpainetta, veren hyytymistä, immuunivastetta ja tulehdustilaa.Matala-asteinen tulehdus assosioituu moniin sairauksiin. Monet omega-3 rasvahapoista tuotettavat eikosanoidit lievittävät tulehdusreaktioita, kun taas omega-6 rasvahapoista tuotettavat eikosanoidit osallistuvat veren hyytymisen säätelyyn sekä tulehdustilan ylläpitoon. Toisaalta omega-6 rasvat voivat myös hillitä tulehdusreaktioita.” Ylenmääräinen omega-6 rasvahappojen saanti suhteessa omega-3 rasvahappojen saantiin tai toisinpäin voi mahdollisesti estää toisen ryhmän rasvahappojen hyödyntämistä elimistössä. Näiden syiden takia on ajateltu, että runsas omega-6 rasvahappojen saanti voisi edistää tulehdusreaktioita. Tutkimuksissa runsas omega-6 rasvahappojen saanti ei ole kuitenkaan johdonmukaisesti johtanut tulehdustekijöiden lisääntymiseen tai vähenemiseen. Lisäksi on viitteitä siitä, että paitsi omega-3 rasvahappojen saanti myös linolihapon saanti ja omega-6 rasvahappojen riittävä pitoisuus verenkierrossa ovat yhteydessä pienempään sydän- ja verisuonisairauksien riskiin. Omega-3 ja omega-6 rasvahappojen saannin suhteella ei ole havaittu yhteyttä sydänsairauksien riskiin.” Lähde: Sydän.fi
- Oxysterolit: Oxysterolit muodostuvat hapettuneesta kolesterolista. Niiden uskotaan vaikuttavan mm. ateroskleroosiin syntyyn ja etenemiseen.”Oxygenated derivatives of cholesterol (oxysterols) present a remarkably diverse profile of biological activities, including effects on sphingolipid metabolism, platelet aggregation, apoptosis, and protein prenylation.The most notable oxysterol activities center around the regulation of cholesterol homeostasis, which appears to be controlled in part by a complex series of interactions of oxysterol ligands with various receptors, such as the oxysterol binding protein, the cellular nucleic acid binding protein, the sterol regulatory element binding protein, the LXR nuclear orphan receptors, and the low-density lipoprotein receptor. Identification of the endogenous oxysterol ligands and elucidation of their enzymatic origins are topics of active investigation.” PubMed
(−) LXR-antagonisteja
- Omega-3 monityydyttämättömät rasvahapot (PUFA). Omega-3 eli alfalinoleenihappo on monien eikosanoidien esiaste ja sillä uskotaan olevan inflammaatiota hillitseviä vaikutuksia.
SREBP-1c (Sterol regulatory element-binding protein 1)
Proteiini, jota ihmisillä koodaa kromosomissa 17 sijaitseva SREBF1-geeni. SREBF1-geenin transkriptiovariantit koodaavat kahta erilaista isoformia: SREBP-1a ja SREBP-1c. Geenin koodaamat proteiinit ovat transkripitotekijöitä, jotka kiinnittyvät DNA:n promoottorisekvenssiin (sterol regulatory element-1; SRE1).
SREBP-1c säätelee geenejä, joita tarvitaa glukoosin aineenvaihdunnassa ja lipidien valmistuksessa. Sen ilmenemistä säätelee insuliini. SREBP-1a säätelee geenejä, jotka liittyvät lipidien ja kolesterolin valmistukseen; sem aktiivisuutta säätelee solun sterolitasot.
”Insulin, cholesterol derivatives, T3 and other endogenous molecules have been demonstrated to regulate the SREBP1c expression, particularly in rodents. Serial deletion and mutation assays reveal that both SREBP (SRE) and LXR (LXRE) response elements are involved in SREBP-1c transcription regulation mediated by insulin and cholesterol derivatives. Peroxisome proliferation-activated receptor alpha (PPARα) agonists enhance the activity of the SREBP-1c promoter via a DR1 element at -453 in the human promoter. PPARα agonists act in cooperation with LXR or insulin to induce lipogenesis.” Lähde: Wikipedia
SREBF1 vuorovaikuttaa ainakin seuraavien kanssa:
- CREB-binding protein,
- DAX1
- LMNA
- TWIST2
- BHLHE40
- BHLHE41
(+) SREBP-1c-agonisteja
- LXR: LXR-reseptorit osallistuvat kolesterolin, rasvahappojen ja glukoosin homeostaasin säätelyyn.
- Suoliston dysbioosi
- Alkoholi
- Insuliini
(−) SREBP-1c-antagonisteja
- n-3 PUFA: Omega-3 rasvahapot
- Metformiini: Diabeteslääke, joka voi hillitä myös inflammaatiota.
- Sirtuiinit
- AMPK
SREBP-2 (sterol regulatory element-binding proteins)
SREBP-2 on transkriptiotekijä, joka säätelee kolesterolin aineenvaihduntaan osallistuvia geenejä. SREB proteiineja tarvitaan kolesterolisynteesiin.
”This gene encodes a ubiquitously expressed transcription factor that controls cholesterol homeostasis by stimulating transcription of sterol-regulated genes. The encoded protein contains a basic helix-loop-helix leucine zipper (bHLH-Zip) domain. Various single nucleotide polymorphisms (SNPs) of the SREBF2 have been identified and some of them are found to be associated with higher risk of knee osteoarthritis. SREBF2 has been shown to interact with INSIG1 and CREB-binding protein.” Lähde: Wikipedia
(−) SREBP-2-antagonisteja
- LXR
- Statiinit
ChREBP (Carbohydrate-responsive element-binding protein)
ChREBP eli MLXIPL on proteiini, jota ihmisillä koodaa MLXIPL-geeni. ChREBP vuorovaikuttaa hiilihydraatteja säätelevään DNA-sekvenssiin. ChREBP siirtyy solun tumaan ja kiinnittyy DNA:han fosforylaation jälkeen.
”Although the regulation of ChREBP remains unknown in detail, the transactivity of ChREBP is partly regulated by a phosphorylation/dephosphorylation mechanism. During fasting, protein kinase A and AMP-activated protein kinase phosphorylate ChREBP and inactivate its transactivity. During feeding, xylulose-5-phosphate in the hexose monophosphate pathway activates protein phosphatase 2A, which dephosphorylates ChREBP and activates its transactivity. ChREBP controls 50% of hepatic lipogenesis by regulating glycolytic and lipogenic gene expression. In ChREBP (-/-) mice, liver triglyceride content is decreased and liver glycogen content is increased compared to wild-type mice. These results indicate that ChREBP can regulate metabolic gene expression to convert excess carbohydrate into triglyceride rather than glycogen.” PubMed
Liiallinen hiilihydraattien saanti johtaa rasvan kerääntymiseen ja insuliiniresistenssiin. Glukoosi ja insuliini säätelevät glukoosin de novo lipogeneesiä maksassa. Insuliini aktivoi useita transkriptiotekijöitä, kuten SREBP1c ja LXR. ChREBP kiinnittyy DNA:ssa hiilihydraatteja säätelevän sekvenssin (ChoRE) promottorialueelle, jossa sen kohteena on glykolyysiä, lipogeneesiä ja glukoneogeneesiä säätelevät geenit
”This gene encodes a basic helix-loop-helix leucine zipper transcription factor of the Myc / Max / Mad superfamily. This protein forms a heterodimeric complex and binds and activates, in a glucose-dependent manner, carbohydrate response element (ChoRE) motifs in the promoters of triglyceride synthesis genes.”
(+) ChREBP-agonisteja
- Glukoosi
(−) ChREBP-antagonisteja
- LXR
- Statiinit
PPAR = peroxisome proliferator-activated receptor;
LXR = liver X receptor; RXR = retinoid X-receptor;
NF-kB = nuclear transcription factor-kB;
SREBP = steroid regulatory element-binding protein;
ChREBP = carbohydrate responsive element-binding protein;
Sirtuins = SIRT-1/2, deacetylating enzymes;
AMPK = AMP-activated protein kinase;
n-3 PUFA = omega-3 polyunsaturated fatty acids.
Selityksiä: kaloreiden rajoittaminen
Sirtuiinit löydettiin tämän vuosituhannen alussa. Jo 1930-luvulta asti on tosin tiedetty, että ravinnosta saatavan energian rajoittaminen pidentää jyrsijöiden elinikää. Energiamäärä, joka on 60-70 % normaalista vaikuttaa suotuisasti elimistön toimintaan.
Sirtuiinit
Energiansaannin rajoittaminen laskee kehon lämpötilaa, pudottaa painoa ja rasvamäärää sekä vähentää insuliini- ja glukoosipitoisuutta. Saadun energian määrällä vaikuttaa olevan suurempi merkitys kuin sillä mistä energia saadaan. (Guarante ja Picard, 2005).
Vähäinen energiansaanti vaikuttaa oksidatiivista stressiä hillitsevästi. Eläinkokeissa energiansaannin rajoittaminen on suojannut laboratorioeläimiä monilta ikään liittyviltä sairauksita sekä diabetekselta ja syöviltä. Vaikuttaa siltä, että vähäinen energiansaanti johtaa aineenvaihdunnan sopeutumismekanismeihin, joissa SIR2-geeni (silent information regulator 2, sirtuiini) on keskeisessä osassa.
Sirtuiinit ovat NAD+:sta riippuvaisia proteiiniasetylaaseja. Nämä entsyymit pidentävät hiivojen elinikää 70 %, matojen elinikää 15-40 %, hyönteisten elinikää 30 % ja hiirien elinikää 30 % (Denu 2005). Sirtuiinit säätelevät myös solujen ohjattua kuolemaa eli apoptoosia, tulehdusvastetta, solujen elämänkaarta, geenitranskriptiota ja aineenvaihduntaa.
Sirtuiineja on seitsemän:
SIRT1: Tumassa sijaitseva deasetylaasi, joka säätelee aineenvaihduntaa ja elinikää.
SIRT2: Solulimassa sijaitseva deasetylaasi, joka vaikuttaa syövän syntyyn.
SIRT3: Mitokondrioissa sijaitseva deasetylaasi, joka osallistuu aineenvaihduntaan.
SIRT4: Mitokondrioissa sijaitseva deasetylaasi, joka osallistuu aineenvaihduntaan ja säätelee aminohappovälitteistä insuliinin eritystä.
SIRT5: Mitokondriossa sijaitseva deasetylaasi.
SIRT6: Tumassa esiintyvä sirtuiini.
SIRT7: Tumassa esiintyvä sirtuiini.
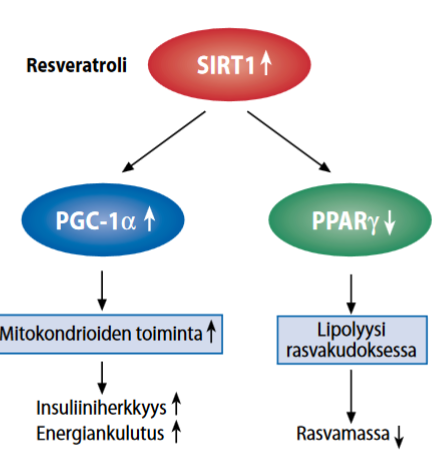
Entiten tutkitulla SIRT1-sirtuiinilla on huomattava rooli aineenvaihdunnan kannalta tärkeissä kudoksissa, kuten haimassa, maksassa ja rasvakudoksessa. SIRT1 säätelee erityisesti mekanismeja, jotka liittyvät ikääntymiseen ja energiansäätelyyn paaston tai niukkaenergisen ruokavalion aikana. SIRT1-aktivaatio voi lisätä insuliiniherkkyyttä sekä laskea insuliini- ja glukoosipitoisuuksia.
SIRT1 on PPARϓ:n estäjä, joka aiheuttaa lipolyysin kiihtymisen rasvakudoksessa ja vähentää näin rasvakudoksen määrää. SIRT1 lisää insuliinin eritystä haimasta ja suojaa haiman beetasoluja oksidatiiviselta stressiltä (Moynihan ym. 2005). Maksassa SIRT1:n aktivaatio lisää glukoosin uudismuodostusta PCG-1α:n aktivoitumisen kautta. Lähde: Sirtuiinit – energiatasapainon ja glukoosimetabolian uudet molekyylit, Markku Laakso
Kuinka ravinto ja elintavat vaikuttavat MS-taudin etenemiseen? Osa 3 julkaistaan Ruokasodassa huhtikuun vaihteen tienoilla. Tässä lienee pureskeltavaa vähäksi aikaa.




