Ketogeeninen ruokavalio & PPMS
Aivan viime aikoihin asti multippeliskleroosia on pidetty ensisijaisesti tulehduksellisena autoimmuunitautina. Lähes täysin huomiotta on jäänyt tautiin liittyvä neurodegeneratiivinen komponentti, joka vaikuttaa sairauden etenemiseen ja invaliditeettiin.
Löysin hyvin kiinnostavan tutkielman vuodelta 2015. Mithu Storonin ja Gordon T. Plantin kirjoittama The Therapeutic Potential of the Ketogenic Diet in Treating Progressive Multiple Sclerosis selvittää ketogeenisen ruokavalion terapeuttista vaikutusta ensisijaisesti etenevää multippeliskleroosia sairastavilla.
Perinteistä kuvaa MS-taudista haastavat kliiniset havainnot tulehduksen ja neurodegeneraation välisestä dissosiaatiosta, jossa neurodegeneratiivisella komponentilla saattaa olla tulehduksellisia tekijöitä merkittävämpi rooli taudin patogeneesissä.
Tässä katsauksessa tutkitaan mitokondrioiden toimintahäiriöiden ja hermoston rappeutumisen suhdetta multippeliskleroosissa. Tarkastelemme todisteita siitä, että ketogeeninen ruokavalio voi korjata mitokondrioiden toimintaa, ja pohdimme ketogeenisen ruokavalion terapeuttista potentiaalia etenevän multippeliskleroosin hoidossa.
Kaikkiin potentiaalisiin terapeuttisiin vaihtoehtoihin tutustuminen on perusteltua, koska etenevään MS-tautiin ei tällä hetkellä tunneta parantavaa tai edes taudin etenemistä hidastavaa hoitoa.

1. Survival of the sickest? Multippelisklerootikko ketoosissa
Näyttö ketogeenisen ruokavalion neurologisista hyödyistä kasvaa nopeasti. Lääkeresistenttiä epilepsiaa on hoidettu ketogeenisellä ruokavaliolla jo vuosisadan ajan. Tutkimuksissa ketogeenisen ruokavalion terapeuttisista hyödyistä Parkinsonin taudin ja Alzheimerin taudin hoidossa on saatu erittäin lupaavia tuloksia.
Löysin hiljattain useita tutkimuksia, jotka tukevat ketogeenisen ruokavalion terapeuttisia hyötyjä multippeliskleroosia sairastavilla. Tämä on uusi pohjaton kaninkolo, johon aion kompastua. Ehkäpä meidän kaikkein sairaimpienkin horisontissa voi nähdä sateenkaaren ja lupauksen paremmasta? Minä en lupaa mitään, mutta katsotaan millainen maailma peilin takana odottaa.
Jean-Martin Charcotin huolellinen kliininen ja patologinen kuvaus potilaasta, jolla oli demyelinoivia leesioita tai “sclérose en plques” vuonna 1868, antoi maailmalle ensimmäisen selkeän kuvauksen multippeliskleroosista (MS).
Puolitoista vuosisataa Charcotin havaintojen jälkeen, taudin patogeneesi on yhä suurelta osin mysteeri. Primaaristi progressivisen, eli ensisijaisesti etenevän multippeliskleroosin hoito ei ole oireenmukaisia hoitoja paitsi edistynyt käytännössä lainkaan.
Arviolta 85 prosentilla MS-potilaista esiintyy toistuvia yksittäisten neurologisten oireyhtymien jaksoja, jotka yleensä häviävät konservatiivisella hoidolla täysin tai lähes täysin. Tätä tautimuotoa kutsutaan relapsoivaksi remittoivaksi tai aaltoillen eteneväksi MS-taudiksi (RRMS).
Noin 15 prosentilla potilaista on asteittainen ja progressiivinen neurologisen toiminnan menetys, joka ei parane. Tätä tautimuotoa kutsutaan primaaristi progressiiviseksi MS-taudiksi (PPMS). Vaikka tautimuodoissa on yhtäläisyyksiä, ne eroavat toisistaan kuin yö ja päivä.
Vaikuttaa siltä, että RRMS on tulehduksellinen autoimmuunitauti ja PPMS neurodegeneratiivinen hermosoluja tuhoava sairaus. Minä olen invalidisoitunut tämän ilman pahenemis- ja paranemisvaiheita etenevän etenevän ms-taudin luomassa kuplassa vuodesta 2008.
Potilaista, joilla on RRMS, suurimmalle osalle kehittyy progressiivisia neurologisia oireita 1-3 vuosikymmentä ms-diagnoosin jälkeen. Tätä tautimuotoa nimitetään toissijaisesti eteneväksi MS-taudiksi (SPMS). Se muistuttaa ensisijaisesti etenevää MS-tautia.
Multippeliskleroosia on perinteisesti pidetty immuunivälitteisenä tulehdussairautena. Immuunivasteen uskotaan aiheuttavan spontaanisti remisoituvia relapseja RRMS:ssä.
Perinteisen näkemyksen mukaan immuunisolut kulkeutuvat vaurioituneen veri-aivoesteen läpi ja aiheuttavat RRMS:lle tyypillisen fokaalisen ja levinneen tulehduksen. Perinteinen näkemys multippeliskleroosista tulehdussairautena on johtanut siihen, että lähes kaikissa terapeuttisissa strategioissa käytetään immunomoduloivaa tai immunosuppressiivista lähestymistapaa. Lähestymistapa toimii aaltoilevaa ms-tautia sairastavilla, mutta siitä ei ole mitään apua etenevää ms-tautia sairastavien hoidossa.
Näkemys multippeliskleroosista tulehduksellisena sairautena on riittämätön, koska fokaalinen tulehdus voi puuttua etenevää tautimuotoa sairastavilta. Neurodegeneraatiolla voi olla keskeisempi rooli etenevän MS-taudin patogeneesissä.
Tulehduksen ja taudin etenemisen välisen dissosiaation todisteiden lisääntyminen ellyttää tarkistettua näkökulmaa neurodegeneraation roolista multippeliskleroosin patogeneesiin ja siten terapeuttisisten strategioiden uudelleenarviointia.
Tässä katsauksessa tutkimme todisteita hermoston rappeutumisesta ja muuttujista etenevän ms-taudin patogeneesissä. Samalla arvioidaan ketogeenisen ruokavalion toimivuutta etenevän multippeliskleroosin hoitomuotona.
Minä aloitin ketogeenisen ruokavalion joulukuun toisena päivänä torjuakseni alkavan diabeteksen. Huomasin pian oloni energisemmäksi ja aktiivisemmaksi. Söin vähemmän, mutta jaksoin enemmän. Painoni putosi muutamassa kuukaudessa 10 kg. Verensokeri laski esidiabeettiselta tasolta optimaaliselle tasolle. Aiemmin korkea verenpaineeni on nyt melko hyvä. Kaiken kaikkiaan minulle tämä ruokavalio on tehnyt hyvää.

2. Onko MS ensisijaisesti neurodegeneratiivinen sairaus?
Perinteinen MS-malli perustuu ”ulkopuolelta-sisään” -tulkintaan. Tässä mallissa virheellisesti toimiva immuunijärjestelmä hyökkää keskushermostoa vastaan. Oletus on, että jokin tai jotkin ulkoiset tekijät laukaisevat tulehduksen, joka johtaa autoimmuunireaktioon ja taudille ominaisiin vaurioihin keskushermostossa.
Perifeeriset immuunisolut läpäisevät vaurioituneen veri-aivoesteen päästäkseen keskushermostoon, jossa ne aiheuttavat akuutteja multifokaalisia tulehduksellisia vaurioita Vauriot ovat joskus oireettomia, mutta yleensä ne liittyvät pahenemisvaiheeseen eli relapsiin aaltoilevasti etenevässä RRMS:sä. Pahenemisvaiheisiin liittyy erilaisia neurologisia oireita.
RRMS on yleisin multippeliskleroosin muoto, mutta suurimmalle osalle aaltoilevasti etenevää tautimuotoa sairastavista potilaista kehittyy multippeliskleroosin toissijaisesti progressiivinen muoto (SPMS) kolmen vuosikymmenen sisällä taudin puhkeamisen jälkeen.
Tulehduksellisten ja neurodegeneratiivisten komponenttien kaksinaisuuden tekee kiinnostavaksi havainto, että MS ”etenee” molemmissa tautimuodoissa osittain yhteneväisellä tavalla riippumatta siitä, sairastuiko potilas aluksi aaltolevasti etenevään tautimuotoon vai ensisijaisesti etenevään tautiin. Patofysiologisesti näiden kahden taudifenotyypin välillä ei löydy eroa.
2.1. Vaihtoehtoinen MS-malli
Todisteet taudin etenemisen ja tulehduksen erillisestä dissosiaatiosta ovat haastaneet perinteisen lähestymistavan. Eteneminen ilman autoimmuunikohtauksia on osoitus erillisestä ja/tai rinnakkaisesta patogeenisestä prosessista.
Jotkut tutkijat ovat ehdottaneet multippeliskleroosiin ”sisältä-ulospäin” -mallia, jossa primaarinen solujen rappeuma on käynnistävä tekijä, joka sitten laukaisee tulehduksen. Rappeuma vapauttaa antigeenisen soluaineen, joka sitten johtaa immuunivasteeseen.
2.2. Tulehduksen pysäyttäminen ei pysäytä taudin etenemistä
Vaikka toistaiseksi ei ole pitävää näyttöä siitä, että solujen rappeuma olisi tulehduksen laukaiseva ensimmäinen tapahtuma (ikivanha muna- vai kana-kysymys), kliiniset havainnot tukevat näiden kahden välistä dissosiaatiota, jossa rappeuma ei seuraa tulehdusta, vaan voi tapahtua tulehduksesta riippumatta.
Tulehduksiin vaikuttavalla immuunimoduloivalla hoidolla ei ole juurikaan merkitystä multippeliskleroosin etenemiseen hyvin pitkällä aikavälillä, vaikka aaltoilevasti etenevän tautimuodon pahenemisvaiheiden hoitona immuunimoduloiva lääkitys toimiikin hyvin.
Autologinen hematopoieettinen kantasolusiirtoihin perustuva hoito on erittäin tehokas tulehduksen vähentämisessä, mutta sekään ei pysäytä aksonien rappeutumista ja aivojen atrofiaa. MS-taudissa tapahtuu progressiivista hermoston rappeutumista ja aksonien atrofiaa tulehduksellisista tekijöistä riippumatta.
Atrofiatarkoittaa solun koon pienenemistä sen rakenneosien vähenemisen seurauksena. Atrofioituvassa solussa rakenneproteiinien hajotus on nopeampaa kuin niiden synteesi. Elimen tasolla atrofialla voidaan tarkoittaa myös kudoksen tai elimen surkastumista, joka saattaa johtua solujen pienenemisen ohella niiden määrän vähenemisestä. Atrofian vastakohta on hypertrofia.
Atrofian taustalla on solujen pyrkimys sopeutua muuttuneisiin ympäristöolosuhteisiin ja säilyä hengissä. Elimen atrofiaa voi aiheuttaa myös vanhenemiseen liittyvä lisääntynyt apoptoosi, eli ohjattu solukuolema.
Atrofian mahdollisia aiheuttajia ovat solun vähentynyt aktiivisuus, hermotuksen heikentyminen, verenkierron tai ravintoaineiden riittämättömyys, hormonitoiminnan muutos ja lisääntynyt paine kudoksessa.
2.3. Harding-oireyhtymä
Teorian tueksi on olemassa patologista näyttöä, joka osoittaa että neurodegeneraatio voi tapahtua ilman mitään edeltävään tulehdukseen viittaavia todisteita. Myeliinivaipan sisäkerroksista on tunnistettu pistemäisiä vaurioita, vaikka myeliinivaipan ulkokerrokset ovat ehjät.
Tämä haastaa T-soluvälitteisen ulkoisen mekanismin mahdollisuuden. Harding-oireyhtymässä on todisteita siitä, että neurodegeneraatio edeltää tulehdusreaktiota. Vastaava perinnöllinen mitokondrioiden toimintahäiriö voi aiheuttaa MS-taudissa havaitun atrofian ja neurodegeneraation.
Harding-oireyhtymässä solujen rappeuma, joka ilmenee mitokondrioiden viallisen toiminnan seurauksena, voi laukaista autoimmuunivasteen ihmisillä, joilla on immunologinen ja geneettinen alttius ko. Oireyhtymälle.
Vaikka Leberin perinnöllinen optinen neuropatia (LHON) on tavallisempi miehillä, naisilla on suurempi riski saada autoimmuunisairaus, ja tämä voi selittää, miksi naisilla esiintyy enemmän Harding-oireyhtymää multippeliskleroosin kaltaisen tulehduksen kanssa, vaikka kyseessä on sama mutaatio kuin LHON.
Leberin perinnöllinen optinen neuropatia (LHON) on mitokondriaalisesti perinnöllinen häiriö, jolle on ominaista kivuton näköhäiriö, joka voi johtaa vakavaan optisen atrofiaan. Se voi liittyä muihin sairauksiin, kuten multippeliskleroosiin (MS).
LHON:n liittymistä MS:n kaltaiseen sairauteen kutsutaan usein Hardingin taudiksi (tai Hardingin oireyhtymäksi).

3. Mitokondrioiden rooli multippeliskleroosissa
Kliininen näyttö, jonka mukaan MS-tudin neurologisiin vaurioihin vaikuttaa sekä neurodegeneraatio että inflammaatio kasvaa koko ajan riippumatta siitä, laukaiseeko neurodegeneraatio tulehduksen vai tulehdus neurodegeneraation. Sekin on mahdollista, että kyse on rinnakkaisista tautitapahtumista.
Mitokondrioiden toimintahäiriöillä uskotaan kuitenkin olevan keskeinen rooli neurodegeneratiivisessa tapahtumissa. Kasvava näyttö osoittaa, että mitokondrioiden toimintahäiriöillä voi olla myös huomattava merkitys MS-taudin patogeneesissä.
3.1. Mitokondrioiden virheellinen toiminta voi selittää aksonien kohtalon
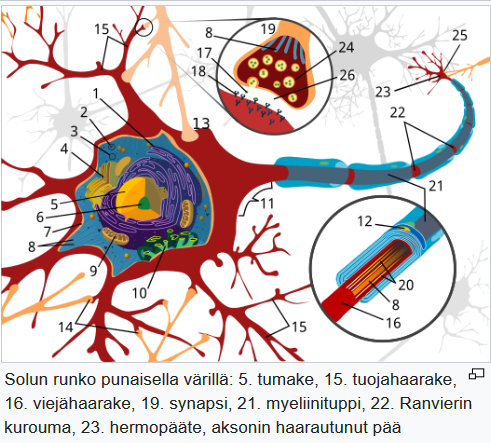
Aksoni, eli viejähaarake (hermosyy) on hermosolun eli neuronin osa, joita on vain yksi neuronia kohti, kun taas tuojahaarakkeita eli dendriittejä on useita yhdessä neuronissa.
Aksoni haarautuu loppupäästään ja muodostaa näin useita hermopäätteitä, jotka puolestaan voivat muodostaa synapsin toisen hermosolun tai lihassolun kanssa. Aksoni voi olla joko myelinisoitunut tai myelinisoitumaton. Myelinisoituneessa aksonissa hermoimpulssi kulkee nopeammin kuin myelinisoitumattomassa, koska hermoimpulssi hyppii myeliiniin muodostuneiden Ranvierien kuroumien välillä. – Wikipedia
Aksonaalinen rappeutuminen on multippeliskleroosille tunnusomainen piirre ja sitä esiintyy jopa ilman paikallista demyelinaatiota. Eläinmallit viittaavat siihen, että mitokondrioiden vaurio voi olla aksonin rappeutumista edeltävä tautitapahtuma.
Reaktiivisten happiradikaalien (ROS) muodostuminen voi myötävaikuttaa aksonien mitokondriovaurioihin. Reaktiivisten happiradikaalien detoksifikaatio voi puolestaan pysäyttää aksonin rappeutumisen.
Rappeutuvien aksonien katsotaan sisältävän toimintahäiriöisiä mitokondrioita, kun taas demyelinaatiosta selviytyvät aksonit sisältävät toimivia mitokondrioita. Nämä havainnot vastaavat äskettäistä tutkimusta glaukomatoottisesta optisesta neuropatiasta, jossa havaittiin, että terveet mitokondriot voivat tarjota suojaa hermoston rappeutumiselta huolimatta korkean silmänsisäisen paineen läsnäolosta.
Demyelinaatiota seuraava aksonien rappeutuinen aiheutuu nykykäsityksen mukaan mitokondrioiden tuottaman energian vähyydestä. Mitokondrioiden toiminta näyttää säätelevän aksonien kohtaloa.
Demyelinaatio: Myeliinikato on MS-taudille tyypillinen myeliinivaurio (myeliini on nopeasti johtavia hermosyitä ympäröivän, eristävän hermotupen rasva-aine).
3.2. Mitokondrioiden toimintahäiriö havaitaan harmaassa aineessa
Harmaan aineen atrofia on multippeliskleroosille tunnusomainen kliininen havainto. Atrofia lisääntyy, kun RRMS-tautimuoto etenee SPMS-tautimuodoksi. Immunohistokemiallisilla värjäystekniikoilla ja mikroskopialla on osoitetettu, että hermosolujen atrofia lisääntyy demyelinaatiosta riippumatta myös aivojen alueilla, joilla on ”terveeltä äyttävää harmaata ainetta”.
MS-taudissa aivokuoren neuronien mitokondrioiden toiminnan on osoitettu vahingoittuneen. Campbell et al. (2011) käytti kompleksista IV / kompleksi II histokemiaa, immunohistokemiaa, laserdisektiomikroskopiaa sekä PCR- ja DNA-sekvensointimenetelmiä osoittamaan silmiinpistävän kompleksien II ja IV aktiivisuuden vähenemisen oksidatiivisen fosforylaatioketjun aikana neuroneissa, jotka saatiin SPMS-tapausten ruumiinavauksista.
3.3. Progressiivinen mitokondrioiden vahingoittuminen voi korreloida relapsien vähentyneen toipumisen kanssa
Transkriptiokofaktorin PGC-1a tasoja, joilla on keskeinen rooli mitokondrioiden toimintaan liittyvien tumatranskriptiotekijöiden aktivaatiossa, voidaan vähentää aivokuoren neuroneissa progressiivisessa MS-taudissa.
Transkriptiokofaktori PGC-1a.n ilmentymisen havaittiin korreloivan hermosolujen tiheyden kanssa. Kun otetaan huomioon havainto, että aivojen atrofian nopeus kasvaa, kun RRMS etenee SPMS-tautimuodoksi, PGC-1a: n lasku voi viitata mitokondrioiden toiminnan samanaikaiseen heikkenemisseen.
Taudin tässä etenemisvaiheessa toipuminen relapseista muuttuu asteittain huonommaksi. Mitokondrioiden toiminnan asteittainen heikkeneminen ja siitä johtuva ATP-saatavuuden heikkeneminen voi aiheuttaa aksonin sietokyvyn heikkenemisen, mikä tekee jokaisesta relapsista toipumisesta yhä vaikeampaa.
PGC-1a-tasojen laskua on havaittu myös muissa neurodegeneratiivisissa taudeissa, kuten Alzheimerin taudissa
Mitokondriot ja neurodegeneraatio
Tutkijapiireissä pidetään todennäköisenä mallia, jossa mitokondrioiden toimintahäiriöt ovat keskeisiä neurodegeneraatiivisten tapahtumien patogeneesissä. Tässä mallissa mitokondrioiden toimintahäiriöt edeltävät synaptista toimintahäiriötä, atrofiaa ja hermosolujen tuhoa.
Multippeliskleroosin eläinmallissa (enkefalomyeliitissä, EAE), mitokondriovaurion on osoitettu edeltävän tulehdusta ja laukaisevan neurodegeneraation. Vaikka mitokondrioiden vaurioihin johtavat tarkat molekyylireitit ovat edelleen tuntemattomia, oksidatiiviset vauriot ovat yksi mahdollinen reitti.
Varhaiset tutkimukset antioksidanttihoidoista MS-eläinmalleissa ovat antaneet lupaavia tuloksia. Superoksididismutaasi 2:n on osoitettu korjaavan aksonihäviön EAE: hen liittyvässä näköhermotulehduksessa.
| Superoksididismutaasi eli SOD on entsyymi, joka katalysoi superoksidi-ionien disproportioitumista vetyperoksidiksi ja hapeksi. Superoksididismutaasi on tärkeä antioksidantti useissa soluissa. |
Synteettisen antioksidantin, Mito-Q:n, on osoitettu olevan neuroprotektiivinen ja hidastavan taudin etenemistä EAE:ssa, vaikka sillä ei ole vaikutusta tulehdustapahtumaan. Tämä vahvistaa edelleen dissosiaatiota kahden erillisen tautiprosessin välillä ja osoittaa, että neurodegeneraation hillitsemistä tulisi harkita mahdollisena terapian kohteena etenevässä multippeliskleroosissa.
Tähän mennessä eräs harvoista etenevän MS-taudin hoitoon käytettävissä olevista vaihtoehdoista, joilla saattaa olla myönteisiä terapeuttisia vaikutuksia, on dimetyylifumaraatti tai DMF.
DMF on ainoa nykyinen lääke, joka immunomoduloivan vaikutuksen lisäksi on toimii voimakkaana antioksidanttina. Sen uskotaan vähentävän oksidatiivista stressiä NRF-2-reitin kautta, ja sillä on siten neuroprotektiivinen vaikutus. Tämä neuroprotektiivinen vaikutus on ollut ilmeinen myös muissa neurodegeneratiivisissa taudeissa.
5. Mitokondriot progressiivisen MS-taudin terapeuttisena kohteena
Mitokondrioiden toimintahäiriöiden rooli neurodegeneraatiossa viittaa siihen, että terapian kohdistaminen mitokondrioiden toimintaan voi olla hyödyllinen terapeuttinen strategia etenevän MS-taudin hoidossa.
Mitokondrioiden toimintaan kohdistuvien lääkkeiden toimivuudesta MS-taudin hoitona on vähän tutkimustietoa, mutta niiden tulokset ovat olleet lupaavia.
Koentsyymi Q10:llä on antioksidanttisia ominaisuuksia ja se on osa elektronin siirtoketjua, joka on vuorovaikutuksessa kompleksin I kanssa.
12 viikon satunnaistettu lumekontrolloitu kaksoissokkoutettu koentsyymi Q10 -lisäravinnetutkimus potilailla, joilla oli relapsoiva remittoiva MS (RRMS), osoitti IL-6:n ja MMP-9:n vähenemistä. Saman ryhmän toisen samanlaisen tutkimuksen tulokset osoittivat Q10-lisäravinteen vähentävän MS-potilaiden masennusta ja väsymystä.
Mito-Q on ubikinonia sisältävä antioksidantti, jonka on osoitettu hidastavan taudin etenemistä ja vähentävän hermosolujen tuhoa multippeliskleroosin hiirimallissa; toisaalta yhdessä tutkimuksessa, jossa käytettiin koentsyymi Q10:n synteettistä analogia, taudin eteneminen ei hidastunut.
Glukoosin hypometabolia
Jotkut tutkimukset ovat viitanneet siihen, että hermosolujen aineenvaihdunnassa voi tapahtua solujen glukoosinoton vähenemiseen vaikuttava bioenerginen muutos ennen neurodegeneraation kliinisten oireiden ilmaantumista.
Tämä glukoosin hypometabolia voi heijastua mitokondrioiden toiminnan heikkenemisenä. Muutoksen on havaittu tapahtuvan kauan ennen neurodegeneraation kliinisten oireiden ilmaantumista, mikä viittaa mahdollisuuteen, että glukoosin hypometabolia voi olla alkuvaihe, joka johtaa aksonin atrofiaan ja hermosolujen menetykseen vähentämällä ATP:n saatavuutta. Bioenerginen muutos näyttää vaikuttavan erityisesti glukoosin metaboliaan. Tällaista muutosta ei havaita ketoosiin perustuvassa aineenvaihdunnassa.
6.1. Glukoosin hypometabolia MS: ssä
Progressiivisen MS-taudin taustalla oleva neurodegeneratiivinen prosessi voi myös johtaa glukoosin hypometaboliaan. Tämä viittaa potentiaaliseen terapeuttiseen etuun energian saannin tehostamisessa vaihtoehtoisella reitillä, kuten ketoosiin perustuvalla metabolialla.
Tutkimus, jossa verrattiin 47 MS-potilasta, joilla oli vaihteleva vireystaso ja 16 tervettä kontrollia, osoitti, että potilailla oli kontrolleihin verrattuna heikentynyt aivojen glukoosimetabolia useilla aivojen eri alueilla, mukaan lukien prefrontaaliset-, premotoriset- ja täydentävät motoriset alueet sekä tyvitumake.
Vireysasteen ja glukoosin metabolisen nopeuden välillä oli käänteinen korrelaatio. Toinen tutkimus, johon osallistui 8 MS-potilasta ja 8 potilaita vastaavaa tervettä vertailuhenkilöä, osoitti MS-potilaiden hermosolujen glukoosinoton heikentyneen 40% terveisiin verrokkiin verrattuna.
Ekstramitokondrioiden metabolia lisääntyy, kun glukoosin mitokondrioiden metabolia on heikentynyt. Pilottitutkimuksessa, jossa verrattiin 85 potilasta, joilla oli relapsoiva remittoiva MS, 54 potilasta, joilla oli sekundaarisesti progressiivinen MS ja 18 tervettä kontrollia, ekstramitokondrioiden glukoosimetabolia osoitti korrelaation taudin etenemisen kanssa, mikä viittaa siihen, että heikentyneellä glukoosin mitokondrioiden metabolialla voi olla merkittävä rooli progressiivisessa MS-taudin etenemisessä.
Vastaavia tuloksia on saatu myös muiden neurodegeneratiivisten tautien, kuten dementian, Alzheimerin taudin ja Parkinsonin taudin tutkimuksissa.
Muita merkittäviä molekyylitodisteita heikentyneestä glukoosimetaboliasta MS-taudissa, nähdään glukoosin (GLUT) ja monokarboksylaattikuljettajien (MCT) muuttuneessa jakautumisessa. MS-tautiin liittyvien kroonisten leesioiden sisällä aksonaalisen GLUT3- ja MCT2-kuljetusmolekyylien määrä on selvästi vähentynyt.
Nämä biokemialliset muutokset hermoston metaboliassa voivat selittää glukoosinoton heikkenemistä demyelinoiduissa aksoneissa. Hermosolut näyttävät muuttuvan eräällä tavalla ”glukoosiresistenteiksi”, koska solujen glukoosinoton tarvitsemien kuljetusmolekyylien määrä romahtaa. Solujen heikentynyt glukoosinotto heijastuu solujen energianpuutteena, hypoglykemiana ja lopulta solujen tuhoutumisena, eli atrofiana.
Jos hermosoluille tarjotaan glukoosin sijaan vaihtoehtoinen polttoaine, hermoston rappeutuminen voi hidastua tai pysähtyä.
Tämä on mielenkiintoinen terapeuttinen mahdollisuus, sillä vielä tämän vuosituhannen alussa oltiin aivan varmoja siitä, että hermosolut tarvitsevat välttämättä glukoosia. Viimeaikaiset tutkimukset ovat osoittaneet, että aivot toimivat jopa tehokkaammin ketoaineilla kuin glukoosilla.
Ketoaineiden vaikutus on osoitettu kliinisesti erilaisilla aivojen kuvantamiseen perustuvilla menetelmillä sekä tutkittavien kognitiivisia kykyjä mittaavilla testeillä. MRI-kuvat ovat osoittaneet, että aivojen aktiivisuus lisääntyy ketoainella. Myös kognitiiviset kyvyt, kuten muisti paranevat ketoaineita saaneilla Parkinsonin ja Alzheimerin tautia sairastavilla potilailla.
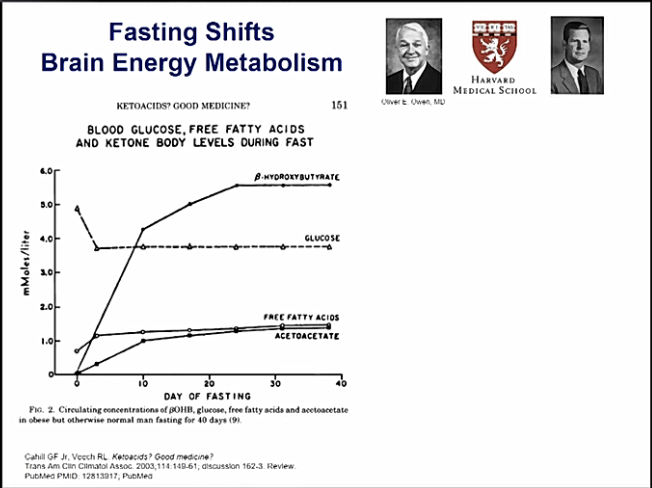
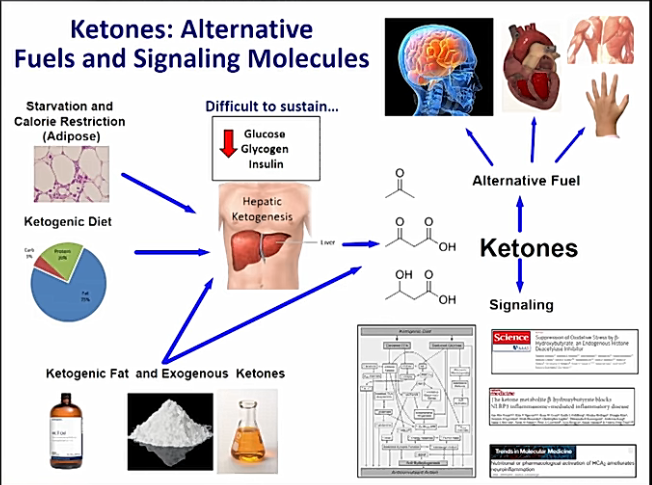
Vuonna 1967 Cahill et al. osoitti, että pitkittyneen paaston aikana keho tarjoaa aivoille vaihtoehtoisen polttoainelähteen ketoaineiden muodossa. Keskushermosto ei pysty käyttämään rasvaa suorana energialähteenä. Pitkittyneen hiilihydraattirajoituksen jälkeen rasva muuttuu ketoaineiksi prosessissa, jota kutsutaan ketogeneesiksi.
Ketogeneesi tapahtuu ensisijaisesti maksassa olevien mitokondrioiden matriisissa. Ketogeneesi johtaa ketoaineiden (beetahydroksibutyraatin, asetoasetaatin ja asetonin) tuotantoon. Ne korvaavat glukoosin aivojen tärkeimpinä polttoaineiden lähteinä.
Hans Krebs erotti normaalin ”fysiologisen” ketoosin, jossa ketonipitoisuus ei ylitä 8 mmol / l, ja diabeettisen ketoasidoosin, eli happomyrkytyksen, joka on diabeteksen komplikaatio, jossa ketoaineineiden määrä voi olla yli 20 mmol / kg L ja voi johtaa kuolemaan.
Ketoaineet voivat helposti läpäistä veri-aivoesteen. Aivojen ketoaineiden hyödyntäminen lisääntyy, kun ketoneiden määrä seerumissa nousee 12 mmol / l:n pitoisuuteen. Eläintutkimusten meta-analyysi on osoittanut, että glukoosin aivojen aineenvaihdunnan nopeus laskee 9% jokaisen plasman ketonien 1 mmol / l kasvun jälkeen.
Ketonit ohittavat glykolyyttisen reitin ja siirtyvät suoraan trikarboksyylihapposykliin (TCA) mitokondrioissa, mikä osaltaan edistää anapleroosia.
Anapleroosi on trikarboksyylihapposyklin välituotteiden muodostumisprosessi. Omenahappoentsyymillä (mtME), fosfenopyruvaattikarboksikinaasilla (PEPCK), propionyyli-CoA-karboksylaasilla, pyruvaattikarboksylaasilla ja proliinidehydrogenaasilla on tärkeä rooli anapleroosissa.
Ketogeeninen ruokavalio progressiivisen MS-taudinn neurodegeneraation estäjänä?
Ketogeenistä ruokavaliota on perinteisesti käytetty resistentin epilepsian hoitoon, mutta on yhä ilmeisempää, että sen edut voivat koskea laajempaa neurologisten sairauksien kirjoa.
Vaikka tutkimus sen käytöstä epilepsian ulkopuolella on vielä alkuvaiheessa, havainnot ovat lupaavia ja niillä on merkittävä potentiaali neurodegeneraation hoidossa, erityisesti mitokondrioiden toiminnan suhteen.
Ketogeenisellä ruokavaliolla on suotuisa vaikutus mitokondrioiden toimintaan. Se vähentää reaktiivisten happiradikaalien määrää ja lisää ATP:n saatavuutta. Ruokavalio voi suojata hermosoluja atrofialta ja vähentää inflammaatiota. Ketogeenisen ruokavalion aikana tuotettuja ketoneja voidaan käyttää vaihtoehtoisena polttoaineen lähteenä heikentyneen glukoosimetabolian yhteydessä.
9. Ketogeenisen ruokavalion vaikutus oksidatiiviseen stressiin
Ketogeenisen ruokavalion on osoitettu vähentävän reaktiivisten happiradikaalien muodostumista vaikuttamalla UCP-irroittajaproteiineihin. Se lisää myös antioksidanttien, mukaan lukien katalaasi ja glutationi, tasoja inhiboivan vaikutuksensa kautta histonideasetylaaseihin ja aktivoimalla Nrf2-reittiä.
Irrooittajaproteiini (UCP) on mitokondrioiden sisäkalvoproteiini, joka on säännelty protonikanava tai kuljettaja. Irrotettava proteiini kykenee siten hajottamaan protonigradientin, joka syntyy NADH-moottorilla pumppaamalla protoneja mitokondrioiden matriisista mitokondrioiden kalvojen väliseen tilaan.

9.1. Ketogeeninen ruokavalio lisää mitokondrioiden UCP-proteiinitasoja
Oksidatiivinen fosforylaatio tuottaa reaktiivisia happiradikaaleja (ROS). Reaktiivisten happiradikaalien ylituotanto korreloi voimakkaasti mitokondriomembraanien potentiaalisten erojen välillä. Proteiinien irrottaminen (UCP) voi vähentää tätä potentiaalieroa sallimalla protonien pääsyn mitokondrioiden matriisiin.
Vaikka tämä irtikytkentä voi vähentää hapettuvan fosforylaation kautta syntyvää ATP:tä, sen kokonaisnettovaikutuksena on parantaa soluhengitystä ja ATP-tasoja vähentämällä reaktiivisten happilajien muodostumista ja suojata solua apoptoottisilta tapahtumilta.
Ketogeeninen ruokavalio näyttää edistävän UCP-aktiivisuutta, erityisesti UCP2:n, UCP4:n ja UCP5:n aktiivisuutta vastaavalla reaktiivisten happilajien vähenemisellä.

9.2. Ketonit estävät histonideasetylaaseja
Betahydroksibutyraatilla on suora, annoksesta riippuva estovaikutus luokan I histonideasetylaaseihin (HDAC), mukaan lukien HDAC1, HDAC3 ja HDAC4.
Asetoasetaatin on myös osoitettu estävän luokan I ja luokan IIa HDAC: ita. Betahydroksibutyraatin HDAC-esto edistää histoni H3-lysiini 9:n ja histoni H3-lysiini 14:n asetylointia ja lisää FOXO3A:n säätelemien geenien transkriptiota.
Näihin kuuluvat geenit, jotka johtavat mitokondrioiden antioksidanttientsyymien, kuten superoksididismutaasin (SOD) ja katalaasin ilmentymiseen.
9.3. Ketogeeninen ruokavalio johtaa Nrf2-reitin aktivoitumiseen
Ketogeeninen ruokavalio nostaa glutationitasoja rottien hipokampuksessa. Tämän uskotaan tapahtuvan Nrf2 (tumatekijä erythroid 2:een liittyvä tekijä) -reitin kautta. Kun ketogeeninen ruokavalio aloitetaan ensimmäisen kerran, oksidatiivinen stressi lisääntyy väliaikaisesti. Tämä voi aktivoida Nrf2:ta, koska viikko oksidatiivisen stressin väliaikaisen nousun jälkeen Nrf2: n ilmentyminen on lisääntynyt.
Kolme viikkoa ruokavalion aloittamisen jälkeen oksidatiivinen stressi laskee alle perustason ja Nrf2 pysyy koholla.
10. Ketogeenisen ruokavalion vaikutus ATP-tasoihin
Ketogeeninen ruokavalio parantaa ATP-tuotantoa. Betahydroksibutyraatin anto aivojen iskemian hiirimallissa säilyttää solujen ATP-tasot. Hiirien ruokinta ketogeenisellä ruokavaliolla kolmen viikon ajan johti lisääntyneeseen ATP-pitoisuuteen ja ATP / ADP-suhteeseen aivoissa.
ATP-tasojen paraneminen voidaan osittain selittää ketogeenisen ruokavalion kyvyllä vähentää oksidatiivista stressiä. Vaikka ruokavalio voi vähentää reaktiivisten happiradikaalien muodostumista lisäämällä UCP-aktiivisuutta, mikä tahansa UCP-aktiivisuuden aiheuttama oksidatiivisen fosforylaation väheneminen on suurempi kuin soluhengityksen tehostuminen ja siihen liittyvä ATP-tuotanto, joka tapahtuu vähentyneen oksidatiivisen stressin seurauksena.
Ketogeeninen ruokavalio näyttää myös säilyttävän ATP-tasot mitokondrioiden soluhengitysketjun toimintahäiriöiden yhteydessä, mahdollisesti täydentämällä TCA-syklin välituotteita.
Betahydroksibutyraatti vaimentaa elektroninsiirtoketjun kompleksin I vaurion aiheuttamaa ATP-tuotannon vähenemistä. Sen uskotaan lisäävän TCA-välisukkinaatin tasoja, joka ohittaa kompleksin I tullessaan TCA-sykliin. Tällä on huomattavia seurauksia MS-taudissa, koska elektronin siirtoketjun sisällä olevan kompleksin I vikoja on havaittu sekä valkoisen aineen vaurioissa että motorisen aivokuoren ”normaaleilla” alueilla.
Ketonit voivat myös säilyttää ATP-tasot, jos elektronin siirtoketjun kompleksi II estetään, mutta tähän liittyy jonkin verran alueellista spesifisyyttä.

11. Ketogeenisen ruokavalion vaikutus mitokondrioiden biogeneesiin
Ketogeeninen ruokavalio lisää mitokondrioiden biogeneesiä rotan hippokampuksessa ja pikkuaivojen vermissä (vermis). Vaikka tarkkaa reittiä tälle ei tunneta, sen uskotaan liittyvän PGC1a-perheen transkriptiokoaktivaattoreihin, jotka edistävät transkriptiotekijöitä, mukaan lukien NRF-1, NRF-2 ja ERRa.
12. Ketogeenisen ruokavalion vaikutus tulehdukseen
MS-taudin rotamallissa ketogeeninen ruokavalio tukahdutti tulehduksellisten sytokiinien ilmentymisen ja lisäsi CA1-hippokampuksen synaptista plastisuutta ja pitkäaikaista potentiointia, mikä johti parantuneeseen oppimiseen, muistiin ja motoriseen kykyyn.
Ketogeenisen ruokavalion tulehdusta ehkäisevä vaikutus voidaan osittain selittää estämällä NLRP3-tulehdusta betahydroksibutyraatilla tavalla, joka on riippumaton nälän aiheuttamista mekanismeista, kuten AMPK, autofagia tai glykolyyttinen esto.
NLRP3-tulehdus on vastuussa prokaspaasi-1:n pilkkomisesta kaspaasi-1: ksi ja sytokiinien IL-1β ja IL-18 aktivaatiosta. Sen esto estää IL-1β: n ja IL-18: n muodostumisen ja niiden alavirran vaikutukset.
13. Ketogeenisen ruokavalion neuroprotektiiviset ominaisuudet
Ketoaineilla on hermosoluja suojaava, eli neuroprotektiivinen rooli neurodegeneraation eläinmalleissa. Neuronien solupinnalla sijaitsevat ATP-herkät kaliumkanavat (K ATP-kanavat) stabiloivat hermosolujen herkkyyttä.
Ketonit edistävät näiden kanavien ”avointa tilaa” ja lisäävät hermosolujen vakautta. K ATP-kanavilla on myös rooli mitokondrioiden toiminnassa ja solukuolemassa. Sisemmällä mitokondriokalvolla sijaitsevien K ATP-kanavien ”avoin tila” estää mitokondrioiden läpäisevyyden siirtymähuokosten (MPTP) muodostumisen, jotka voivat johtaa mitokondrioiden turvotukseen ja solukuolemaan.
Asetoasetaatin ja beetahydroksibutyraatin on osoitettu nostavan kynnystä kalsiumin aiheuttaman MPTP: n muodostumiselle.
14. Ketonien vaikutuksen alueellinen vaihtelu hiiren pikkuaivoissa
Huolimatta näistä näennäisesti positiivisista vaikutuksista mitokondrioiden bioenergeettisiin aineisiin, ketogeenisen ruokavalion vaikutukset hiiren aivojen mitokondrioihin eivät ole homogeenisia ja jotkut tulokset näyttävät ristiriitaisilta.
Tutkimuksessa rotilla, jotka saivat ketogeenistä ruokavaliota 8 viikon ajan, antioksidanttitaso kohosi hippokampuksessa, mutta ei aivokuoressa, ja antioksidanttiaktiivisuuden havaittiin vähenevän pikkuaivossa.
15. Havainnot ihmisillä
Toistaiseksi ihmisillä tehtyjä tutkimuksia ketonien / ketogeenisen ruokavalion vaikutuksista neurodeneratiivisissa häiriöissä on hyvin vähän.
On kuitenkin ainakin yksi satunnaistettu kaksoissokkoutettu lumekontrolloitu tutkimus, jossa tarkasteltiin ketonien vaikutuksia neurodegeneratiiviseen fenotyyppiin 152 lievää tai kohtalaista Alzheimerin tautia sairastavalla. Osallistujilla havaittiin kognitiivisten kykyjen parantumista, kun ketogeenista yhdiste AC-1202:ta käytettiin 90 päivän ajan.
Tämä parannus oli suurempi potilailla, joilla ei ollut APOE4-polymorfismia. Pienemmät tutkimukset muissa neurodegeneratiivisissa olosuhteissa ovat tuottaneet yhtä positiivisia tuloksia.
On todisteita glukoosinkuljettajan toimintahäiriöistä aksoneissa, joihin on muodostunut MS-taudin aiheuttamia kroonisia vaurioita. Tutkimukset ketogeenistä ruokavaliota noudattaneista perinnöllisistä glukoosinkuljettajan toimintahäiriöitä sairastavilla ovat myös antneet positiivisia tuloksia.
16. Päätelmä
Ketogeenisellä ruokavaliolla on potentiaalia hoitaa progressiivisen MS:n neurodegeneratiivista komponenttia seuraavien in vitro ja in vivo -tutkimuksista saatujen havaintojen perusteella:
- Neurodegeneraation uskotaan perustavan progressiivisen MS: n patogeneesin.
- Mitokondrioiden toimintahäiriö voi johtaa ATP: n saatavuuden heikkenemiseen. Tämä voi edistää aksonin atrofiaa, mikä johtaa rappeutumiseen.On todisteita mitokondrioiden toimintahäiriöistä ”normaalilta näyttävässä” harmaassa aineessa ja mitokondrioiden toiminta näyttää korreloivan aksonien eloonjäämisen kanssa.
- In vitro- ja eläintutkimusten mukaan ketogeeninen ruokavalio lisää ATP-tuotantoa, edistää mitokondrioiden biogeneesiä ja ohittaa toimintahäiriöt sisällä mitokondrioiden bioenergeettinen prosessi lisää antioksidanttitasoja ja vähentää oksidatiivisia vaurioita.Koska ATP: n lisääntyminen ja mitokondrioiden toiminnan yleinen paraneminen korreloivat aksonien eloonjäämisen kanssa, ketogeeninen ruokavalio voi tarjota terapeuttista hyötyä MS-taudin neurodegeneratiiviselle komponentille.EAE-eläinmallit eivät edusta tarkasti MS: n taustalla olevaa patogeneesiä, koska neurodegeneraatiolla ei ole merkittävää roolia EAE:ssä.Mitokondrioita kohdentavat aineet, ketonit ja ketogeeninen ruokavalio ovat kuitenkin osoittaneet positiivisia tuloksia useissa hermoston rappeutumismalleissa, ja kun otetaan huomioon progressiivisen MS-tautiin käytettävissä olevan hoidon täydellinen puuttuminen, ketogeeninen ruokavalio on turvallinen vaihtoehto taudin etenemisen hidastamiseen.
Runsaasta rasvan määrästä huolimatta ketogeeninen ruokavalio on turvallinen ja jopa hyödyllinen kardiometabolisten riskitekijöiden suhteen (A. F. Cicero, M. Benelli, M. Brancaleoni, G. Dainelli, D. Merlini, and R. Negri, “Middle and long-term impact of a very low-carbohydrate ketogenic diet on cardiometabolic factors: a multi-center, cross-sectional, clinical study,” ).
Se on ollut jatkuvassa käytössä lähes vuosisadan ajan epilepsian hoidossa, ja se on ollut hyvin siedetty jopa lapsilla. Nykyisiin ketogeenisiin ruokavalioprotokolliin sisältyy useita vaihtoehtoja, mikä kannustaa kokeilemaan itselleen parhaiten sopivaa mallia.
MS-taudin nykyiset hoitovaihtoehdot vaikuttavat immuunijärjestelmän toimintaan ja uusiutumisasteeseen vaikuttaen vain vähän taudin etenemiseen. Niihin liittyy joskus merkittäviä sivuvaikutuksia, kuten lymfopenia ja multifokaalinen leukoenkefalopatia.
Tämän vuoksi joillekin potilaille voi olla edullisempaa noudattaa riskitöntä ruokavaliota, jolla on potentiaalia hidastaa taudin etenemistä vaikuttamatta immuunivasteeseen. Yhteenvetona voidaan todeta, että ketogeeninen ruokavalio ansaitsee lisätutkimuksia progressiivisen MS-taudin potentiaalisena terapiana.
https://citeseerx.ist.psu.edu/viewdoc/download?doi=10.1.1.812.402&rep=rep1&type=pdf

 C-peptidi muodostuu haiman Langerhansin saarekkeiden β-soluissa syntetisoidusta proinsuliinista sen pilkkoutuessa insuliiniksi ja C-peptidiksi. Sitä erittyy vereen insuliinin kanssa ekvimolaarisina määrinä.
C-peptidi muodostuu haiman Langerhansin saarekkeiden β-soluissa syntetisoidusta proinsuliinista sen pilkkoutuessa insuliiniksi ja C-peptidiksi. Sitä erittyy vereen insuliinin kanssa ekvimolaarisina määrinä.