D-vitamiini on saanut valtavasti huomiota sekä erilaisissa medioissa että tutkijapiireissä. Sen vaikutuksista terveyteen on tehty viime vuosina tuhansia tutkimuksia ja uusista terveysvaikutuksista raportoidaan viikoittain. Joillekin on kaikesta huomiosta huolimatta jäänyt epäselväksi, kuinka tärkeä ja monivaikutteinen vitamiini D-vitamiini on.
D-vitamiinin vaikutukset luuston homeostaasiin tunnetaan hyvin, mutta viimeisten 10-15 vuoden aikana tehdyissä tutkimuksissa on on osoitettu, että D-vitamiinilla on myös immuunijärjestelmän toimintaan vaikuttavia ns. immunomodulatorisia ominaisuuksia.
” In addition to its role in calcium and skeletal homeostasis, there is increasing evidence that the hormonal form of vitamin D, 1,25-dihydroxyvitamin D3, appears to serve as a modulator of the immune system.”
”Vitamin D, the sunshine vitamin, has received a lot of attention recently as a result of a meteoric rise in the number of publications showing that vitamin D plays a crucial role in a plethora of physiological functions and associating vitamin D defieciency with many acute and chronic illnessess including disorders of calcium metabolism, autoimmune diseases, some cancers, type 2 diabetes mellitus, cardiovascular disease and infectious diseases. Vitamin D deficiency is now recognized as a global pandemic.”
D-vitamiinin vaikutusmekanismien toiminnan tunteminen on tärkeää D-vitamiinin puutoksen aiheuttamien oireiden ennaltaehkäisyn, tunnistamisen sekä riittävän D-vitamiinin saannin varmistamiseksi .
D-vitamiini
D-vitamiini ei ole ihmelääke, vaan hormonin tavoin vaikuttavan sekosteroidin esiaste ja sellaisena välttämätön elimistön normaalille toiminnalle. D-vitamiini osallistuu kalsiumin homeostaasiin ja säätelee noin 2000 geenin sekä immuunijärjestelmän toimintaa. Ihminen sairastuu, jos D-vitamiinitasot laskevat liian alhaisiksi. Tämän yksinkertaisemmin D-vitamiinia on vaikea määritellä.
Michael F. Holick’in luento oheisella videolla osoittaa, ettei tieteen tekeminen aina ole tylsää. Holick on tutkinut D-vitamiinia ja sen vaikutusmekanismeja lähes viisi vuosikymmentä ja tietää aiheesta todennäköisesti enemmän kuin kukaan muu. Luennolla hän kertoo D-vitamiinin tutkimuksesta, vaikutusmekanismeista sekä sairauksista, joille D-vitamiinin puutos altistaa. Jos, et jaksa kahlata tekstiä läpi, tämä video sisältää kaiken oleellisen ja enemmänkin. Videolla Holick sivuaa myös D-vitamiinisuositusten laskua seurannutta tyypin 1 diabeteksen dramaattista lisääntymistä Suomesta 1950-luvulta alkaen. Puolentoista tunnin luento on lennokas ja jopa hengästyttävä kokemus.
Aitotumallisista selkärankaisiin
D-vitamiini on osallistunut ihmisen elintoimintojen säätelyyn koko ihmisen kehityshistorian ajan ja siksi se on poikkeuksellisen tärkeä osa elimistön hyvinvointia.
Kolesterolisynteesin tuottama D-vitamiini on ollut osa organismien säätely- ja adaptoitumismekanismeja ainakin 500 miljoonaa vuoden ajan. Se kehittyi alkuaan ilmeisesti suojaamaan alkeellisten eliöiden, kuten fytoplanktonin ultraviolettisäteilylle herkkiä makromolekyylejä (proteiineja, ribonukleiinihappoa – RNA ja deoksiribonukleiinihappoa – DNA) auringon UVB-säteilyltä.
D3-vitamiini kehittyi 7-dehydrokolesterolin ja UVB-säteilyn fotokemiallisen reaktion lopputuotteena. Skvaleenista ja lanosterolista alkava kolesterolisynteesi on ilmiönä niin vanha, että se löytyy kaikilta alkeellisilta aitotumallisilta organismeilta, leviltä, kasveilta ja bakteereilta sekä myöhemmin kehittyneiltä selkärankaisilta.
”Cholesterol is important for membrane function regulating endo- and exocytosis and vitamin D may well have acquired such a function early in the evolution of unicellular eukaryocytes. Indeed, the photochemical reaction resulting in vitamin D is considered to be a highly efficient protection of life in early marine organisms against DNA damage induced by UVB.”
Monet kasvit kehittävät D-vitamiinia tai sen provitamiinia, vitamiineja tai vastaavia yhdisteitä ja esimerkiksi tomaatin UVB-säteilylle altistuneissa lehdissä kehittyy sekä D2– että D3-vitamiinia. , D2-vitamiinia, eli ergokalsiferoliakehittyy useimmissa kasveissa ja levissä sekä joissain hiivoissa. Etanoilla on 25-OH-D-vitamiinia, eli kalsidiolia, mutta ei kalsitriolia.
”Solanum glaucophyllum cells are able to synthesize even 1a,25-dihydroxyvitamin D3 (1,25(OH)2D3), as glycoside, and sometimes this concentration is high enough to poison grazing animals.”
Sekä D2-vitamiinia (ergokalsiferolia) että D3-vitamiinia (kolekalsiferolia) esiintyi fotokemiallisen reaktion tuottamina inaktiivisina lopputuotteina miljoonien vuosien ajan ennen selkärankaisten kehittymistä.
Selkärankaisten monimutkainen D-vitamiinin aineenvaihduntaa säätelevä umpieritysjärjestelmä edellyttää solun tumissa sijaitsevien NR-reseptoreiden (nuclear receptor – VDR) ohella D-vitamiinia metaboloivia entsyymeitä (CYP450), D-vitamiinin kuljettamiseen erikoistuneita proteiineja (DBP) sekä FGF23-hormonia. Näiden ohella D-vitamiinin umpieritysjärjestelmään kuuluu monimutkainen solunsisäinen geenien tunnistamiseen ja ”koodaamiseen” liittyvä transkriptio- ja viestintäjärjestelmä.
Vitamin D receptor signaling mechanisms: Integrated actions of a well-defined transcription factor (Carsten Carlberg, 2013)
D-vitamiiniin liittyvät immunomodulatoriset ominaisuudet ovat kehittyneet myöhemmin kuin esimerkiksi luustoa ylläpitävä kalsiumhomeostaasin säätelyjärjestelmä, mutta toisaalta D-vitamiinin aineenvaihduntaan osallistuva umpieritysjärjestelmä löytyy kaikilta selkärankaisilta. Selkärankaisilla on tosin erilaisia menetelmiä D-vitamiinitarpeen tyydyttämiseen: lihansyöjät, kuten kissat, saavat D-vitamiinin ravinnosta ja vampyyrilepakot verestä.
”From amphibians onward, bone is gradually more dynamic with regulated bone resorption, mainly by combined action of PTH and 1α,25-dihydroxyvitamin D3 (1,25(OH)2D3) on the generation and function of multinucleated osteoclasts. Therefore, bone functions as a large internal calcium reservoir, under the control of osteoclasts. Osteocytes also display a remarkable spectrum of activities, including mechanical sensing and regulating mineral homeostasis, but also have an important role in global nutritional and energy homeostasis.” Lue tästä
Vitamin D: calcium and bone homeostasis during evolution (Roger Buillon, Tatsuo Suda)
Skvaleeni
D-vitamiinin synteesissä skvaleenilla on merkittävä rooli. Auringon UVB-säteily syntetisoi D-vitamiinia ihon skvaleenista.
Skvaleeni (C30H50) on luonnollinen hiilivety ja triterpeeni, joka elimistössä muuttuu lanosteroliksi ja edelleen steroideiksi. Se on kaikkien steroidien, kuten nestetasapainoa säätelevän kortikosteroidi aldosteronin, sukupuolisteroidien – estrogeenin ja testosteronin sekä ergosteroleihin kuuluvien kolesterolin ja D3-vitamiinin, eli kolekalsiferolin esiaste. Kuuluisa sveitsiläinen kemian professori tri Paul Carer määritteli skvaleenin kemiallisen rakenteen vuonna 1936.
Skvaleenia kehittyi miljardeja vuosia sitten eläneissä mikrobeissa ja prekambrikaudella eläneiden eliöiden solukalvoissa ja sytoplasmassa. Ensimmäisen kerran skvaleenia eristettiin haikalojen maksaöljystä, mutta nykyään tiedetään, että myös ihmisen, etenkin vastasyntyneiden, elimistössä sitä on pieniä määriä. Hain maksassa esiintyvää skvaleenia on kutsuttu Izun niemimaalla Japanissa ”Samedawa’ksi” (”kaiken parantavaksi”). Japanissa ja Kiinassa hainmaksaöljyllä onkin vuosisatojen ajan lääkitty lähes kaikkia vaivoja ummetuksesta syöpiin.
Pari vuosikymmentä sitten osoitettiin, että skvaleenia esiintyy runsaasti amarantin siemenissä ja oliiviöljyssä. Tutkijat Theresa J. Smith ja Harold L. Newmark ovat esittäneet teorian, jonka mukaan oliiviöljyn (ja Välimeren ruokavalion) terveellisyys perustuu runsaaseen (200-400 mg / päivä) skvaleenin saantiin. On myös osoitettu, että skvaleeni on antioksidantti, jonka saanti laskee rintasyövän riskiä.
Skvaleenin biosynteesi tapahtuu kahdessa vaiheessa. Ensimmäisessä vaiheessa kahdesta farnesyylipyrofosfaattimolekyylistä muodostuu välimuoto preskvaleenipyrofosfaatti ja toisessa vaiheessa preskvaleenipyrofosfaatti hajoaa spontaanisti ja rakenne järjestyy skvaleenimolekyyliksi.
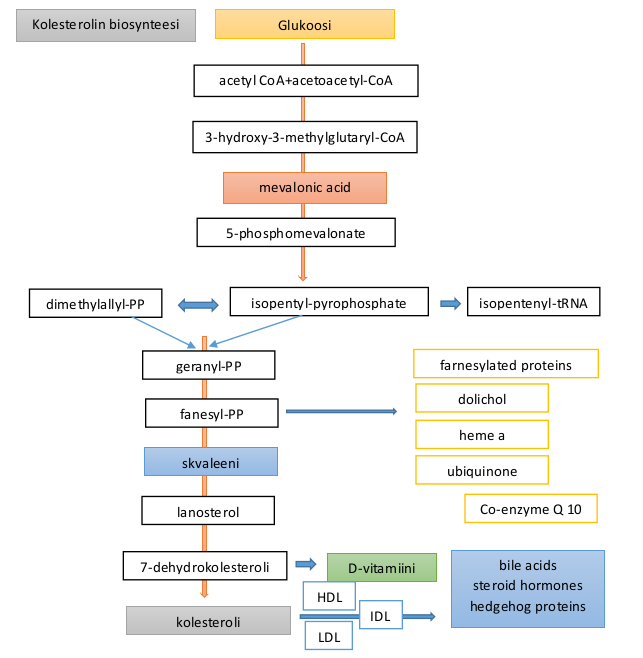
Kolekalsiferoli ja ergokalsiferoli
D3-vitamiini, eli kolekalsiferoli on rasvaliukoinen vitamiini ja sekosteroidi. Se on kalsidiolin ja hormonin tavoin noin 2000 geenin toimintaan vaikuttavan kalsitriolin esiaste.
D2-vitamiini, eli ergokalsiferoli on kasviperäinen D-vitamiini, jota elimistö ei pysty itse valmistamaan. Yleisesti ajatellaan, että kolekalsiferoli imeytyy suolistosta paremmin kuin ergokalsiferoli, mutta tästä ei vallitse yksimielisyyttä.
D-vitamiinin metaboliitit: kalsidioli ja kalsitrioli
D-vitamiinin aineenvaihduntatuotteet syntyvät, kun auringon UVB-säteily syntetisoi ihon (orvaskeden) skvaleenia 7-dehydrokolesteroliksi eli kolekalsiferolin (D3-vitamiinin) esiasteeksi.
D3 (kolekalsiferoli) ja D2 (ergokalsiferoli) -vitamiinin esiasteet hydroksyloidaan 25-hydoksivitamiini D:ksi (25(OH)D), joka on D-vitamiinin epäaktiivinen ”varastomuoto”, kalsidioli. Kalsidiolista hydroksyloidaan edelleen biologisesti aktiivista hormonin tavoin vaikuttavaa 1,25-dihydroksivitamiini D:tä (1,25(OH)2D), eli kalsitriolia. Kalsidiolin puoliintumisaika on noin 20 päivää. Kalsitrioli puoliintuu muutamassa tunnissa.
7-Dehydrocholesterol is the precursor of cholecalciferol. Within the epidermal layer of skin, 7-Dehydrocholesterol undergoes an electrocyclic reaction as a result of UVB radiation, resulting in the opening of the vitamin precursor B-ring through a conrotatory pathway. Following this, the pre-cholecalciferol undergoes a antarafacial sigmatropic rearrangement and therein finally isomerizes to form vitamin D3. – Wikipedia
Kalsitriolin vaikutukset välittyvät soluihin ja geeneihin D-vitamiinireseptorin (VDR) kautta. VDR (Vitamin D(1,25-Dihydroxyvitamin D3) Receptor) on proteiineja ohjaava geeni, johon kalsitrioli sitoutuu ja siirtyy edelleen solun sytoplasmasta tumaan, jossa kalsitrioli-VDR- kompleksi kiinnittyy RXR-proteiiniin ja genomin VDRE-sekvenssiin.
Veren riittävät kalsidiolitasot kasvattavat kalsiumin imeytymistä suolistosta jopa 80 nmol/l tasolle. Mitä korkeammat kalsidiolitasot, sitä alhaisempi riski sairastua suolistosyöpiin. On myös havaittu, että alhaiset kalsidiolitasot vaikuttavat iäkkäämpien ihmisten lihaskuntoon.
Kalsidioli tunnetaan myös nimillä calsifediol, 25-hydroksikolekalsiferoli ja 25-hydroksivitamiini-D (25(OH)D. Helppoa, vai mitä!
A study by Cedric F. Garland and Frank C. Garland of the University of California, San Diego analyzed the blood from 25,000 volunteers from Washington County, Maryland, finding that those with the highest levels of calcifediol had a risk of colon cancer that was one-fifth of typical rates However, randomized controlled trials failed to find a significant correlation between vitamin D supplementation and the risk of colon cancer.
D-vitamiinin puutos lisää kuolleisuutta osoittaa yli 95 000 henkilön tanskalaisseurantatutkimus. http://www.bmj.com/content/349/bmj.g6330
Older people with reduced muscle function often had reduced levels of calcidiol serum concentration. Low levels of calcidiol were not associated with signs of general undernutrition, such as low body mass, or with reduced arm-muscle circumference or triceps skinfold thickness. This finding may suggest a physiological role for calcidiol in muscle function. Reduced muscle strength increased disability in our older subjects, which may be improved by vitamin D supplementation in vitamin D-deficient subjects.
Lähde: http://www.ncbi.nlm.nih.gov/pubmed/9988294
D-vitamiinin riittävä saanti turvaa:
- Kalsiumin imeytymisen ja homeostaasin
- Parathormonin (PTH) liikaerityksen estämisen
- Luun normaalin histologisen rakenteen
Lähde: Ilari Paakkari, Biolääketieteen laitos, Helsingin yliopisto 2012
D-vitamiinin valmistus
D-vitamiini valmistetaan yleensä lampaanvillasta, josta saatavasta lanoliinista (lampaanvillarasvasta) erotetaan 7-dehydrokolesterolia eli D-vitamiinin esiastetta. Se altistetaan ultraviolettisäteilylle, jolloin syntyy kolekalsiferolia.
Tuotantoprosessi on toki monimutkaisempi ja sisältää useita työvaiheita, mutta lyhyesti se menee näin: lampaanvilla puhdistetaan ja siitä erotetaan lanoliini. Seuraavaksi lanoliinista poistetaan rasva ja puhtaasta lanoliinista voidaan erottaa lanoliinialkoholit. Näiden toimenpiteiden jälkeen lanoliinista voidaan edelleen erotella 7-dehydroksikolesterolia, joka puhdistetaan, kuivataan ja altistetaan ultraviolettisäteilylle.
Näin tuotettu kiteinen, lähes puhdas kolekalsiferoli on erittäin vahvaa. 1 gramma lampaanvillasta valmistettua kolekalsiferolia sisältää jopa 750 000 µg eli 30 000 000 IU D-vitamiinia, joka on kemiallisesti identtistä ihmisen oman elimistön syntetisoiman D-vitamiinin kanssa: se toimii elimistössä samalla tavalla. Imeydyttyään ruoansulatuskanavasta verenkiertoon, se hydroksyloidaan ensin maksassa kalsidioliksi ja edelleen munuaisissa aktiiviseksi kalsitrioliksi.
Ergokalsiferolia, eli D2-vitamiinia voidaan valmistaa ainakin eräistä hiivoista.
D-vitamiinin vaikutusmekanismit
D-vitamiinia saadaan vähäisiä määriä ravinnosta, kuten kananmunista, sienistä, rasvaisista kaloista ja maitovalmisteista, mutta tärkein lähde on auringon UVB-säteily, joka syntetisoi ihon orvaskedessä olevasta skvaleenista 7-dehydroksikolesterolia, joka on D3-vitamiinin ja kolesterolin esiaste.
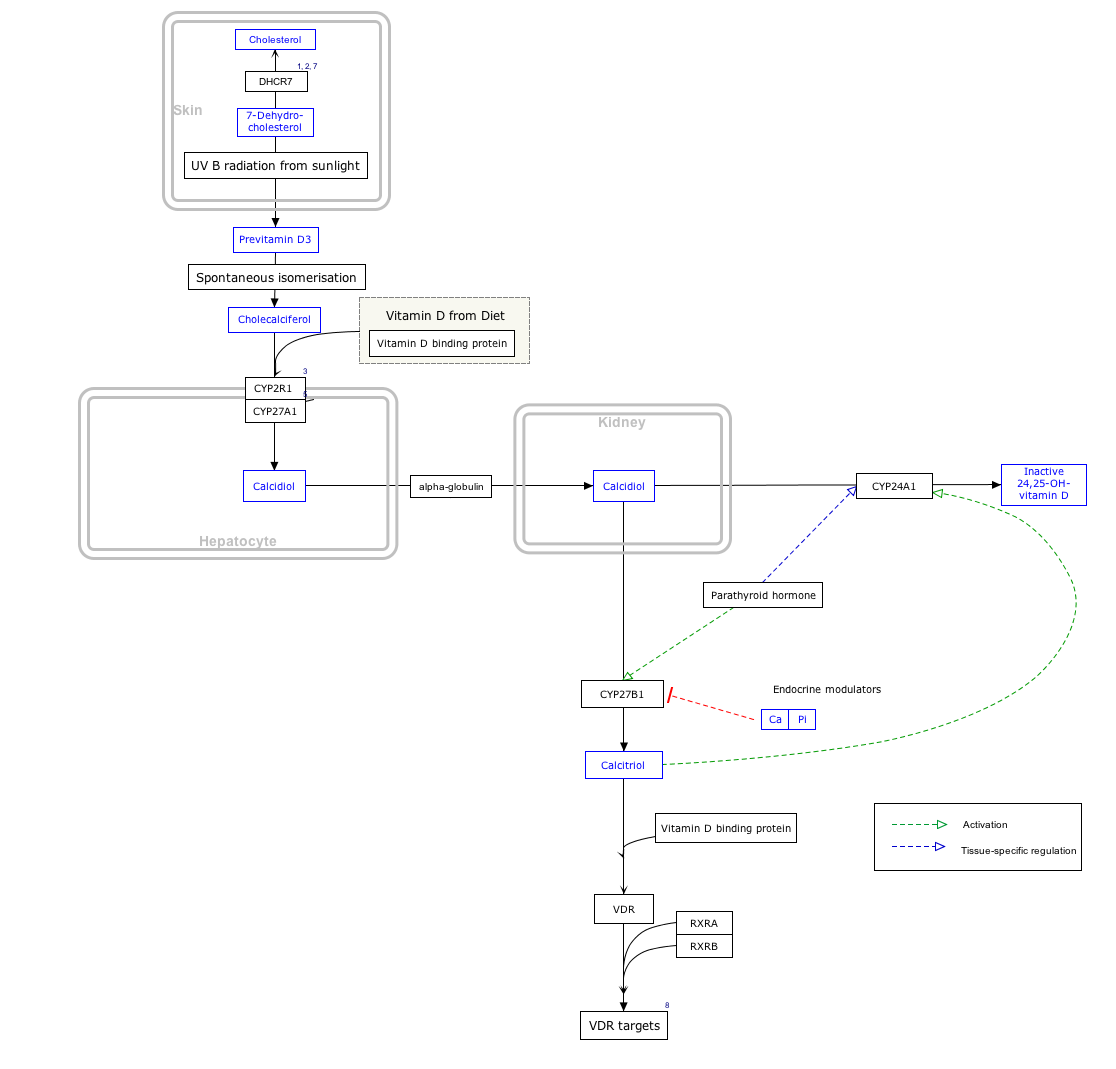
Iholla syntyvä ja suolistosta imeytynyt (syöty) D-vitamiini muuttuvat elimistössä biologisesti aktiiviseen 1,25(OH)2D-vitamiinimuotoon kahden reaktion: hydroksylaation, kautta. Ensimmäinen tapahtuu maksassa ja sen katalyytteinä toimii useita D-25-hydroksylaasientsyymeitä (tärkeimpänä CYP2R1). toinen hydroksylaatio tapahtuu munuaisissa ja sen katalyyttinä vaikuttaa 1α-hydroksylaasi-entsyymi (CYP27B1). Maksassa D-vitamiini muutetaan ensin inaktiiviseksi kalsidioliksi (25-OH-D) ja munuaisissa D-vitamiinin aktiiviseksi metaboliitiksi eli kalsitrioliksi (1,25-OH-2D). Kaavio:

VDR ja kalsitriolin vaikutusmekanismit
Kalsitriolin vaikutukset välittyvät lähes kaikkiin soluihin D-vitamiinireseptoreiden (VDR) kautta.
”This gene encodes the nuclear hormone receptor for vitamin D3. This receptor also functions as a receptor for the secondary bile acid lithocholic acid. The receptor belongs to the family of trans-acting transcriptional regulatory factors and shows sequence similarity to the steroid and thyroid hormone receptors. Downstream targets of this nuclear hormone receptor are principally involved in mineral metabolism though the receptor regulates a variety of other metabolic pathways, such as those involved in the immune response and cancer. Mutations in this gene are associated with type II vitamin D-resistant rickets. A single nucleotide polymorphism in the initiation codon results in an alternate translation start site three codons downstream. Alternative splicing results in multiple transcript variants encoding different proteins. [provided by RefSeq, Feb 2011]”
D-vitamiinireseptoreita löytyy mm. makrofageista, monosyyteistä, dendriittisoluista sekä T-lymfosyyteistä ja keskushermoston soluista, kuten neuroneista, oligodendrosyyteistä, astrosyyteistä ja gliasoluista.
DBP (Vitamin D Binding Protein) on maksan tuottama globuliini (kuljetusproteiini), joka kuljettaa veressä D-vitamiinin metaboliitteja, kuten kalsitriolia kohdesoluihin.
” Globuliinit ovat tärkeitä muun muassa elimistön immuunireaktioissa ja hormonien sekä hivenaineiden kuljettajina.”
Kalsitrioli irrottautuu DBP-proteiinista saavuttaessaan kohdesolun, jossa se sitoutuu sytoplasmassa, eli solulimassa sijaitsevaan VDR-reseptoriin. Syntynyt kompleksi siirtyy edelleen solun tumaan ja kiinnittyy RXR-reseptoriin (Retinoid-X-receptor). Kalsitrioli-VDR-RXR sitoutuu lopulta DNA:ssa VDRE-sekvenssiin (Vitamin D Responsive Elements), jossa se vaimentaa (hiljentää) tai aktivoi sekvenssin geenejä.
D-vitamiini osallistuu kalsiumin ja fosfaatin säätelyjärjestelmään, suojaa verisuonia ja vaikuttaa mm.solujen kasvuun ja erikoistumiseen, hermoston ja immuunijärjestelmän sekä lihasten toimintaan. Kalsitrioli saattaa vaikuttaa myös keskushermostossa neuronien toimintaan ja myelinin tuotantoon, joskaan tätä ei ole aukottomasti todennettu.
VDR: 1,25 DIHYDROXYVITAMIN d3 RECEPTOR VITAMIN D HORMONE RECEPTOR
Besides its role in calcium physiology and bone health, vitamin D also has numerous potential extra-bone actions: protective for the cardiovascular system, antiproliferative (in certain cancers), anti-infectious (innate immunity) and anti-inflammatory and immunomodulatory (adaptive immunity), an effect which could be involved in autoimmune diseases such as type 1 diabetes, Crohn’s disease, rheumatoid arthritis and MS [Holick, 2004, 2007; Vieth, 2007; Vieth et al.. 2007; Borradale and Kimlin, 2009; Hewison, 2012].
We have determined the level of the 1,25-dihydroxyvitamin D3 receptor (VDR) in resting and activated lymphocytes by immuno- and ligand-binding assays. As expected from previous work, the total T lymphocyte population contains VDR whose levels are increased when activated and treated with 1,25-dihydroxyvitamin D3. Surprisingly, the highest concentrations of VDR are found in CD8 lymphocytes, although significant amounts are also present in CD4 lymphocytes. Furthermore, B lymphocytes do not contain detectable amounts of VDR. Cells of the monocyte/macrophage lineage possess small amounts of VDR that are not affected by activation but are increased by treatment with 1,25-dihydroxyvitamin D3. These results suggest that CD8 lymphocytes may be a major site of 1,25-dihydroxyvitamin D3 action, while B lymphocytes are likely not directly regulated by 1,25-dihydroxyvitamin D3. – Expression of 1,25-Dihydroxyvitamin D3 Receptor in the Immune System, Christian M Veldman, Margerita T. Cantoma, Hector F. DeLuca
 Kuvan lähde: https://en.wikipedia.org/wiki/Parathyroid_hormone
Kuvan lähde: https://en.wikipedia.org/wiki/Parathyroid_hormone
The VDR is widely distributed in tissues, and is not restricted to those tissues considered the classic targets of vitamin D. The VDR upon binding to 1,25(OH)2D heterodimerizes with other nuclear hormone receptors, in particular the family of retinoid X receptors. This complex then binds to special DNA sequences called vitamin D response elements (VDRE) in the promoters of genes which it regulates. A variety of additional proteins called coactivators complex with the activated VDR/RXR heterodimers either to form a bridge from the VDR/RXR complex binding to the VDRE to the proteins responsible for transcription such as RNA polymerase II binding to the transcription start site or to help unravel the chromatin at the site of the gene via recruitment of histone acetyl transferases (HAT), allowing transcription to proceed. – Wikipedia
Kalsitriolin säätelyjärjestelmä
Veren matala kalsiumpitoisuus sekä paratyroidi hormoni (PTH) stimuloivat munuaisissa tapahtuvaa hydroksylaatiota lisäten veren kalsitriolipitoisuutta. Korkea kalsitriolipitoisuus ja seerumin FGF23 (phosphaturc hormone fibroblast growth factor 23) toimivat käänteisesti hilliten hydroksylaatiota. Näin kalsitriolin pitoisuus veressä säilyy hyvänä (45-165 pmol/l).
”The kidney is the principal target for FGF23, and the major function of this hormone is to regulate phosphate reabsorption and production of 1,25(OH)2D”.
D-vitamiini-24-hydroksylaasi-entsyymi, jota säätelee CYP24A1-geeni, voi myös passivoida D-vitamiinin aineenvaihduntatuotteita. FGF23 säätelee sekä D-vitamiini-24-hydroksylaasi-entsyymiä että seerumin kalsitriolipitoisuutta. CYP24A1-geenin vaimentavan geenimutaation on osoitettu aiheuttavan vastasyntyneillä vakavaa hyperkalsemiaa.
D-vitamiinin saanti, varastoiminen ja kulutus
Vain 15-30 minuutin altistuminen auringosta saatavalle säteilylle kesällä syntetisoi paljaalla iholla n. 250µg D-vitamiinia. Muutaman aurinkoisen kesäpäivän ”UVB-säteilyhoito” viikossa riittää ylläpitämään terveyden kannalta riittäviä kalsidiolitasoja myös syystalvea varten. D-vitamiinin synteesi käynnistyy kuitenkin vain keskikesän kuukausina ja kello 11-15 välisenä aikana. Muina aikoina otsonikerros imee noin 90 % UVB-säteilystä. Myös aurinkovoiteet estävät tehokkaasti D-vitamiinisynteesin. Aurinkoon ei kuitenkaan kannata mennä polttamaan itseään, koska ihosyöpä on kavala sairaus. 15-30 minuuttia päivässä paljaille käsivarsille ja jaloille riittää.
Kesäkuukausina D-vitamiini varastoituu kalsidiolina mm. rasvasoluihin, joista sitä vapautuu elimistön käyttöön pimeinä talvikuukausina jolloin iho ei pysty syntetisoimaan D-vitamiinia auringon UVB-säteilystä.
D-vitamiinin vuorokausikulutus on n. 40 µg ja pimeänä aikana varastot supistuvat nopeasti. Myös tupakointi kuluttaa D-vitamiinia verestä ja kudoksista. D-vitamiinia voi täysin turvallisesti syödä pimeänä vuodenaikana (elokuun ja toukokuun välillä) 100-250 µg / vrk. Näin elimistön D-vitamiinitasot pysyvät riittävän korkeina. Päiväntasaajan lähellä luonnonvaraisesti elävillä kansoilla elimistön veren kalsidiolipitoisuudet ovat ympäri vuoden 100-200 nmol/l, kun suomalaisten kalsidiolipitoisuudet ovat keskimäärin 50 nmol/l. Tämä korreloi tilastollisesti mm. autoimmuunitautien esiintymisen kanssa.
Ikääntyneillä osteoporoosiin liittyvät luunmurtumat estyvät merkittävästi vasta kun kalsidiolin määrä veressä ylittää 75 nmol/l. Yleisesti hyväksytään se, että alle 50 nmol/l kalsidiolitasot merkitsevät D-vitamiinin puutosta, joka lisää lasten riisitaudin, aikuisten osteomalasian ja ikääntyneiden osteoporoosin riskiä. Luuston terveyden kannalta suositeltavana tasona voidaan pitää D-25-pitoisuutta, joka on yli 80 nmol/ l.
D-vitamiinin pitoisuuteen plasmassa vaikuttaa:
- Painoindeksi (BMI)
- UVB:n saanti (pigmentti, pukeutuminen ja leveyspiiri)
- Kalsidiolipitoisuden taso hoidon alussa
- Ruokavalio
- Ikä (ikääntyneillä D-vitamiinin luonnollinen synteesi iholla hidastuu tai loppuu)
- Suolistosairaudet ja -imeytymishäiriöt
- Perinnölliset tekijät
Huom!
D-vitamiinin puute on sitä yleisempää, mitä kauempana päiväntasaajasta asutaan. Pohjois-Euroopassa S-D-25 vähenee kesän jälkeen keskimäärin 1 nmol/l/viikko, eli talven mittaan 25–35 nmol/l. Pitoisuudet ovat pienimmillään maalis-toukokuussa. Kesän auringonvalo suurentaa S-D-25:ttä sitä nopeammin ja enemmän, mitä pienemmästä lähtöarvosta lähdetään nousemaan (Wulf 2012).
S-D-25 pitoisuus on korkeimmillaan loppukesällä auringonvalon vaikutuksesta ja matalimmillaan keskitalvella. Kesällä runsas UVB-säteilyn saanti voi nostaa D-25 pitoisuudet tasolle 100-200 nmol/l. Korkeat tasot säilyvät kuitenkin vain 1-2 kuukautta. Auringosta ei voi saada D-vitamiinimyrkytystä, koska elimistössä on rajallisesti D-vitamiinisynteesin tarvitsemaan skvaleenia. Voisiko ihon palaminen liittyä siihen, että orvaskeden skvaleeni on syntetisoitu D-vitamiiniksi ja silloin UVB-muuttuu haitalliseksi – en tiedä. Ajatuksena se, että skvaleeni suojaisi ihoa palamiselta on kuitenkin kiinnostava.
Etelänavan retkikunnalla tehdyssä tutkimuksessa havaittiin, että ihminen kuluttaa päivässä n. 40 µg D-vitamiinia, eli tätä vähäisemmällä päiväsaannilla kalsidiolipitoisuus laski auringonvalon puuttuessa. On arvioitu, että päivittäinen 15-20 µg D-vitamiinilisä kohottaa veren kalsidiolin minimitasolle (50nmol/l) ja annos 40-50 µg kohottaa veren kalsidiolin vastaavasti tasolle 75 nmol/l, jota alhaisempia tasoja mm. Kanadassa, Espanjassa, Virossa ja USA:ssa pidetään riittämättöminä.
Yksiköt, pitoisuudet ja tavoitteet
D-vitamiinimääristä käytetään yksikköinä joko mikrogrammaa (µg) tai kansainvälistä yksikköä (IU, International Unit; joskus lyhenteenä käytetään kirjaimia KY). 40 IU on 1 µg. D-vitamiinin mittayksiköiden kanssa on syytä olla tarkkana, koska ne vaihtuvat usein lennossa nanogrammoista nano- tai pikomooleihin ja mikrogrammoista kansainvälisiin yksiköihin. Sekavaa. Tiedän.
1 gramma = 1000 milligrammaa (mg)
1 milligramma = 1000 mikrogrammaa (µg)
eli gramma on 1 000 000 µg.
Kansainväliset yksiköt (IU tai KY, kuinka haluatte):
400 IU = 10 µg
1000 IU = 25 µg
1200 IU = 30 µg
2000 IU = 50 µg
2400 IU = 60 µg
4000 IU = 100 µg
5000 IU = 125 µg
10000 IU = 250 µg
Veren kalsidiolipitoisuuksissa mittayksikkö on nanomoolia litrassa, eli mol/l. Kalsitriolin pitoisuudet ilmaistaan pikomooleina / litrassa, eli pmol/l. Kansainvälisissä julkaisuissa kalsidiolin pitoisuus voidaan ilmaista myös nanogrammoina / millilitra, jolloin kerroin on 2,5. Eli 10 ng/ml = 25 nmol/l.
Tavoitearvot, annostus ja yliannostus
D-vitamiinin määrää elimistössä arvioidaan määrittämällä verenkierrosta seerumin 25-hydroksi-D-vitamiini (S-D-25) pitoisuus, joka kuvaa hyvin elimistön D-vitamiinivarastoja ja D-vitamiinin saantia. Mittauksessa verestä tarkistetaan kemiluminesenssi-menetelmällä D2- ja D3-vitamiinien 25-hydroksyloituneet metaboliitit.
Huom!
1,25(OH)2-D- vitamiini (S -D-1,25, eli kalsitrioli) määritystä ei käytetä elimistön D-vitamiinivarastojen arviointiin. Tutkimus kuvaa biologisesti aktiivia hormonia ja sitä käytetään vain erikoistapauksissa, joissa selvitetään 1-hydroksylaatioon vaikuttavia sairauksia (munuaistauteja sekä perinnöllisiä D-vitamiiniaineenvaihdunnan tauteja).
Lähde: https://vita.fi/laboratoriokasikirja/tutkimus/69
D-vitamiinin (S-D-25) viitearvot Suomessa:
alle 25 nmol/l Vakava puutos
alle 50 nmol/l Puutos
50 – 75 nmol/l Yleensä riittäväksi katsottu pitoisuus
75 – 120 nmol/l Tavoitepitoisuus osteoporoosipotilailla
yli 375 nmol/l Toksinen pitoisuus / myrkytystila
Viitearvot Kanadassa, Virossa, Espanjassa ja Ranskassa:
25 – 74 nmol/l Riittämätön pitoisuus / D-vitamiinin puutos
75 -250 nmol/l Normaali pitoisuus
Viitearvot USA:ssa
75 – 150 nmol/l USA:n endokrinologiyhdistyksen suositus
Muita viitearvoja
<20 nmol/l Vaikea puute
20-50 nmol/l Puute1
50-75 nmol/l Vaje (insufficiency)2,3
75-100 nmol/l Riittävä saanti (sufficiency) luuston kannalta
100-150 nmol/l Luustoon liittymättömiä terveyshyötyjä4
1 Institute of Medicine (IOM) 2011
2 International Osteoporosis Foundation (IOF) 2010
3 American Endocrine Society & Canadian Society of Endocrinology 2011
4 Ottawa Vitamin D Disease Prevention Symposium, 1.11.2012
1,25(OH)2-D- vitamiini (S -D-1,25, kalsitrioli), viitearvot:
45 -165 pmol/l*
*Mitataan poikkeustapauksissa(esim. eräiden munuaistautien ja perinnöllisten D-vitamiinin aineenvaihduntahäiriöiden yhteydessä.
D-vitamiinin vaikutuksia tehostavat koentsyymit.
Koentsyymi eli orgaaninen kofaktori on pieni orgaaninen yhdiste, joka auttaa muodostamaan toimivan entsyymin sitoutumalla entsyymin proteiiniosaan (apoentsyymi). Tällöin muodostuu täydellinen entsyyminä aktiivisesti toimiva holoentsyymi.
Koentsyymi ei ole proteiini, vaan usein vitamiini, vitamiinijohdos tai hivenaine. Koentsyymit osallistuvat entsyymien reaktioihin kulumatta itse reaktioissa. Koentsyymi on välttämätön joidenkin entsyymien toiminnalle. – Wikipedia
- Yksi kolmestasadasta ihmisestä saa D-vitamiinista allergisia oireita. Ongelma johtuu usein magnesiumin puutoksesta.
- Magnesium tehostaa D-vitamiinin vaikutuksia n. 30 %.
- Omega-3 tehostaa kalsidiolin ja kalsitriolin tuotantoa ihmisillä, joilla on munuais- tai maksaongelmia.
- K2 ja D-vitamiini siivoavat verisuonia kuolleista soluista ja kuljettavat kalsiumia luustoon, mikä ehkäisee valtimoiden kalkkeutumista ja ateroskleroosia.
- K2-vitamiinia tulisi syödä D-vitamiinin kanssa n. 100 µg
Onko Suomessa aihetta tarkastaa kalsidiolin viitearvoja?
Suomessa D-vitamiinin saannin turvallisena ylärajana pidetään 100 µg päivässä ympäri vuoden. Tästä johtuen yleisiä saantisuosituksia (10 µg / päivä) on vaikea perustella mitenkään järkevästi. Suositukset ovat pelottavan alhaiset kansanterveyttä ja kansantaloutta ajatellen. Vähintään 25-50 µg päivittäiset suositukset esikoululaisille ja sitä vanemmille parantaisivat ihmisten vastustuskykyä ja toisivat huomattavia säästöjä terveysmenoihin kautta linjan. D-vitamiinin puutoksesta on tullut globaali pandemia, joka altistaa useille vakaville sairauksille.
”Vitamin D may represent the single most cost effective medical intervention we have today.”- [Ottawa Vitamin D Disease Prevention Symposium, 1.112012]
Japanilaisessa koululaisilla tehdyssä tutkimuksessa osoitettiin, että vain 20 µg:n päivittäinen D-vitamiinilisä puolitti riskin sairastua A-influenssaan. Voidaankin perustellusti kysyä, vähenisikö kausittaisiin A-influenssaan sairastuneiden määrä, jos Suomessa D-vitamiinin saantisuosituksia korotettaisiin.
Institute of Medicine (IOM) ja Euroopan elintarviketurvallisuusvirasto (EFSA) korottivat D-vitamiinin turvallisen päiväannoksen 100 µg/vrk tasolle 2011-2012. 100 µg päivittäinen D-vitamiinilisä siis tiedetään turvalliseksi myös Suomessa, mutta silti suomalaisten viranomaisten suositukset ovat vain kymmenesosa turvalliseksi osoitetusta päiväannoksesta.
Neo- ja perinatologit suosittelevat odottaville äideille 100 µg / vrk:
On tutkimusnäyttöä siitä, että sekä äidin alkuraskauden, että varhaislapsuuden aikaiset alhaiset D-vitamiinitasot kohottavat lapsen riskiä sairastua MS-tautiin. Odottavan äidin alkuraskauden aikaiset alhaiset 25(OH)D-tasot lähes kaksinkertaistavat lapsen riskin sairastua MS-tautiin. Lue tästä.
”Supplementation of lactating mothers with high doses of vitamin D (100 µg/d) allows the achievement of optimal 25(OH)D concentrations (>80 nmol/l) in the maternal and infant serum without any risk of hypervitaminosis Di n the mother”- [Marshall, I., Mehta, R., & Petrova, A. 2012 – Vitamin D in the maternal-fetal-neonatal interface: Clinical implications and requirements for supplementation. The Journal of Maternal-Fetal & Neonatal Medicine]
Odottavilla naisilla D-vitamiinitasojen tulisi olla vähintään 100 nmol/l, mikä edellyttää 100 µg D-vitamiinia vuorokaudessa (sanoo Protect Our Children Now -kampanjaa johtava neonatologi (vastasyntyneiden erikoislääkäri) Carol Wagner. Hänen työryhmänsä antoi imettäville äideille 160 µg/vrk, mikä osoittautui tehokkaaksi ja turvalliseksi. Suomessa suositus on vain 10 µg/vrk. WTF!
Imetyksen aikana nautittu 6400 IU eli 160 mikrogrammaa (µg) päivässä on turvallista ja se nostaa äidinmaidon D-vitamiinin pitoisuuden sekä äidille että vauvalle riittäväksi (Hollis ym. 2015).
Entä jos kalsidiolipitoisuudet kasvaisivat tasolle 100-150 nmol/l
Ottawa Vitamin D Disease Prevention Symposium keräsi 2012 johtavia asiantuntijoita kouluttamaan lääkäreitä ja terveydenhoitohenkilökuntaa sekä pohtimaan, minkälaisia vaikutuksia korkeammilla kalsidiolipitoisuuksilla olisi terveyden ja kansantalouden kannalta. Symposiumiin osallistuivat Badeg A Quraishi, MD, Michael F Holick, PhD, MD, Robert P Heaney, MD, Reinhold Vieth, PhD, Gregory APlotnikoff, MD, Cedric F Garland, DR, PH.
Arvioidut vaikutukset olisivat huomattavia:
- 100-150 nmol/l kalsidiolipitoisuus ehkäisisi Kanadassa 18 000 rintasyöpää (75 % tapauksista.
- 15 000 paksusuolen syöpää (67 % tapauksista) voitaisiin ehkäistä.
- MS-tautiin sairastuvien määrä puolittuisi 100-150 nmol/l kalsidiolipitoisuuksilla
- Muina terveyshyötyinä olisi estovaikutus seuraaviin: astma, infektiot, karies, tyypin 1 diabetes, sydän- ja verenkiertotaudit, hypertonia, eturauhassyöpä, osteomalasia ja osteoporoosi.
Lähde: Ilari Paakkari, Biolääketieteen laitos, Helsingin yliopisto, 2012
Omat kokemukset
Sairastan MS-tautia ja olen lääkinnyt itseäni suuriannoksisella D-vitamiinilla jo vuosia elo- ja toukokuun välisenä aikana. Pimeänä vuodenaikana olen syönyt 250-1000 µg / vrk ja kesäisin annostus on ollut pienempi, eli: 0-125 µg / vrk. Tämä voi vaikuttaa mielenvikaiselta, mutta korkeita määriä tukevia tutkimuksia MS-tautiin liittyen on useita. En tiedä, onko D-vitamiini hidastanut taudin etenemistä, koska eteneminen on yksilöllistä ja mitään vertailukohtaa ei ole. Sivuvaikutuksia runsaasta D-vitamiinista ei kuitenkaan ole seurannut. En tosin sellaisiin uskonutkaan.
Huom!
250 nmol/l on osoitettu turvalliseksi ylärajaksi (Mayo-klinikan julkaisema suurtutkimus, 2015).
Suomessa terveyssisaret antoivat vuosina 1946 ja 1948 lapsille D-vitamiinia pistoksina (kerta-annoksina) 7500 mikrogrammaa (µg), eikä mitään myrkytyksiä ilmennyt.
Iranilaisen lastenklinikan lääkkärit antoivat diabeetikkolapsille saman annoksen, 7500 µg, jolloin lasten HbA1c-lukemat (ns. pitkäsokeri) paranivat. Sivuvaikutuksia ei ilmennyt (Mohammadian ym. 2015).
Philadelphian lastensairaalan vuoden mittaisen tutkimuksen mukaan 175 µg (7000 IU) päivässä on täysin turvallista lapsille ja nuorille aikuisille (Shall ym.2015)
Iranilaisessa tutkimuksessa MS-potilaat saivat 12 vikkoa D-vitamiinia 250 µg/päivä. D-vitamiini lisäsi tulehdusta ehkäisevän interleukiini 17:n(IL-17 pitoisuutta merkittävästi, mikä ehkäisee taudin etenemistä. Sivuvaikutuksia ei todettu (Toghianifar ym. 2015).
Johns Hopkinsin yliopistossa Yhdysvalloissa neurologian professori Peter A. Calabresin johdolla tehtiin kliininen tutkimus, jossa MS-potilaille annettiin D-vitamiinia joko 260 tai 20 µg/vrk. Suurempi annos oli hyödyksi, pienempi tehoton.
Italialaisten neurologien tutkimus osoitti, ettei 5000 IU eli 125 µg/vrk riitä nostamaan riittävästi MS-potilaiden liian matalia D-vitamiinipitoisuuksia (Riccio ym. 2016).
Poikkeustapauksissa on suuria D-vitamiinin kerta-annoksia (500 000 KY eli 12 500 µg) annettu kerran vuodessa ilman haittavaikutuksia. Vaikka suurista kerta-annoksista ei ole ollut välitöntä haittaa, tutkimukset viittaavat siihen, että tällä antotavalla ei saavuteta osteoporoottisten murtumien estymistä.
Lähde: http://www.terveyskirjasto.fi/terveyskirjasto/tk.koti?p_artikkeli=dlk01044
Myrkytys
D-vitamiinimyrkytyksessä yleisimpiä myrkytysoireita ovat ruokahaluttomuus, laihtuminen, yleinen heikkous, sekavuus, oksentelu ja nestevajaus. Toksisuusrajana pidetään D-25-pitoisuutta 375 nmol/l.
Lähde: https://vita.fi/laboratoriokasikirja/tutkimus/69
Bostonissa arviolta 33 000 kuluttajaa altistui viiden ja puolen vuoden ajan maidolle, jossa oli D-vitamiinia litraa kohden yli satakertainen määrä normaalisaantiin verrattuna. Sadat ihmiset sairastuivat. Yleisimpiä myrkytysoireita olivat ruokahaluttomuus, laihtuminen, yleinen heikkous, sekavuus, oksentelu ja nestevajaus. Laboratoriotutkimuksissa veren kalsiumarvot ylittivät normaalin ja veren D-vitamiinin (kalsidiolin) pitoisuudet olivat hyvin suuret (keskimäärin 560 nmol/l).
Lähde: http://www.terveyskirjasto.fi/terveyskirjasto/tk.koti?p_artikkeli=dlk01044
Oireet, jotka saattavat viitata D-vitamiinin puutostilaan (hypovitaminosis D):
Eräät aivan arkipäiväiset oireet voivat viitata D-vitamiinin puutokseen. Näitä ovat mm: lihasheikkous, lievä päänsärky, lihasten kipeytyminen, krampit ja suonenveto, heikentynyt immuunijärjestelmä (jatkuva sairastelu) ja jopa lievät muisti- ja keskittymisvaikeudet. Vastaavia oireita voi aiheuttaa monet tekijät – ei pelkästään D-vitamiinin puutos. Se on kuitenkin yksi varteenotettava selitys monille arkisille oireille.
Yli kolmannes suomalaisista kärsii jatkuvasta D-vitamiinin puutoksesta ja edellä mainitut oireet ovat monille tuttuja. Ne ovat D-vitamiinin puutoksen tavallisimpia oireita. Jos D-vitamiinitasot ovat jatkuvasti hyvin alhaiset, seurauksena voi olla vakavia sairauksia, kuten: sydän- ja verisuonitaudit, autoimmuunisairaudet, eräät syövät, osteomalasia, osteoporoosi jne.
Michael F. Holick puhuu luennollaan teoriasta, jonka mukaan influenssojen esiintyminen etenkin kevättalvella (kun elimistön D-vitamiinitasot ovat alhaisimmillaan), johtuu siitä, että immuunijärjestelmä toimii alhaisilla D-vitamiinitasoilla huonommin kuin riittävillä D-vitamiinitasoilla. Tilastot ja tutkimukset tukevat hypoteesia.
Huom!
100 µg D-vitamiinia laskee infektioherkkien ihmisten sairastumisen ja antibioottien tarpeen puoleen, selviää ruotsalaisten infektiolääkäreiden tutkimuksesta (Bergman ym. 2015).
Joka viides masennus voitaisiin ehkäistä D-vitamiinilla, osoittaa puolestaan THL:n tutkimus.
Tuore kuopiolaistutkimus kertoo, että 6–8-vuotiaiden suomalaislasten D-vitamiinin saanti on järkyttävän vähäistä (Soininen ym. 2016). Se on keskimäärin vain 5,9 (SD 2,1) mikrogrammaa (µg) päivässä. Vain 40,8 % lapsista otti D-vitamiinilisää (koska ravitsemustieteilijät toitottavat mediassa, ettei D:tä tarvitse ottaa ”purkista” ja monet vanhemmat uskovat heitä). 82,4 % lapsista ei saanut D:tä edes 10 µg päivässä, vaikka joivat D-vitaminoitua maitoa. Maito antoi lähes puolet lasten saamasta D-vitamiinista. Joka viidennen lapsen S-D-25 oli alle 50 nmol/l eli heillä oli huutava D-vitamiinin puute (kansainvälinen viitearvo on 75–150 nmol/l, Virossa, Espanjassa, Ranskassa 75–250 nmol/l). Vain 31 % lapsista pääsi yli 75 nmolin/l. Puutetta oli jopa sellaisilla lapsilla, jotka joivat päivittäin yli ½ litraa maitoa, harrastivat yli 2,2 tuntia liikuntaa päivässä, jotka saivat päivänvaloa yli 13 t/vrk ja joiden verikoe oli otettu kesän jälkeen (jolloin pitoisuus on suurimmillaan) (Soininen ym. 2016). Moni näin vähän D-vitamiinia saavista lapsista tulee sairastumaan ihan turhaan valtimonkovetustautiin ja muihin pitkäaikaissairauksiin.Lähde: http://www.tritolonen.fi/artikkelit/247-ajankohtainen-d-vitamiini
D-vitamiinin puutos, geenit ja sairastuminen
Geenejä tunnetaan noin 23 000 ja ne ovat aina parilliset sukukromosomien geenejä lukuun ottamatta. Yhden geeniparin sairauksia tunnetaan noin 8000, mutta jokaisen geeniparin toiminnan häiriö voi aiheuttaa jonkun sairauden tai lievemmän poikkeaman. Tällä hetkellä D-vitamiinin säätelemiä geenejä tunnetaan arviolta 2000. MS-taudille altistavia geenimuutoksia on löydetty noin 200.
Perintötekijät vaikuttavat aina sairastumiseen, mutta vain harvoissa sairauksissa perintötekijät määräävät täysin sairastuuko ihminen vai ei. Useimmissa sairauksissa puhutaan ns. monitekijäisestä periytymisestä: eli sairastumiseen vaikuttaa sekä geenit että jokin taudin laukaiseva ympäristötekijä. Lue tästä.
D-vitamiinin puutos on osallisena kymmenissä sairauksissa autoimmuunitaudeista eräisiin syöpiin ja sydän- ja verisuonitauteihin. Syykin on ilmeinen: D-vitamiinin aktiivinen hormonin tavoin vaikuttava aineenvaihduntatuote, kalsitrioli säätelee immuunijärjestelmää ja osallistuu siten mm. solujen kasvuun ja erikoistumiseen. Jos ”hormonin tavoin vaikuttava” ei soita kelloja, kannattaa muistella hormonien merkitystä.
Hormoni on elimistön itse valmistama eli endogeeninen kemiallinen välittäjäaine, joka kulkee erittymispaikastaan kohdesoluihin pääosin verenkierron välityksellä. Hormonit osallistuvat lähes kaikkiin elimistön aineenvaihduntaprosesseihin, ja niitä erittyy eri puolilla elimistöä sijaitsevista umpirauhasista. Aivolisäke säätelee muiden umpirauhasten toimintaa ja hypotalamus säätelee autonomisen hermoston signaalien mukaan aivolisäkkeen toimintaa. Hormoni voi vaikuttaa aivan pieninäkin määrinä sellaiseen soluun, jossa on hormonille spesifisiä reseptoreja.
Hormonit vaikuttavat elimistössä lisääntymisen säätelyyn, kasvuun, kehitykseen sekä energian tuotantoon, käyttöön ja varastointiin.
Hormonit voivat olla joko vesi- tai rasvaliukoisia. Vesiliukoisia hormoneja ovat muun muassa katekoliamiinit, glukagoni ja insuliini, jotka vaikuttavat kohdesolunsa solukalvossa oleviin reseptoreihin. Solukalvon reseptorit puolestaan aktivoivat toisiolähettejä eli cAMP:ta, cGMP:ta tai kalsium-ioneja. Nämä toisiolähetit puolestaan aktivoivat solun toimintaa esimerkiksi aktivoimalla proteiinikinaaseja.
Rasvaliukoisia hormoneja puolestaan ovat steroidit, D-vitamiini ja kilpirauhashormonit, jotka kulkevat verenkierrossa veren proteiineihin sitoutuneina ja sitoutuvat kohdesolunsa reseptoreihin joko solulimassa tai tumassa, koska rasvaliukoisina ne pääsevät solukalvon läpi. Rasvaliukoiset hormonit aktivoivat tai inhiboivat tiettyjen proteiinien proteiinisynteesiä.
Lähde: Wikipedia
A ChIP-seq defined genome-wide map of vitamin D receptor binding: Associations with disease and evolution – Seeram V. Ramagopalan, Andreas Heger, Antonio J. Berlanga etc. 2010
http://atlasgeneticsoncology.org/Genes/GC_VDR.html
Wikigenes: MS-Disease
Sairaudet, joille D-vitamiinin puutos voi altistaa
Michael F. Holick laskeskeli, että D-viamiinia käsitteleviä julkaisuja on ilmestynyt vuoden 1969 jälkeen noin 33 000. D-vitamiinin vaikutuksista eri sairauksiin on siis kirjoitettu äärettömän paljon. En tässä yksilöi ja selvittele sen tarkemmin sairauksia, joille D-vitamiinin puutos altistaa, koska se veisi aivan mielettömästi aikaa. Oheinen lista sisältää linkkejä ko sairautta käsitteleviin tutkimuksiin. Kannattaa tutustua.
Geeni-ympäristö-vuorovaikutus
Vuonna 1902 Sir Archibald Garrod havaitsi, että ruokavalion vaikutukset voivat vaimentaa eräitä synnynnäisiä aineenvaihdunnan häiriöitä. Tämä johti teoriaan geeni-ympäristö-vuorovaikutuksesta (gene-environment interaction), joka nyt yli sata vuotta myöhemmin tarjoaa lääketieteelle huimia mahdollisuuksia.
Geeni-ympäristö-vuorovaikutus vaikuttaa todennäköisesti monimutkaisten neurologisten sairauksien patogeneesissä. Tällaisia vuorovaikutuksia voidaan tarkastella tilastollisesti ja biologisesti. Tilastollinen esimerkki vuorovaikutuksesta löydetään esimerkiksi tupakoinnin ja CFH-geenin väliltä. CFH Y402H-geenimuutos ja tupakointi yhdessä lisäävät silmiä rappeuttavan ARMD-sairauden puhkeamista selvästi enemmän, kuin vain toinen riskitekijöistä yksin. Vaikka taudin mekanismia ei täysin tunneta, voidaan geneettisesti alttiita henkilöitä ohjeistaa geenimuutoksen aiheuttamasta kasvaneesta riskistä ja siihen vaikuttavasta ympäristötekijästä, jonka poistaminen laskee sairastumisen riskiä merkittävästi.
Biologinen vuorovaikutus voidaan määritellä suorista kemiallisista ja fysiologisista havainnoista, joissa ympäristötekijä ja geenimuuttuja reagoivat keskenään, niin, että tämän geeni-ympäristö-vuorovaikutuksen ja taudin etenemisen välille voidaan vetää kausaalinen yhteys. Tällaiset esimerkit ovat harvinaisia. Keliakiassa geneettinen alttius liittyy kromosomissa 6 sijaitsevaiin antigeenin esittelyä sääteleviin HLA-geeneihin ja erityisesti DQ2 ja DQ8-alleeleihin. Ympäristön laukaisevana mekanismina on gluteenin sisältämä glykoproteiini gliadiini.
D-vitamiini, geenit ja MS-taudin patogeneesi
Artikkelin lopuksi käsittelen lyhyesti geenien ja ympäristön merkitystä MS-taudin patogeneesissä.
Tieto D-vitamiinin vaikutusmekanismeista ja MS-taudin ptogeneesistä on kasvanut valtavasti viimeisten 10-15 vuoden aikana. Useat tutkimukset [Hayes, 2000; Van Amerogen et al. 2004; Ascherio & Munger, 2007; Holick, 2007; Ebers, 2008; Nino et al. 2010; Ascherio et al. 2010, 2012; Pierrot_Deseilligny & Souberbielle, 2010; Hanwell & Banwell, 2011; Mowry, 2011; Simon et al. 2012; Hølmoy et al. 2012; van der Mei et al. 2012] osoittavat, että D-vitamiinin puutos vaikuttaa merkittävällä tavalla MS-taudin kehittymiseen. Lue tarkemmin tästä linkistä!
MS-taudin epidemologiset tutkimukset ja runsas tieteellinen näyttö osoittavat sekä geenien että jonkin ympäristössä esiintyvän laukaisevan tekijän vaikuttavan taudin syntyyn. Jos oletetaan, että taudille altistavat geenit pysyvät muuttumattomina, laukaisevan ympäristötekijän merkitys etiologiassa kasvaa. D-vitamiinin puutos ja/tai virheellinen toiminta elimistössä on vahva epäilty taudin laukaisevaksi tekijäksi.
D-vitamiinin ja MS-taudin välinen korrelaatio on tunnettu jo vuosikymmeniä [Goldberg, 1974], mutta viimeisimmät tutkimukset osoittavat kuinka tärkeällä tavalla D-vitamiini osallistuu elimistön immunomodulatorisiin, eli immuunijärjestelmän säätelyyn vaikuttaviin prosesseihin. Juuri tämän immuunijärjestelmän säätelyyn vaikuttavan ominaisuuden kautta D-vitamiinin puutos kytkeytyy merkittävällä tavalla MS-taudin patogeneesiin.
MS-taudin esiintyvyys on runsainta alueilla, joissa auringosta saatava UVB-säteily on vähäisintä ja päinvastoin: Alueilla, joissa UVB-säteilyä saadaan tasaisesti läpi vuoden, riski sairastua MS-tautiin on pieni, ja koska UVB-säteily on välttämätöntä D-vitamiinin luonnolliselle synteesille, on päätelty, että D-vitamiinin puutos vaikuttaa riskiin sairastua MS-tautiin. Teoriaa tukee löydöt, joiden mukaan odottavien äitien alkuraskauden aikaiset alhaiset D-vitamiinitasot lähes kaksinkertaistavat lapsen riskin sairastua MS-tautiin. Lisäksi on havaittu, että MS-potilaiden lapsuudenaikaiset veren D-vitamiini-, eli kalsidiolitasot ((25(OH)D) ovat merkittävästi alhaisemmat kuin sukupuoli-, ikä- ja etnisyys-kontrolloiduilla verrokeilla. Myös Epstein-Barr virusinfektio ja tupakointi kasvattavat sairastumisen riskiä.
MS-taudin esiintyvyys näyttää korreloivan myös eräiden pohjois-eurooppalaisten geenien haploryhmien kanssa. Haploryhmät ovat ihmisen perimän tyyppejä, joka on eri alkuperää olevilla väestöryhmillä erilainen. Tarkemmin haploryhmä on keskenään lähisukuisten DNA:n haplotyyppien joukko tai tietyn geenin tai genominosan kehityslinja lajin sisällä. Esimerkiksi: Skotlannissa ja erityisesti Orkney-saarilla sekä MS-taudia että geenien DR2-haploryhmää esiintyy poikkeuksellisen paljon verrattuna Englantiin.
Eurooppalaistaustaisilla MS-taudin riski pieneni 41 % jokaista seerumin kalsidiolin 50 nmol/l lisäystä kohden; ts. niillä eurooppalaistaustaisilla, joiden veren 25(OH)D oli esimerkiksi 120 nmol/l, riski sairastua oli käytännössä hyvin pieni. Merkittävää on myös se, että esimerkiksi Englannista Etelä-Afrikkaan muuttavien lasten riski putoaa paikallisten hyvin alhaiselle riskitasolle. Sen sijaan Etelä-Afrikasta Englantiin muuttavien lasten riski kasvaa samalle korkealle riskitasolle kuin paikallisilla. Edelleen on osoitettu, että identtisten kaksosten konkordanssiprosentti on 30-40 % (ei-identtisillä kaksosilla ja muilla sisaruksilla selvästi alempi), eli jos toinen identtisistä kaksosista sairastuu, toisen riski sairastua on n. 30-40 %, mikä tukee vahvasti ympäristön roolia sairauden puhkeamisessa.
Kaksostutkimukset osoittavat, että geenit tai geenien haploryhmä eivät riitä selittämään sairastumista, vaan sairastumiselle täytyy olla jokin laukaiseva ympäristötekijä: jokin ympäristömuuttuja, jonka seurauksena toinen identtisistä kaksosista sairastuu ja toinen ei.
”The largest MS genetic association in Northern Europeans is with the extended major histocompatibility complex (MHC) haplotype HLA-DQB1*0602-DQA1*0102-DRB1*1501-DRB5*0101(DR2). Other haplotypes in this region also demonstrate epistatic interactions to modify risk, highlighting the MHC as the key susceptibility locus in MS.” http://www.ncbi.nlm.nih.gov/pmc/articles/PMC2882222/
D-vitamiinin ja HLA-DRB1-geenin vuorovaikutus
Useat HLA-geenialueen alleelit, erityisesti HLA-DRB1*1501, vaikuttavat sairastumiseen. D-vitamiini hydroksyloituu maksassa kalsidioliksi (CYP2R1-geeni) ja munuaisissa aktiiviseksi kalsitrioliksi (CYP27B1-geeni). MS-potilailla on havaittu noin 200 geenimuutosta. Yksi näistä on kalsitriolin hydroksylaatiota munuaisissa säätelevässä CYP27B1-geenissä.
”This (VDR) receptor is a member of the steroid receptor superfamily and influences the rate of transcription of vitamin D–responsive genes by binding to vitamin D response elements (VDREs) in the genome. The effects of vitamin D on MHC class II gene expression have long been appreciated and early studies demonstrate that vitamin D can alter HLA-DR antigen expression and presentation.”
Ramagopalan tutkijaryhmineen halusi löytää sekä geenit että ympäristömuuttujan yhdistävän tekijän MS-taudille altistavista VDRE-lokuksista (geenin tai DNA-jakson sijaintipaikka kromosomissa) ja selvittää, voiko siihen vaikuttaa D-vitamiinilla. Yksittäinen VDRE promoottorioalueen (geenin perusaktiivisuudesta vastaava alue) HLA-DRB1 tunnistettiin. Tällä alueella oli selkeitä, hyvin säilyneitä haplotyyppi-spesifejä eroja tärkeässä MS-tautiin yhdistetyssä DR2-haploryhmässä sekä MS-tautiin vahvasti liittyvä HLA-DRB1*15-alleeli (saman geenin vaihtoehtoinen muoto, jolla on kromosomissa sama lokus eli paikka). HLA-DRB1*15-alleellin 1,25-dihydroksivitamiin D3-herkkyys varmennettiin ja osoitettiin, että tämä VDRE vaikutti geenin ilmenemiseen. On huomattava, että ei-MS-tautiin liittyvissä haploryhmissä VDRE-variantti HLA-DRB1 ei ollut responsiivinen 1,25 hydroksivitamiin D3:lle.

”..a recent study in twins with MS supports the notion that vitamin D levels are under regulation by genetic variation in the 1α-hydroxylase and vitamin D receptor genes, perhaps pointing to their importance in the disease pathogenesis.” – Neurology
Contribution of vitamin D insufficiency to the pathogenesis of multiple sclerosis, Charles Pierrot-Deseilligny, Jean-Claude Souberbielle – 2013
CYP27B1-hypoteesi
Voisiko olla niin, että odottavan äidin alkuraskauden aikaiset alhaiset kalsidiolitasot vaimentavat sikiön CYP27B1-geenin (MS-taudissa yleinen geenimuutos)? Jos näin on, 25(OH)D-1alfa-hydroksylaasi-entsyymin toiminta MS-potilailla on häiriintynyt jo sikiövaiheessa ja se vaikuttaa kalsidiolin hydroksylaatioon munuaisissa, mikä voi estää tai heikentää tärkeän kalsitriolin tuotantoa.
Tässä hypoteesissa geneettinen alttius sairastua MS-tautiin liittyisi CYP27B1-geenin virheelliseen toimintaan ja taudin laukaisevana ympäristötekijänä olisi D-vitamiinin puutos.
MS-taudin patogeneesi voitaisiin siis määritellä siten, että potilaan elimistö ei geenivirheen vuoksi pysty tuottamaan immuunijärjestelmää ja noin 2000 geenin toimintaa säätelevää aktiivista kalsitriolia, joka joidenkin lähteiden mukaan osallistuu sekä solujen kasvuun ja erikoistumiseen että neurologisiin prosesseihin, kuten myeliinin valmistukseen. Jos näin on, meillä on savuava ase ja todennäköisesti toimiva hoitomuoto: kalsitrioli.
Myös ergokalsiferoli muutetaan maksassa kolekalsiferoliksi ja osa siitä 25-hydroksikalsiferoliksi eli kalsidioliksi. Pieni osa kalsidiolista muuttuu pääasiassa munuaisissa mutta myös paksusuolessa, eturauhasessa, rintarauhasessa ja veren valkosoluissa aktiiviseksi kalsitrioliksi eli 1,25-dihydroksikalsiferoliksi. – Wikipedia
Jos kalsitriolia hydroksyloituu pieniä määriä myös munuaisten ulkopuolella, kuten edellinen lainaus antaa ymmärtää, MS-tautia sairastavien kyky tuottaa kalsidiolista kalsitriolia on heikentynyt merkittävästi, mutta elimistö tuottaa sitä edelleen pieniä määriä. Oletan, että jos paksusuolessa, rinta- ja eturauhasessa sekä valkosoluissa hydroksyloituu kalsitriolia, prosessia ohjaa jokin toinen geeni ja entsyymi, kuin munuaisissa tapahtuvaa hydroksylaatiota. Voin olla väärässäkin.
Kalsitriolilla hoidetaan eräitä munuaistauteja sekä perinnöllistä D-vitamiinin aineenvaihdunasairautta sairastavia. Tyypin 1 diabeteksessa haima ei pysty tuottamaan elimistön tarvitsemaa insuliinia, joten potilaan on lääkittävä itseään insuliinilla. Voisiko MS-taudissa kyse olla vastaavasta tilanteesta, jossa munuaisten kyky tuottaa välttämätöntä kalsitriolia olisi häiriintynyt? Voitaisiinko kalsitriolilla hoitaa MS-potilaita samaan tapaan kuin insuliinilla hoidetaan diabeetikkoja? Onko tämä aivn hatusta vedetty hullu ajatus? Ei ole. Kalsitriolin vaikutuksia MS-tautiin on tutkittu mm. Wisconsinin yliopistossa.
VDRE on spesifi DNA-sekvenssi, joka sijaitsee D-vitamiinin ohjaamien geenien promoottorialueella. Promoottorialue vastaa geenin perusaktiivisuudesta. Lokus on geenin tai DNA-jakson sijaintipaikka kromosomissa ja alleeli on saman geenin vaihtoehtoinen muoto, jolla on kromosomissa sama lokus eli paikka.
DNA-molekyyli sisältää kaiken tiedon proteiinien rakentamiseksi ja siten se ohjaa elimistön toimintoja ja rakentumista. DNA:ssa tieto tallennetaan neljän emäksen avulla: adeniini (A), guaniini(G), sytosiini(C) ja tymiini(T). Emäksistä aneniini- ja guaniinimolekyylit muodostuvat kaksirenkaisesta rakenteesta ja niitä kutsutaan puriineiksi. Sytosiini- ja tymiinimolekyylit ovat molekyylirakenteeltaan yksirenkaisia ja niitä sanotaan pyrimidiineiksi. DNA-molekyylin (deoxyribonucleic acid) runko koostuu deoksiriboosi-sokerista ja fosforista.
Solujen välinen viestintä
Solujen välinen viestintä perustuu viestin lähettäjäsolun tuottamaan viestimolekyylin ja viestin vastaanottajasolun ilmentämän reseptoriproteiinin kohtaamiseen.
Viestimolekyylit voivat olla proteiineja, peptidejä, aminohappoja, steroideja tai kaasumaisia yhdisteitä kuten NO. Hydrofobiset eli rasvaliukoiset ja kaasumaiset aineet kulkeutuvat solukalvon läpi, mutta vesiliukoiset eivät läpäise kalvoa. Reseptorit voivat vastaanottajasolussa sijaita joko solukalvolla, solun sytoplasmassa tai tumassa. Solukalvoreseptorin viesti välittyy solussa solunsisäisten viestinvälitysketjujen avulla ja vaikutukset voivat kohdistua solun toiminnan säätelyyn joko proteiini- tai geenitasolla. Sytoplasmassa tai tumassa sijaitsevat tumareseptorit sitoutuvat DNA:han ja vaikuttavat solun geenien ilmenemiseen. Solun sisäiset viestinvälitysmekanismit pohjautuvat peräkkäisiin fosforylaatiotapahtumiin, jotka usein viime kädessä saavat aikaan DNA:han sitoutuvien transkriptiotekijöiden fosforylaatioon ja usein myös transkriptiotekijöiden oligomeerien muodostumiseen. Tällainen aktivoitunut transkriptiotekijä voi DNA:n kohdejaksoonsa sitoutuessaan aktivoida tietyn geenin.
Lähde: Solunetti
The Vitamin D response Element-binding Protein – Hong Chen, Bing Hu, Elizabeth A. Allegretto, John S. Adams
Expression of the Multiple Sclerosis-Associated MHC Class II Allele HLA-DrB1*1501 Is Regulated by Vitamin D – Seeram V. Ramagopalan, Narelle J. Maugen, Lahiru Handunnetthi, Matthew R. Lincoln, Sarah-Michelle Orton, David A. Dyment, Gabriele C. DeLuca etc.
Kalsitrioli tuhoaa autoreaktiivisia T-soluja keskushermostossa
Journal of Neuroimmunology raportoi 6.8.2013 Wisconsinin yliopiston hiirillä tehdystä kokeesta, joka osoitti, että yksi annos biologisesti aktiivista D-vitamiinia, eli kalsitriolia (1,25(OH)2D) tuhosi keskushermostossa tulehdusta ylläpitäviä T-soluja, pysäytti EAE:n etenemisen (experimental autoimmune encephalomyelitis) ja johti EAE-taudin remissioon. Kalsitrioli aktivoi keskushermoston uinuvat T-auttajasolut (Treg), jotka hillitsevät immuunivastetta ja laskivat kudoksia tuhoavien Th1- ja Th17-solujen määrää. – Lähde: Multiple Sclerosis Discovery Forum.
CALCITRIOL, VITAMIN D AND MULTIPLE SCLEROSIS – Dr. C. E. Hayes, Ph.D.,Professor of Biochemistry, U. Wisconsin, Madison, Wi, 2014
Mouse studies reveal promising vitamin D-based treatment for MS
Th-solujen alaluokkien toiminnan ymmärtämisellä on myös kliinistä merkitystä. Esimerkiksi Th17-alatyypin toiminnan estävillä lääkkeillä toivotaan olevan autoimmuunitaudeissa sekä hyvä teho että mahdollisimman vähän vaikutuksia muuhun kuin ei-toivottuun immuunivasteeseen (van den Berg ja Miossec 2009). Lisäksi Th-solujen alatyyppien toiminnan molekylaarisen taustan tutkiminen valaisee myös häiriytyneen immunivasteen aiheuttamien tautien patogeneesiä. Tästä hyvänä esimerkkinä on tulehdusta kiihdyttävän Th1-alatyypin synnyssä välttämättömän Stat4-transkriptiotekijän geneettinen yhteys reumaan ja SLE:hen samoin kuin tuore suomalainen tutkimustulos, jonka mukaan Th17-solujen toimintaa säätelevän Stat3:n mutaatio suojaa MS-taudin kehittymiseltä (Remmers ym. 2007, Jakkula ym. 2010).
Lähde: Lääketieteellinen aikakauskirja Duodecim
EAE on MS-tautia muistuttava eläinten autoimmuunitauti, jonka tutkimusta sovelletaan MS-taudin tutkimukseen. MS-taudissa elimistön oma immuunijärjestelmä tuhoaa keskushermoston kudoksia, erityisesti aksoneita suojaavaa myeliiniä (demyelinoiva prosessi), mikä aiheuttaa keskushermostossa kulkevien signaalien hidastumista ja edelleen taudille ominaisia oireita. Käytännössä elimistön immuunijärjestelmän solut menevät sekaisin ja niistä tulee ”tuholaisia”.
Multiple sclerosis (MS) is an incurable inflammatory demyelinating disease. We investigated one calcitriol dose plus vitamin D3 (calcitriol/+D) as a demyelinating disease treatment in experimental autoimmune encephalomyelitis (EAE). Evidence that calcitriol-vitamin D receptor pathway deficits may promote MS, and data showing calcitriol enhancement of autoimmune T cell apoptosis provided the rationale. Whereas vitamin D3 alone was ineffective, calcitriol/+D transiently increased central nervous system (CNS) Helios(+)FoxP3(+) T cells and sustainably decreased CNS T cells, pathology, and neurological deficits in mice with EAE. Calcitriol/+D, which was more effective than methylprednisolone, has potential for reversing inflammatory demyelinating disease safely and cost-effectively. – Nashold et al. 2013
Coimbra-protokolla
Brasiliassa MS-tautia ja muita autoimmuunitauteja hoidetaan ns. Coimbra-protokollan mukaisilla jopa 50 000 IU (1250 µg) D-vitamiiniannoksilla. Hoitotulokset ovat lupaavia, mutta tietoa Coimbra-protokollasta on saatavilla lähinnä portugaliksi. Michael F. Holick puhuu artikkelin alussa olevalla videolla Coimbra-protokollasta hyvin positiiviseen sävyyn. Euroopassa ja USA:ssa on yhteensä joitakin kymmeniä lääkäreitä, jotka noudattavat tätä hoitomuotoa. Oheisella videolla Coimbra kertoo hoidosta. Video on italiankielinen, mutta siihen on englanninkieliset tekstitykset.
D-vitamiinin tutkimus
Suuri tutkimustietokanta (PubMed) antaa haulla: ”Vitamin D” yli 67 000 osumaa. Se osoittaa, että D-vitamiini on kansainvälisissä tutkijapiireissä ”kuuma” aihe, johon viitataan tutkimuksissa hyvin aktiivisesti. D-vitamiinia käsittelevien tutkimusten selvittäminen ja jäsentely yksiin kansiin toisi motivoituneelle tutkijaryhmälle työsarkaa vuosiksi eteenpäin.
VitaminDwiki ylläpitää myös tutkimustietokantaa, joka raportoi säännöllisesti D-vitamiinia käsittelevistä uusista tutkimuksista. Sivustolla tutkimukset on organisoitu D-vitamiinin puutokseen liittyvien sairauksien mukaan.
Yhteinen nimittäjä viime vuosien tutkimuksissa on se, että D-vitamiinin puutos toimii altistavana tekijänä monille sairauksille ja, että monilla sairailla mitataan keskiarvoa selvästi alhaisempia kalsidiolipitoisuuksia. Se ei voi olla sattumaa.
D-vitamiinin tutkimukseen ja kansainväliseen D-vitamiinin merkitystä korostavaan tendenssiin suomalaiset viranomaistahot suhtautuvat väheksyvästi. Se on hullua, kun huomioidaan, että D-vitamiinilla on ollut keskeinen merkitys immuunijärjestelmän säätelijänä koko ihmisen kehityshistorian ajan, sekä siksi, että uusimmissa tutkimuksissa D-vitamiinin merkitys n. 2000 geenin säätelijänä ja immunomodulatorisena vaikuttajana on entisestään vahvistunut.
Tuhannet tutkimukset tukevat D-vitamiiniin liittyviä terveysväittämiä. Se ei ehkä yksin paranna sairauksia, mutta riittävät D-vitamiinitasot antavat hyvän ja tarpeellisen suojan sekä ehkäisevät monien sairauksien puhkeamista. Itse pidän hyvin todennäköisenä, että kalsitrioli voi toimia MS-taudin oireita helpottavana – jopa tapahtuneita myeliinivaurioita korjaavana lääkkeenä.
loista ja aurinkoista alkanutta kevättä kaikille!
T: Sami











