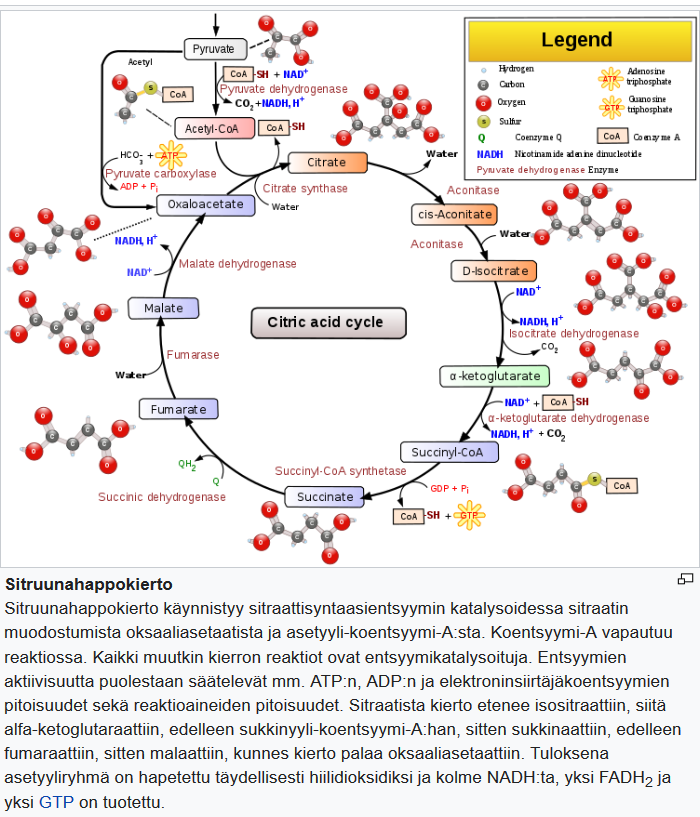
Ketogeeninen ruokavalio, sydän- ja verisuonitaudit 3: ketoaineet ja energiametabolismi
Ketogeenisen ruokavalion (KD) vaikutusta sydämen energia-aineenvaihduntaan tutkitaan ja kuvataan yhä enemmän. Tämä johtuu ketoosista, jossa ketoaineiden (asetonin, asetoasetaatin ja β-hydroksibutyraatin) tuotanto lisääntyy. β-hydroksibutyraatti, vaikuttaa erityisesti sydänlihaksen ja aivojen aineenvaihduntaan ja toimintaan. Toisin kuin pitkäketjuiset rasvahapot, se läpäisee veri-aivoesteen.
Ketoaineet ja sydämen energiametabolia
Kaikista elimistä sydämellä ja aivoilla on suurin energiantarve. Tämä johtuu tarpeesta työskennellä jatkuvasti sikiöstä kuolemaan asti. Sydänlihaksen soluille (kardiomyosyyteille) on ominaista kehon korkeimmat mitokondrioiden pitoisuudet. Mitokondriot ovat solujen energiakeskuksia, sillä ne vastaavat energian tuotannosta adenosiinitrifosfaatin (ATP) muodossa [144,145].
ATP:n saamiseksi sydän voi käyttää asetyylikoentsyymi A:ta (asetyyli-CoA) glukoosista (glykolyysin kautta) tai lipideistä (β-oksidaation kautta).
Normaaliolosuhteissa rasvahapoista peräisin oleva asetyyli-CoA on ensisijainen substraatti ATP:n tuotannolle sydämessä. HFrEF-potilailla ketoaineiden hapettumisen osuus sydänlihaksen ATP-tuotannosta kasvaa 6,4 prosentista (kontrolliryhmässä) 16,4 prosenttiin [146]. Ketoaineet ovat hyvä ja monissa tapauksissa jopa glukoosia parempi energialähde ATP:n tuotannolle [97,147].
Sydänsairauden alkuvaiheessa sydän voi siirtää energiankäyttönsä rasvahapoista glukoosiin, mikä liittyy aineenvaihdunnan joustavuuden menetykseen [98,148]. Toisaalta ei tiedetä varmasti, johtuuko aineenvaihdunnan poikkeavuudet sydänsairauden puhkeamisesta vai onko sydänsairaus aineenvaihdunnan poikkeavuuksien seuraus [149].
Energiametabolian muutokset voivat lopulta aiheuttaa sydämen vajaatoimintaa, mikä johtaa sydämen aineenvaihdunnan uudelleenohjelmointiin kohti ketoaineiden ottoa ja käyttöä energianlähteenä. Se, että tämä voi olla adaptiivinen vaste, tarjoaa vakuuttavan argumentin ketoaineiden merkityksestä sydämen aineenvaihdunnalle. Tätä tukevat useat julkaisut, jotka osoittavat ketoaineiden suurempia pitoisuuksia ja suurempaa ottoa muun muassa sydämen vajaatoiminnan yhteydessä [150,151,152,153,154].
Sydän suosii ketoaineita glukoosiin verrattuna olosuhteissa, joissa molemmat substraatit ovat saatavilla. Tämä osoitettiin Gormsenin ym. tutkimuksessa, jossa ketoaineiden pitoisuuden nostaminen 3,8 mM:iin johti sydänlihaksen glukoosinottoon 50 %:n vähenemiseen. Tämä tapahtui maksimaalisesta insuliinistimulaatiosta ja riittävästä glukoosipitoisuudesta huolimatta [155].
Näyttää siltä, että ketoaineiden lisääntynyt hapettuminen on erityisen hyödyllistä sydämelle (ja aivoille), koska hyperketonemia ei vaikuta glukoosin ja rasvahappojen ottokykyyn muissa elimissä [156,157].
Sydämen energiankulutuksen lisääntymisen ja kahden ketoaineen, BHB:n ja asetonin, pitoisuuksien välillä on havaittu positiivinen yhteys [158]. Horton ym. osoitti ketoaineiden sydämen kannalta merkityksellisyyden käyttämällä esimerkkinä Cre-lox BDH1-KO -hiirten sydämiä, joilta puuttui D-β-hydroksibutyraattidehydrogenaasi (BDH1), ketoaineiden hapetuksesta vastaava mitokondrioentsyymi (se katalysoi 3-hydroksibutyraatin (3OHB) hapettumisen ensimmäistä vaihetta) [150].
Hiirillä, joilla ei ollut BDH1:tä, sydämen vajaatoiminta paheni paaston tai paineen aiheuttaman ylikuormituksen/iskemian seurauksena verrattuna hiiriin, joilla oli BDH1. Samalla lisääntynyt hydroksibutyraatin anto paransi patologista sydämen uudelleenmuodostusta ja toimintahäiriöitä sekä eristettyjen mitokondrioiden bioenergeettistä termodynamiikkaa rasvahappojen käytön vähenemisen aikana.
Sydän lisää ketoaineiden käyttöä metabolisen stressin seurauksena. On arveltu, että ketoaineiden anto voi olla tärkeä osa sydämen vajaatoiminnan hoitoa. Toinen tutkimus osoitti, että kaikkien ketoaineiden pitoisuus oli lähes kaksi kertaa korkeampi sydämen vajaatoimintaa sairastavilla koirilla verrattuna kontrollikoiriin. Lisäksi folistatiini 1:n kaltaisen sydäntä suojaavan proteiinin (FSTL1) antaminen vähensi ketoaineiden ottoa [159].
Vaikka suurin osa tutkimuksesta keskittyy eksogeenisten ketonien vaikutukseen sydämen energia-aineenvaihduntaan, on myös julkaisuja, jotka tarkastelevat itse ketogeenisen ruokavalion suoraa vaikutusta. Guo et al. raportoivat kiinnostavia havaintoja vuoden 2022 tutkimuksessa. Tutkimus osoitti, että joka toinen päivä noudatettu ketogeeninen ruokavalio suojasi sydämen vajaatoiminnalta aiheuttamalla vahvan sydäntä suojaavan vaikutuksen.
8 viikon jatkuvan ketogeenisen ruokavalion aikana ei osoitettu sydämen vajaatoiminnalta suojaavia vaikutuksia. Kirjoittajat päättelivät, että vaikka ketogeenisen ruokavalion jatkuva käyttö heikensi maksan ketogeneesikapasiteettia, joka toinen päivä toteutettuna maksan ketogeneesi ei hidastunut [160].
Vuonna 2017 tehdyssä 3,2 vuotta kestäneessä väestöpohjaisessa tutkimuksessa havaittiin yhteys kohonneiden BHB-tasojen ja sydän- ja verisuonitapahtumien riskin lisääntymiseen 405 hemodialyysihoitoa saavalla iäkkäällä potilaalla. Kirjoittajat ilmoittivat, että kohonneet BHB-tasot liittyivät itsenäisesti sydän- ja verisuonitapahtumiin ja mistä tahansa syystä johtuvaan kuolemaan tutkitussa potilasryhmässä [161].
Vaikka sukupuolten välillä ei havaittu eroja tuloksissa, toinen, suurempi väestöpohjainen tutkimus osoitti eroja. Flores-Guerrero ym. osoittivat, että korkeat plasman BHB-tasot liittyivät lisääntyneeseen sydämen vajaatoiminnan riskiin ja pienentyneeseen ejektiofraktioon (HFrEF), erityisesti naisilla [162].
Molemmissa tutkimuksissa saadut tulokset antavat alustavan kuvan syy-yhteydestä. Samaan aikaan, kuten aiemmissa julkaisuissa on osoitettu, sydämen vajaatoiminnassa (ja muissa sydänvaurioissa) ketoaineiden pitoisuus kasvaa, ja tätä tulisi pitää pikemminkin ”pelastuspolttoaineena”. Tulokset/havainnot siis vahvistavat, että ketoaineet ovat tärkeitä sairaan sydämen toiminnalle. Tätä tukee vuoden 2023 julkaisu [163].
Kashiwagin ym. tutkimus osoitti, että B-tyypin natriureettinen peptidi (BNP) voi indusoida kohonneita ketoaineiden pitoisuuksia, joita voidaan käyttää tärkeänä vaihtoehtoisena polttoaineena vajaatoimintaisessa sydämessä. Kirjoittajat osoittivat, että BNP stimuloi korkeampia ketoaineiden pitoisuuksia voimakkaammin kuin hemodynamiikan heikkeneminen. Tämä johtui havainnosta, että ketoaineiden ja BNP-pitoisuuksien välillä oli positiivinen korrelaatio, mutta ei ketoaineiden ja vasemman kammion loppudiastolisen paineen (LVEDP), vasemman kammion loppusystolisen tilavuusindeksin (LVESVI) ja vasemman kammion loppudiastolisen tilavuusindeksin (LVEDVI) välillä [164].
Sydämen vajaatoimintaa sairastavilla potilailla havaittujen korkeampien β-hydroksibutyraattipitoisuuksien lisäksi tämä ilmeni myös asetonin (yksi ketoaineista) lisääntyneenä määränä näiden henkilöiden uloshengitysilmassa.
Yhdessä tutkimuksessa havaittiin, että HFrEF-potilailla oli kohonneet asetonipitoisuudet, ja mikä tärkeintä, nämä olivat kääntäen verrannollisia sydämen toimintaan.
Kirjoittajat totesivat, että korkeat uloshengitysilman asetonipitoisuudet voivat liittyä huonoon ennusteeseen HFrEF-potilailla [165]. EMPA-RESPONSE-AHF-tutkimukseen osallistuneen 79 akuuttia sydämen vajaatoimintaa sairastavan potilaan post hoc -analyysissä osoitettiin, että ketoaineiden, erityisesti asetonin, pitoisuudet olivat merkittävästi koholla akuutin dekompensoidun sydämen vajaatoiminnan aikana verrattuna tilan vakauttamiseen [166].
Satunnaistetussa kontrolloidussa tutkimuksessa Nielsen ym. osoittivat, että 3-hydroksibutyraatin (3-OHB) anto sydämen vajaatoimintaa sairastaville potilaille lisäsi sydämen minuuttitilavuutta 2,0 ± 0,2 l/min. Iskutilavuus kasvoi 20 ± 2 ml ja syke 7 ± 2 lyöntiä minuutissa (BPM). Lisäksi vasemman kammion ejektiofraktio nousi 8 ± 1 %. Kirjoittajat päättelivät, että seerumin BHB-pitoisuuden nousulla fysiologisella tasolla oli hyödyllisiä hemodynaamisia vaikutuksia potilailla, joilla oli HFrEF ilman heikentynyttä sydänlihaksen ulkoista tehokkuutta (MEE) [167]. Nasser ym. osoittivat mainittujen tutkimusten [151,152,168,169,170] perusteella, että ketoaineet (jotka ovat peräisin ketogeenisestä ruokavaliosta) voivat parantaa sydänlihaksen toimintaa ja edistää sydän- ja verisuonitautien toimintahäiriöistä kärsivien potilaiden tehokkaampaa hoitoa [97].
On myös useita muita todisteita ketoaineiden huomattavasta merkityksestä sydämen toiminnalle, kuten muun muassa Abdul ym. ovat kuvanneet [147]. Toisen julkaisun johtopäätökset viittaavat siihen, että ketogeeninen ruokavalio on kiehtova ei-farmakologinen vaihtoehto sydän- ja verisuonisairauksien, erityisesti sydämen vajaatoiminnan, hoitoon ja ehkäisyyn [171].
Vuoden 2023 julkaisu osoittaa, että todisteet tukevat ketoaineiden aineenvaihdunnan adaptiivista roolia sydämen vajaatoiminnassa sydänelinten normaalin toiminnan edistämisessä ja taudin etenemisen lieventämisessä [172].
Keskipitkäketjuiset rasvahapot (MCT) ovat tärkeässä roolissa ketogeenisissä ruokavalioissa [173]. Tämä johtuu siitä, että ne ovat ketogeenisimpiä rasvahappoja. Ne sulavat helposti ja johtavat ketonien nopeampaan tuotantoon verrattuna pitkäketjuisiin rasvahappoihin.
MCT:t edustavat ”nopeaa energiaa”, koska toisin kuin pitkäketjuiset rasvahapot, ne eivät vaadi haiman entsyymejä sulatukseen ja ohittavat tavanomaisen reitin ruoansulatuskanavan läpi, kulkeutuvat porttilaskimon kautta maksaan ja tarjoavat nopean energialähteen tai muuntuvat ketoaineiksi [19].
MCT-rasvojen korkean ketogeenisyyden vuoksi ne voivat olla hyödyllinen osa sydämen metabolista terveyttä erityisesti yhdistettynä ketogeeniseen ruokavalioon.
Tämä on entistäkin tärkeämpää, koska MCT-rasvojen on osoitettu lisäävän mitokondrioiden biosynteesiä ja aineenvaihduntaa (jota esiintyy pääasiassa sydänlihassoluissa), mikä parantaa suorituskykyä liikunnan aikana [174].
Lisäksi havaittiin, että sepelvaltimotautia sairastavilla potilailla kookosöljyn (joka on MCT-rasvojen lähde) sisällyttäminen lisäsi HDL-kolesterolin osuutta ja pienensi vyötärön ympärysmittaa [175]. MCT-rasvojen monitahoisten hyödyllisten vaikutusten vuoksi niiden lisääminen ruokavalioon on perusteltua.
Lyhytketjuisilla rasvahapoilla (MCT) on erityinen vaikutus aivojen ja sydämen energiantuotantoon, koska ne imeytyvät ja metaboloituvat nopeammin kuin tavalliset pitkäketjuiset rasvahapot. Erityisesti aivojen osalta, kun glukoosin hyödyntäminen heikkenee (esim. ikääntyessä tai tiettyjen sairauksien yhteydessä), MCT-rasvahapot tarjoavat vaihtoehtoisen energianlähteen tuottamalla ketoaineita maksassa. Nämä ketoaineet voivat ylittää veri-aivoesteen ja toimia aivosolujen polttoaineena.
Vaikutukset aivoihin
MCT-rasvahapot, erityisesti MCT-öljyn muodossa, ovat tunnettuja siitä, että ne tarjoavat nopeaa energiaa aivoille. Aivot käyttävät yleensä glukoosia pääasiallisena energianlähteenä, mutta tietyissä tilanteissa, kuten ketogeenisellä ruokavaliolla tai aineenvaihdunnan häiriöissä, ketoaineet voivat toimia tehokkaana korvaavana polttoaineena. Esimerkiksi Alzheimerin taudissa aivojen glukoosiaineenvaihdunta heikkenee, ja MCT-öljyn on tutkittu tuovan apua tarjoamalla aivoille vaihtoehtoisen energialähteen.
Vaikutukset sydämeen
Vaikka MCT-rasvahapot muistuttavat kemiallisesti pitkäketjuisia rasvahappoja, niiden metabolia eroaa merkittävästi. Sydämen energiantuotannon kannalta on havaittu, että MCT-rasvahapot voivat parantaa sydämen toimintaa tietyissä tilanteissa, kuten rasvahappojen hapettumishäiriöistä kärsivillä potilailla. Sydämen terveydestä yleisesti puhuttaessa tutkimustulokset ovat kuitenkin ristiriitaisia.
Joissain tutkimuksissa MCT-rasvahapoilla on havaittu olevan positiivisia, tulehdusta vähentäviä vaikutuksia, kun taas toisissa tutkimuksissa on havaittu, että ne voivat huonontaa kolesteroliarvoja (esim. LDL- ja HDL-kolesterolin suhdetta), mikä viittaa mahdolliseen lisääntyneeseen sydän- ja verisuonitautien riskiin. On tärkeää huomata, että lisätutkimuksia tarvitaan, jotta ymmärrettäisiin paremmin MCT-rasvahappojen kokonaisvaikutus sydämen terveyteen.
β-hydroksibutyraatti
β-hydroksibutyraatti (BHB) on yksi tärkeimmistä ketonirungoista (toiset ovat aseoasetaatti ja asetoni). Sitä syntyy maksassa rasvahapoista, kun hiilihydraattien saanti on vähäistä (paasto, ketogeeninen ruokavalio, raskas liikunta, nälkiintyminen). BHB ei ole pelkkä vaihtoehtoinen energialähde, vaan sillä on myös signaalimolekyylin rooleja.
Vaikutukset aivoihin
- Energia-aineenvaihdunta
- Aivot eivät voi käyttää rasvahappoja suoraan, mutta BHB läpäisee veri–aivoesteen monokarboksylaattikuljettajien (MCT1/2) avulla.
- BHB muuttuu takaisin asetoasetaatiksi ja sitten asetyyli-CoA:ksi → käytetään sitruunahappokierrossa ATP:n tuottamiseen.
- Pitkittyneessä ketoosissa BHB voi kattaa jopa 60–70 % aivojen energiantarpeesta.
- Hermoston suojaus
- BHB vähentää oksidatiivista stressiä tehostamalla mitokondrioiden toimintaa.
- Lisää GABA:n (rauhottava välittäjäaine) ja vähentää glutamaatin (kiihottava välittäjäaine) vaikutusta → voi selittää ketogeenisen ruokavalion epilepsialle edullisia vaikutuksia.
- Toimii HDAC-estäjänä (histoni-deasetylaasi-inhibitio) → vaikuttaa geenien säätelyyn, mm. antioksidanttien ja neurotrofisten tekijöiden (BDNF) lisäämiseen.
- Saattaa suojata Alzheimerin ja Parkinsonin taudeissa energiapuutteen ja tulehduksen yhteydessä.
- Kognitio ja mieliala
- Monet kokevat selkeämpää ajattelua ja tarkkaavaisuuden paranemista ketoosissa. Mekanismeina energiatehokkuus, vakaa verensokeri ja välittäjäaineiden muutokset.
Vaikutukset sydämeen
- Energianlähde
- Sydänlihas käyttää normaalisti paljon rasvahappoja. Ketoosissa BHB:sta tulee merkittävä energiasubstraatti.
- BHB on ”puhtaampi polttoaine” kuin rasvahapot: tuottaa enemmän ATP:tä suhteessa kulutettuun happeen → parempi energiatehokkuus.
- Iskeemiasuoja
- BHB vähentää oksidatiivista stressiä ja parantaa mitokondrioiden toimintaa hapenpuutteessa.
- Eläin- ja kliinisissä tutkimuksissa ketonien lisääntyminen on liittynyt sydämen vajaatoiminnan oireiden lievenemiseen.
- Sydänsairauksissa
- Uusissa tutkimuksissa sydämen vajaatoimintapotilailla mitattiin kohonneita ketonipitoisuuksia – joiden tulkitaan olevan sydämen kompensatorinen keino hankkia energiaa, kun rasvahappojen käyttö on rajoittunut.
- BHB-infuusio voi parantaa sydämen pumppaustehoa joissakin tutkimuksissa.
Yhteenveto
- Aivoissa: BHB toimii tärkeänä energiavaihtoehtona, vähentää hermoston yliärsytystä ja oksidatiivista stressiä, sekä vaikuttaa suotuisasti geenien säätelyyn ja kognitioon.
- Sydämessä: BHB parantaa energiatehokkuutta, vähentää oksidatiivista stressiä ja saattaa suojata vajaatoiminnassa tai iskemiatilanteissa.
| Ominaisuus | Aivot | Sydän |
| Energianlähde | Läpäisee veri–aivoesteen, kattaa ketoosissa jopa 60–70 % energiantarpeesta | Korvaa osittain rasvahapot, tuottaa enemmän ATP:tä per käytetty happi (energiatehokkaampi) |
| Metabolinen hyöty | Vähentää verensokerin vaihtelua, vakauttaa energiansaantia | Tehostaa mitokondrioiden toimintaa, säästää happea |
| Hermoston / kudoksen suojaus | Lisää antioksidanttien tuotantoa, vähentää oksidatiivista stressiä ja tulehdusta | Vähentää oksidatiivista stressiä, suojaa iskemialta ja vajaatoiminnalta |
| Geenien säätely | Toimii HDAC-estäjänä → lisää BDNF:ää ja muita suojaavia tekijöitä | Voi muuttaa geenien ilmentymistä energiansaantia tehostavaan suuntaan |
| Välittäjäainevaikutukset | Lisää GABA-aktiivisuutta, vähentää glutamaattia → epilepsian ja hermoston yliärsytyksen hillintä | Ei suoraa vaikutusta välittäjäaineisiin, mutta parantaa pumppaustehoa vajaatoiminnassa |
| Kliininen merkitys | Käytetään epilepsian hoidossa (ketogeeninen ruokavalio), tutkitaan Alzheimerin ja Parkinsonin taudeissa | Sydämen vajaatoimintapotilailla kohonneet BHB-tasot liittyvät kompensaatioon; infuusio voi parantaa suorituskykyä |
Kirjoittajat: Damian Dyńka , Katarzyna Kowalcze , Anna Charuta , Agnieszka Paziewska ,*
Alkuperäinen artikkeli: https://pmc.ncbi.nlm.nih.gov/articles/PMC10421332/
Käännös & editointi: Sami Raja-Halli
Lähdeviitteet
143.Liu S.H., Chen Y.X., Tzeng H.P., Chiang M.T. Fish Oil Enriched n-3 Polyunsaturated Fatty Acids Improve Ketogenic Low-Carbohydrate/High-Fat Diet-Caused Dyslipidemia, Excessive Fat Accumulation, and Weight Control in Rats. Nutrients. 2022;14:1796. doi: 10.3390/nu14091796. [DOI] [PMC free article] [PubMed] [Google Scholar]
144.Stoll S., Leimena C., Qiu H. Mitochondria and Heart Disease. InTech; London, UK: 2018. [DOI] [Google Scholar]
145.Brown D.A., Perry J.B., Allen M.E., Sabbah H.N., Stauffer B.L., Shaikh S.R., Cleland J.G.F., Colucci W.S., Butler J., Voors A.A., et al. Expert consensus document: Mitochondrial function as a therapeutictarget in heart failure. [(accessed on 24 April 2023)];Nat. Rev. Cardiol. 2017 14:238–250. doi: 10.1038/nrcardihttps://www.researchgate.net/publication/327299198_Mitochondria_and_Heart_Diseaseo.2016.203. Available online: . [DOI] [PMC free article] [PubMed] [Google Scholar]
146.Murashige D., Jang C., Neinast M., Edwards J.J., Cowan A., Hyman M.C., Rabinowitz J.D., Frankel D.S., Arany Z. Comprehensive quantification of fuel use by the failing and nonfailing human heart. Science. 2020;370:364–368. doi: 10.1126/science.abc8861. [DOI] [PMC free article] [PubMed] [Google Scholar]
147.Abdul Kadir A., Clarke K., Evans R.D. Cardiac ketone body metabolism. Biochim. Biophys. Acta Mol. Basis Dis. 2020;1866:165739. doi: 10.1016/j.bbadis.2020.165739. [DOI] [PubMed] [Google Scholar]
148.Sack M.N., Rader T.A., Park S., Bastin J., McCune S.A., Kelly D.P. Fatty acid oxidation enzyme gene expression is downregulated in the failing heart. Circulation. 1996;94:2837–2842. doi: 10.1161/01.cir.94.11.2837. [DOI] [PubMed] [Google Scholar]
149.Carley A.N., Taegtmeyer H., Lewandowski E.D. Matrix revisited: Mechanisms linking energy substrate metabolism to the function of the heart. Circ. Res. 2014;114:717–729. doi: 10.1161/CIRCRESAHA.114.301863. [DOI] [PMC free article] [PubMed] [Google Scholar]
150.Horton J.L., Davidson M.T., Kurishima C., Vega R.B., Powers J.C., Matsuura T.R., Petucci C., Lewandowski E.D., Crawford P.A., Muoio D.M., et al. The failing heart utilizes 3-hydroxybutyrate as a metabolic stress defense. JCI Insight. 2019;4:e124079. doi: 10.1172/jci.insight.124079. [DOI] [PMC free article] [PubMed] [Google Scholar]
151.Bedi K.C., Snyder N.W., Brandimarto J., Aziz M., Mesaros C., Worth A.J., Wang L.L., Javaheri A., Blair I.A., Margulies K.B., et al. Evidence for intramyocardial disruption of lipid metabolism and increased myocardial ketone utilization in advanced human heart failure. Circulation. 2016;133:706–716. doi: 10.1161/CIRCULATIONAHA.115.017545. [DOI] [PMC free article] [PubMed] [Google Scholar]
152.Aubert G., Martin O.J., Horton J.L., Lai L., Vega R.B., Leone T.C., Koves T., Gardell S.J., Krüger M., Hoppel C.L., et al. The Failing Heart Relies on Ketone Bodies as a Fuel. Circulation. 2016;133:698–705. doi: 10.1161/CIRCULATIONAHA.115.017355. [DOI] [PMC free article] [PubMed] [Google Scholar]
153.Lommi M.D.J. Blood ketone bodies in congestive heart failure. J. Am. Coll. Cardiol. 1996;28:665–672. doi: 10.1016/0735-1097(96)00214-8. [DOI] [PubMed] [Google Scholar]
154.Voros G., Ector J., Garweg C., Droogne W., Van Cleemput J., Peersman N., Vermeersch P., Janssens S. Increased cardiac uptake of ketone bodies and free fatty acids in human heart failure and hypertrophic left ventricular remodeling. Circ. Heart Fail. 2018;11:e004953. doi: 10.1161/CIRCHEARTFAILURE.118.004953. [DOI] [PubMed] [Google Scholar]
155.Gormsen L.C., Svart M., Thomsen H.H., Sondergaard E., Vendelbo M.H., Chris-tensen N., Tolbod L.P., Harms H.J., Nielsen R., Wiggers H., et al. Ketone Body Infusion with 3-Hydroxybutyrate Reduces Myocardial Glucose Uptake and Increases Blood Flow in Humans: A Positron Emission Tomography Study. J. Am. Heart Assoc. 2017;6:e005066. doi: 10.1161/JAHA.116.005066. [DOI] [PMC free article] [PubMed] [Google Scholar]
156.Svart M., Gormsen L.C., Hansen J., Zeidler D., Gejl M., Vang K., Aanerud J., Moeller N. Regional cerebral effects of ketone body infusion with 3-hydroxybutyrate in humans: Reduced glucose uptake, unchanged oxygen consumption and increased blood flow by positron emission tomography. A randomized, controlled trial. PLoS ONE. 2018;13:e0190556. doi: 10.1371/journal.pone.0190556. [DOI] [PMC free article] [PubMed] [Google Scholar]
157.Lauritsen K.M., Søndergaard E., Luong T.V., Møller N., Gormsen L.C. Acute Hyperketonemia Does Not Affect Glucose or Palmitate Uptake in Abdominal Organs or Skeletal Muscle. J. Clin. Endocrinol. Metab. 2020;105:1785–1790. doi: 10.1210/clinem/dgaa122. [DOI] [PubMed] [Google Scholar]
158.Du Z., Shen A., Huang Y., Su L., Lai W., Wang P., Xie Z., Xie Z., Zeng Q., Ren H., et al. 1H-NMR-based metabolic analysis of human serum reveals novel markers of myocardial energy expenditure in heart failure patients. PLoS ONE. 2014;9:e88102. doi: 10.1371/journal.pone.0088102. [DOI] [PMC free article] [PubMed] [Google Scholar]
159.Seki M., Powers J.C., Maruyama S., Zuriaga M.A., Wu C.L., Kurishima C., Kim L., Johnson J., Poidomani A., Wang T., et al. Acute and chronic increases of circulating FSTL1 normalize energy substrate metabolism in pacing-induced heart failure. Circulation. 2018;11:e004486. doi: 10.1161/CIRCHEARTFAILURE.117.004486. [DOI] [PMC free article] [PubMed] [Google Scholar]
160.Guo Y., Liu X., Li T., Zhao J., Yang Y., Yao Y., Wang L., Yang B., Ren G., Tan Y., et al. Alternate-Day Ketogenic Diet Feeding Protects against Heart Failure through Preservation of Ketogenesis in the Liver. Oxid. Med. Cell. Longev. 2022;2022:4253651. doi: 10.1155/2022/4253651. [DOI] [PMC free article] [PubMed] [Google Scholar]
161.Obokata M., Negishi K., Sunaga H., Ishida H., Ito K., Ogawa T., Iso T., Ando Y., Kurabayashi M. Association between Circulating Ketone Bodies and Worse Outcomes in Hemodialysis Patients. J. Am. Heart Assoc. 2017;6:e006885. doi: 10.1161/JAHA.117.006885. [DOI] [PMC free article] [PubMed] [Google Scholar]
162.Flores-Guerrero J.L., Westenbrink B.D., Connelly M.A., Otvos J.D., Groothof D., Shalaurova I., Garcia E., Navis G., de Boer R.A., Bakker S.J.L., et al. Association of beta-hydroxybutyrate with development of heart failure: Sex differences in a Dutch population cohort. Eur. J. Clin. Investig. 2021;51:e13468. doi: 10.1111/eci.13468. [DOI] [PMC free article] [PubMed] [Google Scholar]
163.Manolis A.S., Manolis T.A., Manolis A.A. Ketone Bodies and Cardiovascular Disease: An Alternate Fuel Source to the Rescue. Int. J. Mol. Sci. 2023;24:3534. doi: 10.3390/ijms24043534. [DOI] [PMC free article] [PubMed] [Google Scholar]
164.Kashiwagi Y., Nagoshi T., Inoue Y., Tanaka Y., Takahashi H., Oi Y., Kimura H., Minai K., Yoshimura M. Close linkage between blood total ketone body levels and B-type natriuretic peptide levels in patients with cardiovascular disorders. Sci. Rep. 2021;11:6498. doi: 10.1038/s41598-021-86126-0. [DOI] [PMC free article] [PubMed] [Google Scholar]
165.Marcondes-Braga F.G., Batista G.L., Gutz I.G.R., Saldiva P.H.N., Mangini S., Issa V.S., Ayub-Ferreira S.M., Bocchi E.A., Pereira A.C., Bacal F. Impact of exhaled breath acetone in the prognosis of patients with heart failure with reduced ejection fraction (HFrEF). One year of clinical follow-up. PLoS ONE. 2016;11:e0168790. doi: 10.1371/journal.pone.0168790. [DOI] [PMC free article] [PubMed] [Google Scholar]
166.Voorrips S.N., Boorsma E.M., Beusekamp J.C., DE-Boer R.A., Connelly M.A., Dullaart R.P.F., VAN-DER-Meer P., VAN-Veldhuisen D.J., Voors A.A., Damman K., et al. Longitudinal Changes in Circulating Ketone Body Levels in Patients with Acute Heart Failure: A Post Hoc Analysis of the EMPA-Response-AHF Trial. J. Card. Fail. 2023;29:33–41. doi: 10.1016/j.cardfail.2022.09.009. [DOI] [PubMed] [Google Scholar]
167.Nielsen R., Møller N., Gormsen L.C., Tolbod L.P., Hansson N.H., Sorensen J., Harms H.J., Frøkiær J., Eiskjaer H., Jespersen N.R., et al. Cardiovascular Effects of Treatment With the Ketone Body 3-Hydroxybutyrate in Chronic Heart Failure Patients. Circulation. 2019;139:2129–2141. doi: 10.1161/CIRCULATIONAHA.118.036459. [DOI] [PMC free article] [PubMed] [Google Scholar]
168.Kashiwaya Y., Sato K., Tsuchiya N., Thomas S., Fell D.A., Veech R.L., Passonneau J.V. Control of glucose utilization in working perfused rat heart. J. Biol. Chem. 1994;269:25502–25514. doi: 10.1016/S0021-9258(18)47278-X. [DOI] [PubMed] [Google Scholar]
169.Sato K., Kashiwaya Y., Keon C.A., Tsuchiya N., King M.T., Radda G.K., Chance B., Clarke K., Veech R.L. Insulin, ketone bodies, and mitochondrial energy transduction. FASEB J. 1995;9:651–658. doi: 10.1096/fasebj.9.8.7768357. [DOI] [PubMed] [Google Scholar]
170.Schugar R.C., Moll A.R., André d’Avignon D., Weinheimer C.J., Kovacs A., Crawford P.A. Cardiomyocyte-specific deficiency of ketone body metabolism promotes accelerated pathological remodeling. Mol. Metab. 2014;3:754–769. doi: 10.1016/j.molmet.2014.07.010. [DOI] [PMC free article] [PubMed] [Google Scholar]
171.Luong T.V., Abild C.B., Bangshaab M., Gormsen L.C., Søndergaard E. Ketogenic Diet and Cardiac Substrate Metabolism. Nutrients. 2022;14:1322. doi: 10.3390/nu14071322. [DOI] [PMC free article] [PubMed] [Google Scholar]
172.Matsuura T.R., Puchalska P., Crawford P.A., Kelly D.P. Ketones and the Heart: Meta-bolic Principles and Therapeutic Implications. Circ Res. 2023;132:882–898. doi: 10.1161/CIRCRESAHA.123.321872. [DOI] [PMC free article] [PubMed] [Google Scholar]
173.Likhodii S.S., Musa K., Mendonca A., Dell C., Burnham W.M., Cunnane S.C. Dietary fat, ketosis, and seizure resistance in rats on the ketogenic diet. Epilepsia. 2000;41:1400–1410. doi: 10.1111/j.1528-1157.2000.tb00115.x. [DOI] [PubMed] [Google Scholar]
174.Wang Y., Liu Z., Han Y., Xu J., Huang W., Li Z. Medium Chain Triglycerides enhances exercise endurance through the increased mitochondrial biogenesis and metabolism. PLoS ONE. 2018;13:e0191182. doi: 10.1371/journal.pone.0191182. [DOI] [PMC free article] [PubMed] [Google Scholar]
175.Cardoso D.A., Moreira A.S., de Oliveira G.M., Raggio Luiz R., Rosa G. A Coconut Extra Virgin Oil-Rich Diet Increases Hdl Cholesterol and Decreases Waist Circumference and Body Mass in Coronary Artery Disease Patients. Nutr. Hosp. 2015;32:2144–2152. doi: 10.3305/nh.2015.32.5.9642. [DOI] [PubMed] [Google Scholar]