Kirjallisuuskatsaus: ketogeenisen ruokavalion terveysvaikutukset osa 1 mikrobiomi
Kathryn Dowis, Simran Banga
Editor: Marcellino Monda;
Käännös ja editointi: Sami Raja-Halli
https://pmc.ncbi.nlm.nih.gov/articles/PMC8153354/
Tiivistelmä
Suosiotaan kasvattavan ketogeenisen ruokavalion (KD) vaikutuksista terveyteen ei ole tehty kattavaa tutkimuskatsausta. Tämä kirjallisuuskatsaus kokoaa yhteen tutkimuksia ketogeenisen ruokavalion vaikutuksista mikrobiomiin, epigenomiin, diabeteksen hoitoon, laihtumiseen, sydän- ja verisuoniterveyteen sekä alttiuteen sairastua syöpään. Tämä ensimmäinen osa käsittelee mikrobiomia.
KD voi lisätä mikrobiomin geneettistä monimuotoisuutta ja bakteroidien määrää suhteessa firmikuutteihn. Firmikuutit on bakteerien pääjakso, johon kuuluu kolme luokkaa ( bacillus, listeria ja staphylococcus) ja yli 250 bakteerisukua.
KD vaikuttaa suotuisasti epigenomiin, koska se luo signaloivan molekyylin, joka tunnetaan nimellä β-hydroksibutyraatti (BHB).
KD on auttanut diabetesta sairastavia potilaita laskemaan HbA1c:tä ja vähentämään insuliinin tarvetta. On myös näyttöä siitä, että KD on erinomainen ruokavalio painonhallinnassa. Tutkimusten mukaan KD vähentää sisäelinten rasvoittumista/ viskeraalista rasvaa ja auttaa ruokahalun hallinnassa.
Tutkimukset viittaavat siihen, että runsasrasvainen ruokavalio parantaa lipidiprofiileja laskemalla LDL-kolesterolia, lisäämällä HDL-kolesterolia ja vähentämällä triglyseridejä (TG).
Warburg-vaikutteen* avulla KD:tä käytetään adjuvanttihoitona syöpäsolujen nälkiinnyttämiseen, mikä tekee syöpäsoluista alttiimpia kemoterapialle ja säteilyhoidolle. KD:n mahdolliset positiiviset vaikutukset kullakin näistä alueista edellyttävät lisäanalyysejä, parempia tutkimuksia ja hyvin suunniteltuja satunnaistettuja kontrolloituja tutkimuksia, joilla voidaan edelleen valaa tämän ruokavalion tarjoamia terapeuttisia mahdollisuuksia.
*Warburg-ilmiö lyhyestiOtto Warburg havaitsi 1920-luvulla, että syöpäsolut tuottavat energiaa eri tavalla kuin terveet solut. Terveet solut käyttävät ensisijaisesti happea energian tuottamiseen, kun taas syöpäsolut suosivat anaerobista glykolyysiä eli sokerin hajottamista ilman happea. Tämä ilmiö on nimetty hänen mukaansa Warburg-ilmiöksi. Ketogeenisen ruokavalion vaikutus syöpäsoluihin:
|
1. Johdanto
Ketoosi saavutetaan rajoittamalla hiilihydraattien saantia, kohtuullistamalla proteiinin kulutusta ja lisäämällä rasvasta saatujen kalorien määrää [1].
Hiilihydraattien rajoittaminen ohjaa elimistön glukoosiaineenvaihduntasta rasva-aineenvaihduntaan. Rasva ja ketoaineet korvaavat hiilihydraateista saatavan glukoosin ensisijaisena energianlähteenä. Sokereiden rajoittaminen vie aineenvaihdunnan tilaan, jossa keho käyttää rasvaa ensisijaisena polttoaineena. Ketogeenisellä ruokavaliolla aineenvaihdunta ohjataan polttamaan rasvasoluihin varastoitua rasvaa energiaksi.
|
Viimeisimmät ketogeenistä ruokavaliota seuraavat ravitsemustutkimukset ovat antaneet lupaavia tuloksia:
|
Havaintojen mukaa ketogeeninen ruokavalio tehostaa eräitä syöpähoitoja ja parantaa syövän ennustetta. Lue ketogeenisestä ruokavaliosta syövän terapiana.
KD parantaa solujen terveyttä autofagiana tunnetun soluja puhdistavan ja uusivan mekanismin seurauksena. Betahydroksibutyraatin roolia aivosolujen toiminnan tehostajana tutkitaan mm. Yhdysvaltojen puolustusministeriössä ja NASA:ssa. [2, 3]
Lihavuudesta, aikuistyypin diabeteksesta ja metabolisesta oireyhtymästä kärsivien ihmisten määrä on globaalisti kasvussa. Metabolisen oireyhtymän yleisiä merkkejä ovat keskivartalolihavuus, insuliiniresistenssi, korkea verenpaine, kohonneet triglyseriditasot ja verenpainetauti. [4,5]
Edellä listatut kardiometaboliset oireet lisäävät sydän- ja verisuonitautien, diabeteksen, aivohalvauksen ja Alzheimerin taudin riskiä. WebMD:n mukaan USA:ssa on tällä hetkellä 27 miljoonaa tyypin 2 diabetesta sairastavaa. 86 miljoonaalla amerikkalaisella on esidiabetes. CDC arvioi, että lähes 40 prosenttia amerikkalaisista aikuisista ja noin 20 prosenttia lapsista on lihavia. [6,7].
Eräät tutkijat ovat argumentoineet, että nämä sairaudet ovat seurausta hiilihydraatti-intoleranssista ja insuliiniresistenssistä. Ruokavalio, joka vähentää altistusta hiilihydraateille (mukaan lukien täysjyväviljat), voi olla painonhallinnan ja terveyden kannalta suotuisa. [8]
Terveysvaikutusten osalta tutkimusraportissa seurataan kahta ruokavaliota: tavallista ketogeenistä ruokavaliota ja terapeuttista ketogeenistä ruokavaliota (kuva 1). Molemmat ruokavaliot rajoittavat hiilihydraattien saantia vaihtelevassa määrin. Terapeuttista ketogeenistä ruokavaliota, joka rajoittaa merkittävästi sekä hiilihydraatteja että proteiinia, käytetään myö epilepsian ja eräiden syöpien hoidossa.
Amerikkalaisten ravitsemusohjeiden mukaan 45-65 % päivittäisestä energiasta pitäisi saada hiilihydraateista, eli sokereista (kuva1). Henkilöllä, joka kuluttaa 2000 kilokaloria päivässä, määrä vastaa 225-325 g hiilihydraatteja. [9].
Kuvateksti: Vertailu tavallisen amerikkalaisen ruokavalion, terapeuttisen KD:n ja perinteisen ketogeenisen ruokavalion makroravinteiden suhteellisista osuuksista. Terapeuttista ketogeenistä ruokavaliota käytetään joskus epilepsia- ja syöpähoitojen osana.
Vähähiilihydraattinen/runsasrasvainen ruokavalio on valtavirtaistumassa. Karppaamisen, eli LCHF-ruokavalion ja vähähiilihydraattisen ketogeenisen ruokavalion (LCKD) välillä on eroja.
Ketoosi saavutetaan yleensä joko paastoamisella tai hiilihydraattien huomattavalla rajoittamisella. Vähähiilihydraattinen ruokavalio viittaa tyypillisesti ruokavalioon, jossa hiilihydraattien saanti on 50-150 g päivässä. Vaikka LCHF sisältää vähemmän hiilihydraatteja kuin ravintosuositukset, se ei laske hiilihydraattien saantia tarpeeksi aineenvaihdunnan ohjaamiseksi ketoosiin.
Hiilihydraattien päivittäisen saannin rajoittaminen 20-50 grammaan johtaa siihen, että solut eivät saa riittävästi energiaa glukoosista, jolloin aineenvaihdunnan on pakko siirtyä varajärjestelmään – eli polttamaan energiaksi kehon varastoimaa läskiä. [10].
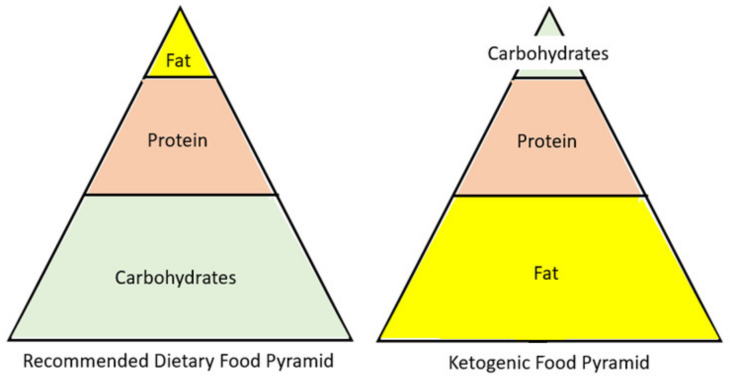
Ketogeeninen ruokavalio kääntää tutun ruokapyramidin ylösalaisin. Runsaasti hiilihydraatteja sisältävän ruokavalion sijaan KD sisältää runsaasti rasvaa (Kuva2). Hiilihydraattirajoitus alentaa veren glukoosipitoisuutta. Myöhemmät insuliinipitoisuuden muutokset ohjaavat kehoa siirtymään rasvan säilyttämisen ja varastoimisen tilasta rasvan polttamiseen. Rasvassa on 2,5 x enemmän energiaa kuin hiilihydraateissa, joten runsaasti rasvaa sisältävä ruokavalio pitää hyvin nälän kurissa ehkäisten rajuja verensokeri- ja insuliinipiikkejä. [10].
Kun hiilihydraatit (sokerit) korvataan rasvalla, ketoaineiden tuotanto (ketogeneesi) käynnistyy. Ketogeneesi muodostaa maksassa eräistä aminohapoista ja sitruunahappokierron lopputuotteista asetonia, asetoasetaataattia ja β-hydroksibutyraattia, joita lähes kaikki elimistön solut pystyvät käyttämään energianlähteinä. Poikkeuksena on veren punasolut ja eräät hermosolut, joilta puuttuu mitokondriot; ne tarvitsevat välttämättä ravinnokseen glukoosia. Aineenvaihdunta osaa kuitenkin syntetisoida kaiken tarvitsemansa glukoosin glukoneogeneesissä. [11]
Tutkimukset viittaavat siihen, että β-hydroksibutyraatti toimii signaalimolekyylinä jolla voi olla rooli ruokahalun tukahduttamisessa. [12]
Kuvateksti: Vertailu ravintosuositusten ruokapyramidista, ml. tärkeimmät makroravinteet (hiilihydraatit, proteiinit, rasvat), ketogeenisen ruokavalion ruokapyramidiin.
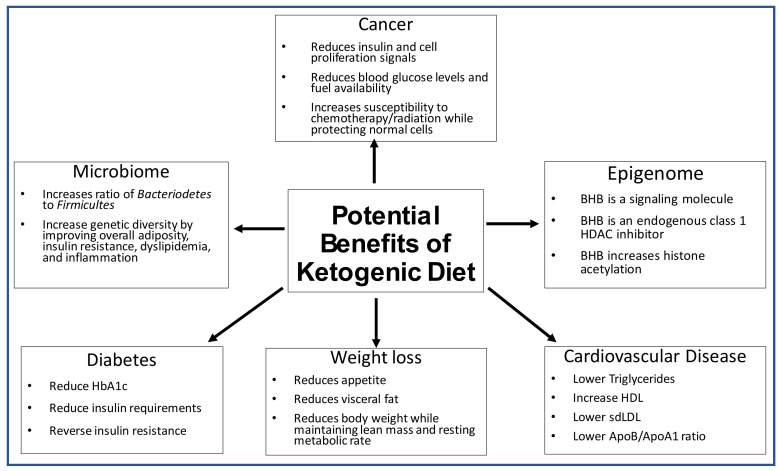
Käytettävissä olevissa tiedoissa on jonkin verran epäyhtenäisyyttä. Tämän tarkastelun tavoitteena on korostaa ketogeenisen ruokavalion roolia mikrobiomin, epigeneettisten tekijöiden, laihtumisen, diabeteksen, sydän- ja verisuonitautien sekä syövän suhteen. (Kuva 3).
Kuva3.
Ketogeenisen ruokavalion mahdolliset terapeuttiset vaikutukset mikrobiomiin, epigenomiin, diabeteksen lääkkeettömään hoitoon, laihduttamiseen ja sydän- ja verisuonitauteihin.
2. Ketogeenisen ruokavalion vaikutus mikrobiomiin
Mikrobiomin biljoonat mikroskooppiset organismit kolonisoivat ruoansulatuskanavan ja suoliston. Mikrobiomi koostuu yli 8000 erityyppisestä bakteerista, arkista, viruslajista ja sienestä, jotka elävät monimutkaisessa ekosysteemissä. Ihmisen ja mikrobiomin suhde on mutualistinen – molempia hyödyttävä. [13]
| Ihminen muodostaa normaalimikrobistonsa kanssa superorganismin, jossa ihmissoluja on vain 10 %. Iholla ja limakalvoilla elää 1014 mikrobi-lajia, valtaosa ruoansulatuskanavan loppupäässä, jossa ne aineenvaihdunnallisesti aktiivisena, lähinnä bakteereista koostuvana noin 1,5 kilon painoisena solumassana muodostavat monimuotoisen dynaamisen ekosysteemin. Suolistomikrobiston koostumusta on tutkittu toistaiseksi laajimmin nukleiinihappopohjaisilla menetelmillä, ja lajitason monimuotoisuudeksi on arvioitu 1 200- 16 000 bakteerifylotyyppiä. Suolistomikrobien tiedetään vaikuttavan ihmisen fysiologiaan, immuunipuolustuksen kehittymiseen, kolonisaatioresistenssiin ja ravitsemukseen. Uudet tutkimusmenetelmät ja globaali tutkimuskenttä ovat kuitenkin paljastamassa suolistomikrobien laajempaa merkitystä terveydelle esimerkiksi mikrobiston muutosten liittymistä tulehduksellisiin suolistosairauksiin, ärtyvän paksusuolen oireyhtymään, paksusuolisyöpään, lihavuuteen ja tyypin 2 diabetekseen. Duodecim |
Miksi mikrobiomi on niin tärkeä?
- Ruoansulatus:Suolistossa elävä mikrobisto auttaa meitä hajottamaan ruokaa ja imemään ravinteita. Se tuottaa myös vitamiineja ja muita ravintoaineita, joita elimistömme tarvitsee.
- Immuunijärjestelmä:Mikrobiomi kouluttaa immuunijärjestelmämme erottamaan haitalliset bakteerit hyödyllisistä. Se auttaa myös suojaamaan meitä infektioilta.
- Aineenvaihdunta:Mikrobit vaikuttavat aineenvaihduntamme monin tavoin. Ne voivat esimerkiksi vaikuttaa painoon, verensokerin säätelyyn ja jopa mielialaan.
- Hermosto:Suolisto-aivo-akselin kautta mikrobit vaikuttavat aivojen toimintaan. On havaittu yhteyksiä suolistomikrobiston ja esimerkiksi ahdistuksen, masennuksen sekä neurodegeneratiivisten sairauksien välillä.
Viimeaikaiset tutkimukset viittaavat siihen, että elintavat, kuten riittävä uni, liikunta, ruokavalio ja antibiootit vaikuttavat mikrobiomin geneettiseen koostumukseen. Mikrobiomi osallistuu ravinnon hyödyntämiseen tuottaen aineenvaihduntatuotteina mm. hyödyllisiä lyhytketjuisia rasvahappoja, eräitä vitamiineja ja serotoniinia*.
|
*Miten suolisto tuottaa serotoniinia?
Miksi suoliston serotoniini on tärkeä?
|
Ruoansulatuskanavan ja suoliston bakteerit, arkit ja sienet vaikuttavat ravintolähteiden aineenvaihduntaan. Erilaisilla bakteereilla on erilaisia kykyjä hyödyntää ravintoa. Vaikutus havaitaan esimerkiksi postprandiaalisessa (aterianjälkeisessä) glukoosivasteessa (PPGR). [13]
Verensokerin homeostaasista huolehtiminen vähentää monien aineenvaihduntasairauksien, kuten diabeteksen ja lihavuuden riskiä. Weizmann-instituutissa tehty tutkimus osoitti, että matemaattista algoritmia voidaan soveltaa yksilön mikrobiomiprofiilin määrittämisessä ja tämän glykeemisen vasteensa ennustamiseen. Yksilön glykeemistä vastetta erilaisiin elintarvikkeisiin voidaan hyödyntää yksilöllisen ruokavalion suunnittelussa. Tulokset vahvistettiin Mayo-klinikalla. [13, 14].
Mikrobiomilla on merkittävä rooli ihmisten terveydelle. Se rakentuu erityisesti ympäristötekijöiden vaikutuksesta. Rothschild et al. tekemän tutkimuksen mukaan., suoliston mikrobiomin periytyvyys on vain 1,9%, kun taas yli 20 prosenttia vaihtelevuudesta liittyi ruokavalioon ja elämäntapaan. [15]
Tutkimus, jossa tutkittiin prebioottisten elintarvikkeiden, kuten inuliinin ja oligosakkaridien etuja, havaittiin, että bifidobakteerien määrä lisääntyminen paksusuolessa kasvatti muiden butyraattia tuottavien bakteerien osuutta mikrobiomissa. [16]
Toisessa tutkimuksessa havaittiin, että suoliston mikrobiomin monimuotoisuuteen vaikutti enemmän länsimainen ruokavalio kuin koehenkilöiden painoindeksi. Länsimaisia ruokavalioita noudattaneiden henkilöiden suolistossa huonot mikrobit (firmikuutit) lisääntyivät ja vastaavasti hyödyllisten bakteroidien kannat pienenivät. [17]
Tutkimuskatsauksessa raportoitiin positiivisia muutoksia suoliston mikrobiomissa ja yleisessä terveydessä henkilöillä, jotka noudattivat energiaa rajoittavaa ruokavaliota sekä ruokavalioissa, jotka sisälsivät runsaasti kuitua ja kasviksia. [18]
Runsaasti prosessoitua ruokaa syömällä ihmiset vähentävät mikrobiomin monimuotoisuutta, kun taas runsaasti hedelmiä ja vihanneksia sisältävä ruokavalio lisää monimuotoisuutta suoliston mikrobiomissa [19].
Suoliston mikrobiomit, joista puuttui geneettinen monimuotoisuus, liittyivät lihavuuteen, insuliiniresistenssiin, dyslipidemiaan ja tulehdukselliseen fenotyyppiin. [20]
Vaikuttaako ketogeeninen ruokavalio positiivisesti tai negatiivisesti mikrobiomin lajiston monimuotoisuuteen?
Jotkut tutkimukset ovat osoittaneet, että täysjyväviljalla on keskeinen rooli terveen mikrobiomin kehittämisessä ja ne ovat välttämättömiä hyvän terveyden kannalta. Saako ketogeenistä ruokavaliota noudattava henkilö tarpeeksi täysjyvätuotteita terveellisen mikrobiomin ylläpitämiseksi? [12, 21]
Adam-Perrot et al. mukaan vähähiilihydraattisilla ruokavalioilla on riski olla ravitsemuksellisesti riittämättömiä kuidun, välttämättömien vitamiinien, kivennäisaineiden ja raudan saannin osalta. Tämä tulkinta perustuu yleisesti suositeltujen ruokavalioiden analyysiin ja tutkimuksiin, jotka on tehty välttämättömien ravintoaineiden saannin määrittämiseksi samalla kun kulutetaan vaihtelevia määriä hiilihydraatteja [12, 22].
Suolistomikrobiomin terveyden kannalta on tärkeää, että ketogeenistä ruokavaliota noudattavat ihmiset suosivat sellaisia vähähiilihydraattisia ravintoaineita, jotka sisältävät kuitua. Lisäksi ketogeenisessa ruokavalion tulee sisältää kohtuullisesti proteiineja (n. 1,5g/painokilo/päivä). [23]
Jos ketogeeniseen ruokavalioon sisältyy punaista lihaa ja sisäelimiä kuten maksaa, ruokavalio turvaa riittävä raudan saannin. Vihreiden kasvisten, kuten pinaatin ja parsakaalin, pähkinöiden, marjojen ja resistenttiä tärkkelystä* sisältävien kasvisten saanti ylläpitää terveellistä suoliston mikrobiomia. [23]
Resistentti tärkkelys: Ravintokuitu, joka ruokkii hyviä bakteereja
Resistentti tärkkelys on siinä mielessä erikoislaatuinen hiilihydraatti, että se ei imeydy ohutsuolessa samalla tavalla kuin tavallinen tärkkelys. Sen sijaan se kulkeutuu paksusuoleen, jossa se toimii ravintona suoliston hyödyllisille bakteereille. Tämä tekee siitä erittäin arvokkaan ravintokuidun.
*Miten resistentti tärkkelys vaikuttaa mikrobiomiin?
Resistentin tärkkelyksen lähteetResistenttiä tärkkelystä löytyy monista luonnollisista elintarvikkeista. Sen määrä voi vaihdella ruoan valmistustavasta ja kypsyysasteesta riippuen. Hyviä lähteitä ovat muun muassa:
Resistentin tärkkelyksen hyödyt terveydelle
Resistentti tärkkelys on tärkeä osa terveellistä ruokavaliota. Se on luonnollinen tapa ruokkia suoliston hyviä bakteereja ja edistää näin yleistä terveyttä. Lisäämällä resistentin tärkkelyksen saantia ruokavaliossa voit tukea suoliston hyvinvointia ja vähentää riskiä moniin sairauksiin. |
Ketogeenisen ruokavalion pitkäaikaiset vaikutukset mikrobiomiin
Tällä hetkellä tutkijoilla ei ole tietoa ketogeenisen ruokavalion pitkäaikaisista vaikutuksista suoliston mikrobiomiin.
Eri tutkimuksiin perustuen tutkijat uskovat, että KD vaikuttaa positiivisesti mikrobiomiin lisäämällä batteriets- ja bifidobakteerilajeja, jotka yhdistetään parempaan terveyteen ja sellaisten mikrobilajien vähenemiseen, joiden tiedetään lisäävän terveysriskejä.
Epileptiaa sairastavien imeväisten heikentynyt mikrobiomi parani viikon ketogeenisellä ruokavaliolla. Ketogeeninen ruokavalio kasvatti mikrobiomin bakteerimäärää ~24%. Eräässä 6 kuukauden tutkimuksessa havaittiin, että kohenkilöiden refraktoristen epilepsialääkkeiden tarve väheni merkittävästi; mikrobiomin bakteerit lisääntyivät, mutta sen monimuotoisuus väheni. [24, 25]
Joidenkin tutkimusten mukaan firmikuuttien vähäinen määrä suhteessa bakteroideihin indikoi tervettä suolistomikrobiomia. Näistä tutkimuksista kerättyjen havaintojen perusteella lihavilla on todennäköisesti enemmän firmikuutteja suhteessa hyödyllisten bakteroidien määrään kuin hoikilla. Lihavien ulosteesta mitattiin myös hoikkien näytteitä korkeampia lyhytketjuisten rasvahappojen (SCFA) pitoisuuksia. Lihavilla todettiin bakteroidien lisääntymistä firmikuuttitasojen pysyessä ennallaan. Tutkimukset viittaavat siihen, että llaihtuminen ketogeenisellä ruokavaliolla johtaa positiivisiin muutoksiin mikrobiomissa. [5, 26, 27, 28]
Basciani et al. analysoi suoliston mikrobiomin muutoksia lihavilla insuliiniresistentillä potilailla, jotka noudattivat ketogeenisiä ruokavalioita vaihtelevilla energiamäärillä ja proteiinilähteillä. Vähäenergiset ketogeeniset ruokavaliot (VLCKD) sisälsivät vehnä-, kasvi- tai eläinproteiineja. Kaikissa seurantaryhmissä havaittiin 45 päivän jälkeen hyödyllisiä muutoksia, joissa firmikuuttien suhteellinen osuus mikrobiomissa oli vähentynyt ja hyvien bakteerikantojen osuus lisääntynyt. Muutos ei kuitenkaan ollut yhtä selvä eläinproteiineja saaneessa seurantaryhmässä. [29, 30]
Muutamassa lyhytaikaisessa tutkimuksessa verrattiin KD:n vaikutuksia tutkittavien mikrobiomiin. Nagpal et al. analysoi modifioidun välimeren ketogenisen ruokavalion (MMKD) ja American Heart Association Diet (AHAD) -ruokavalion vaikutuksia normaalin kognition ja lievän kognitiivisen häiriön potilailla. Modifioitu välimeren ketogeeninen ruokavalio ei tuottanut merkittäviä muutoksia Firmicutes- tai Bacteroides-kannoissa 6 viikon seurantajaksolla. Bifidobacteriaceae-perheen mikrobit sen sijaan vähenivät ja Verrucomicrobiaceae-perheen mikrobit lisääntyivät. Tätä pidettiin positiivisena muutoksena. Lisäksi hyödyllinen SCFA – butyraatti lisääntyi MMKD:ssä. Butyraatin tiedetään indikoivan suoliston terveyttä. [31].
Summa summarum: Miten mikrobiomi voi vaikuttaa terveyteen?
Mikrobiomin epätasapaino, eli dysbioosi, voi aiheuttaa/pahentaa erilaisia terveysongelmia. Esimerkiksi:
- Suolistosairaudet: Crohnin tauti, ärtyvän suolen oireyhtymä
- Aineenvaihduntasairaudet: Lihavuus, diabetes
- Ihosairaudet: Atooppinen ihottuma, psoriaasi
- Mielenterveyshäiriöt: Ahdistus, masennus, autismi
- Autoimmuunisairaudet: Reuma, MS-tauti
Miten voimme huolehtia mikrobiomistamme?
- Monipuolinen ruokavalio: Syö runsaasti kuituja sisältäviä kasviksia, hedelmiä ja täysjyvätuotteita. Probiootit, kuten jogurtti ja kefiiri, voivat myös olla hyödyllisiä.
- Riittävä uni: Uni on tärkeä palautumisen kannalta, ja se vaikuttaa myös suolistomikrobiston toimintaan.
- Liikunta: Liikunta edistää suoliston toimintaa ja voi parantaa mikrobiston monimuotoisuutta.
- Stressinhallinta: Stressi voi häiritä suolistomikrobiston toimintaa. Rentoutumiskeinot, kuten meditaatio ja jooga, voivat auttaa.
- Antibioottien harkittu käyttö: Antibiootit voivat tuhota mikrobiomia, joten niitä tulee käyttää vain tarpeen mukaan.
Lähteet
- 1.Moore J., Westman E.C. Keto Clarity: Your Definitive Guide to the Benefits of a Low-Carb, High-Fat Diet. Victory Belt Publishing Inc.; Las Vegas, NV, USA: 2020. [Google Scholar]
- 2.Hallberg S.J., McKenzie A.L., Williams P.T., Bhanpuri N.H., Peters A.L., Campbell W.W., Hazbun T.L., Volk B.M., McCarter J.P., Phinney S.D., et al. Effectiveness and Safety of a Novel Care Model for the Management of Type 2 Diabetes at 1 Year: An Open-Label, Non-Randomized, Controlled Study. Diabetes Ther. 2018;9:583–612. doi: 10.1007/s13300-018-0373-9. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 3.Edwards C., Canfield J., Copes N., Rehan M., Lipps D., Bradshaw P.C. D-beta-hydroxybutyrate extends lifespan in C. elegans. Aging. 2014;6:621–644. doi: 10.18632/aging.100683. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 4.Longo V.D., Mattson M.P. Fasting: Molecular Mechanisms and Clinical Applications. Cell Metab. 2014;19:181–192. doi: 10.1016/j.cmet.2013.12.008. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 5.Den Besten G., van Eunen K., Groen A.K., Venema K., Reijngoud D.J., Bakker B.M. The role of short-chain fatty acids in the interplay between diet, gut microbiota, and host energy metabolism. J. Lipid Res. 2013;54:2325–2340. doi: 10.1194/jlr.R036012. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 6.Fryar C.D., Carroll M.D., Afful J. Prevalence of Overweight, Obesity, and Severe Obesity among Adults Aged 20 and over: United States, 1960–1962 through 2017–2018. NCHS Health; Hyattsville, MD, USA: 2020. [(accessed on 12 May 2021)]. E-Stats. Available online: https://www.cdc.gov/nchs/data/hestat/obesity-adult-17-18/obesity-adult.htm. [Google Scholar]
- 7.Fryar C.D., Carroll M.D., Afful J. Prevalence of Overweight, Obesity, and Severe Obesity among Children and Adolescents Aged 2–19 Years: United States, 1963–1965 through 2015–2016. NCHS Health; Hyattsville, MD, USA: 2020. [(accessed on 12 May 2021)]. E-Stats. Available online: https://www.cdc.gov/nchs/data/hestat/obesity_child_15_16/obesity_child_15_16.htm. [Google Scholar]
- 8.Westman E.C., Yancy W.S., Mavropoulos J.C., Marquart M., McDuffie J.R. The effect of a low-carbohydrate, ketogenic diet versus a low-glycemic index diet on glycemic control in type 2 diabetes mellitus. Nutr. Metab. 2008;5:36. doi: 10.1186/1743-7075-5-36. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 9.Abbasi J. Interest in the Ketogenic Diet Grows for Weight Loss and Type 2 Diabetes. JAMA. 2018;319:215–217. doi: 10.1001/jama.2017.20639. [DOI] [PubMed] [Google Scholar]
- 10.Westman E.C., Feinman R.D., Mavropoulos J.C., Vernon M.C., Volek J.S., Wortman J.A., Yancy W.S., Phinney S.D. Low-carbohydrate nutrition and metabolism. Am. J. Clin. Nutr. 2007;86:276–284. doi: 10.1093/ajcn/86.2.276. [DOI] [PubMed] [Google Scholar]
- 11.Paoli A. Ketogenic Diet for Obesity: Friend or Foe? Int. J. Environ. Res. Public Health. 2014;11:2092–2107. doi: 10.3390/ijerph110202092. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 12.Adam-Perrot A., Clifton P., Brouns F. Low-carbohydrate diets: Nutritional and physiological aspects. Obes. Rev. 2006;7:49–58. doi: 10.1111/j.1467-789X.2006.00222.x. [DOI] [PubMed] [Google Scholar]
- 13.Wallace C. Dietary advice based on the bacteria in your gut. 2018 February 25. Wall Street Journal. [(accessed on 12 May 2021)]; Available online: https://www.wsj.com/articles/dietary-advice-based-on-the-bacteria-in-your-gut-1519614301.
- 14.Zeevi D., Korem T., Zmora N., Israeli D., Rothschild D., Weinberger A., Ben-Yacov O., Lador D., Avnit-Sagi T., Lotan-Pompan M., et al. Personalized Nutrition by Prediction of Glycemic Responses. Cell. 2015;163:1079–1094. doi: 10.1016/j.cell.2015.11.001. [DOI] [PubMed] [Google Scholar]
- 15.Rothschild D., Weissbrod O., Barkan E., Kurilshikov A., Korem T., Zeevi D., Costea P.I., Godneva A., Kalka I.N., Bar N., et al. Environment dominates over host genetics in shaping human gut microbiota. Nature. 2018;555:210–215. doi: 10.1038/nature25973. [DOI] [PubMed] [Google Scholar]
- 16.Rivière A., Selak M., Lantin D., Leroy F., De Vuyst L. Bifidobacteria and Butyrate-Producing Colon Bacteria: Importance and Strategies for Their Stimulation in the Human Gut. Front. Microbiol. 2016;7:979. doi: 10.3389/fmicb.2016.00979. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 17.Davis S.C., Yadav J.S., Barrow S.D., Robertson B.K. Gut microbiome diversity influenced more by the Westernized dietary regime than the body mass index as assessed using effect size statistic. Microbiologyopen. 2017;6:e00476. doi: 10.1002/mbo3.476. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 18.Lynch S.V., Pedersen O. The Human Intestinal Microbiome in Health and Disease. N. Engl. J. Med. 2016;375:2369–2379. doi: 10.1056/NEJMra1600266. [DOI] [PubMed] [Google Scholar]
- 19.Claesson M.J., Jeffery I.B., Conde S., Power S.E., O’Connor E.M., Cusack S., Harris H.M.B., Coakley M., Lakshminarayanan B., O’Sullivan O., et al. Gut microbiota composition correlates with diet and health in the elderly. Nature. 2012;488:178–184. doi: 10.1038/nature11319. [DOI] [PubMed] [Google Scholar]
- 20.Gerhauser C. Impact of dietary gut microbial metabolites on the epigenome. Philos. Trans. R. Soc. B Biol. Sci. 2018;373:20170359. doi: 10.1098/rstb.2017.0359. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 21.Gong L., Cao W., Chi H., Wang J., Zhang H., Liu J., Sun B. Whole cereal grains and potential health effects: Involvement of the gut microbiota. Food Res. Int. 2018;103:84–102. doi: 10.1016/j.foodres.2017.10.025. [DOI] [PubMed] [Google Scholar]
- 22.Kennedy E.T., A Bowman S., Spence J.T., Freedman M., King J. Popular Diets. J. Am. Diet. Assoc. 2001;101:411–420. doi: 10.1016/S0002-8223(01)00108-0. [DOI] [PubMed] [Google Scholar]
- 23.Miller V.J., Villamena F.A., Volek J.S. Nutritional Ketosis and Mitohormesis: Potential Implications for Mitochondrial Function and Human Health. J. Nutr. Metab. 2018;2018:5157645. doi: 10.1155/2018/5157645. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 24.Xie G., Zhou Q., Qiu C.-Z., Dai W.-K., Wang H.-P., Li Y.-H., Liao J.-X., Lu X.-G., Lin S.-F., Ye J.-H., et al. Ketogenic diet poses a significant effect on imbalanced gut microbiota in infants with refractory epilepsy. World J. Gastroenterol. 2017;23:6164–6171. doi: 10.3748/wjg.v23.i33.6164. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 25.Zhang Y., Zhou S., Zhou Y., Yu L., Zhang L., Wang Y. Altered gut microbiome composition in children with refractory epilepsy after ketogenic diet. Epilepsy Res. 2018;145:163–168. doi: 10.1016/j.eplepsyres.2018.06.015. [DOI] [PubMed] [Google Scholar]
- 26.Ley R.E., Turnbaugh P.J., Klein S., Gordon J.I. Microbial ecology: human gut microbes associated with obesity. Nature. 2006;444:1022–1023. doi: 10.1038/4441022a. [DOI] [PubMed] [Google Scholar]
- 27.Turnbaugh P.J., Ley R.E., Mahowald M.A., Magrini V., Mardis E.R., Gordon J.I. An obesity-associated gut microbiome with increased capacity for energy harvest. Nat. Cell Biol. 2006;444:1027–1031. doi: 10.1038/nature05414. [DOI] [PubMed] [Google Scholar]
- 28.Ley R.E., Bäckhed F., Turnbaugh P., Lozupone C.A., Knight R.D., Gordon J.I. Obesity alters gut microbial ecology. Proc. Natl. Acad. Sci. USA. 2005;102:11070–11075. doi: 10.1073/pnas.0504978102. [DOI] [PMC free article] [PubMed] [Google Scholar]
- 29.Schwiertz A., Taras D., Schaefer K., Beijer S., Bos N.A., Donus C., Hardt P.D. Microbiota and SCFA in Lean and Overweight Healthy Subjects. Obesity. 2010;18:190–195. doi: 10.1038/oby.2009.167. [DOI] [PubMed] [Google Scholar]
- 30.Basciani S., Camajani E., Contini S., Persichetti A., Risi R., Bertoldi L., Strigari L., Prossomariti G., Watanabe M., Mariani S., et al. Very-Low-Calorie Ketogenic Diets with Whey, Vegetable, or Animal Protein in Patients With Obesity: A Randomized Pilot Study. J. Clin. Endocrinol. Metab. 2020;105:2939–2949. doi: 10.1210/clinem/dgaa336. [DOI] [PubMed] [Google Scholar]
- 31.Nagpal R., Neth B.J., Wang S., Craft S., Yadav H. Modified Mediterranean-ketogenic diet modulates gut microbiome and short-chain fatty acids in association with Alzheimer’s disease markers in subjects with mild cognitive impairment. EBioMedicine. 2019;47:529–542. doi: 10.1016/j.ebiom.2019.08.032. [DOI] [PMC free article] [PubMed] [Google Scholar]