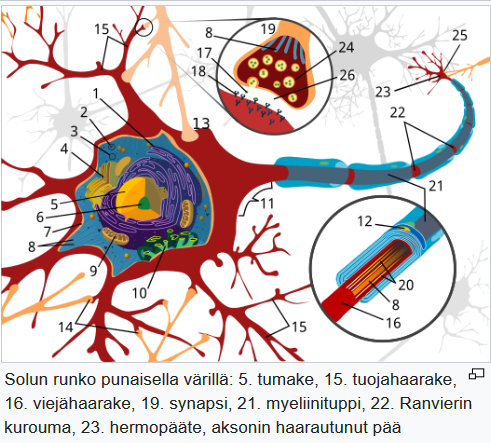
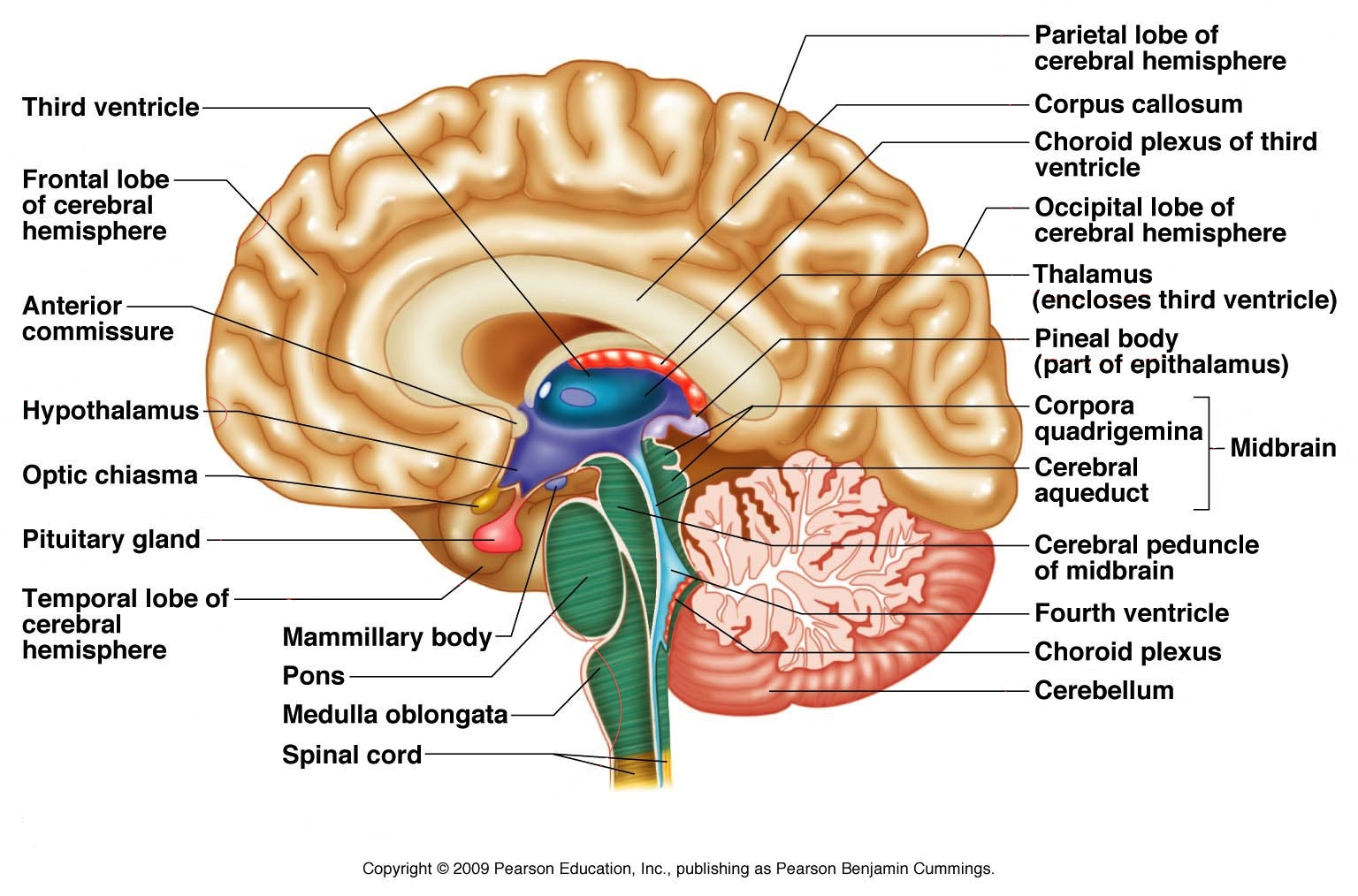
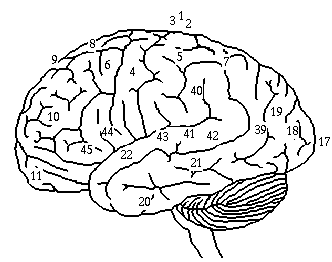
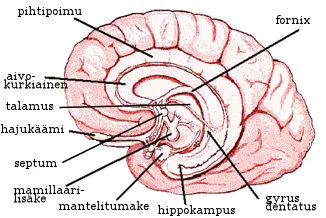
Infektiot ja autoimmuunitaudit osa 1
The Role of infections in autoimmune disease: A M Ercolini ja S D Miller (1)
Kääntänyt ja kommentoinut: Sami Raja-Halli
Saatteeksi
Jopa lievät ja oireettomat mikrobi-infektiot voivat laukaista autoimmuunitaudin tai muuttaa solujen proteiinisynteesiä ja DNA:ta niin, että soluista tulee pahanlaatuisia syöpäsoluja. Minua surettaa koronainfektioon liittyvä vähättelevä ja piittaamaton asenne. Sairastan etenevää MS-tautia, jonka saattoi laukaista aikuisena sairastamani mononukleoosi tai jokin muu infektio. Tutkimukset vahvistavat, että MS-taudille altistumiseen vaikuttaa 100-200 geeniä, alhaiset sikiöaikaiset D-vitamiinitasot sekä yksi tai useampi autoimmuunitaudin laukaiseva ympäristötekijä.
Yleistä mononukleoosia (rauhaskuume, pusutauti) aiheuttava Epstein-Barrin virus assosioituu vahvasti MS-tautiin. Se on yksi MS-taudin puhkeamiseen vaikuttava ympäristötekijä. Useimmat lapset sairastavat pusutaudin oireettomana tai lievänä ennen viidettä ikävuottaan. Vanhempana sairastettu rauhaskuume voi olla oireiltaan ja jälkitaudeiltaan vakavampi.
|
Mononukleoosi on viruksen aiheuttama kuumetauti, johon aikuisilla liittyy useimmiten nielurisatulehdus ja yleinen imusolmukkeiden suureneminen sekä oireeton maksatulehdus. Pikkulapsilla taudin ainoat oireet ovat usein kuume ja suurentuneet imusolmukkeet (”rauhaset”) kaulalla. Taudin aiheuttaa Epstein–Barrin virus (EBV), joka siirtyy ihmisestä toiseen syljen välityksellä. Lähes kaikki suomalaiset saavat EBV-tartunnan. Puolet saa tartunnan ennen viidettä ikävuotta, oletettavasti vanhemmiltaan. Toinen tartuntojen vilkas kausi on nuori aikuisuus, jolloin ainakin suutelu levittää virusta. – Terveyskirjasto Duodecim |
Epstein-Barr ja MS-tauti
Herpesvirusten perheeseen kuuluva EBV on yksi yleisimmistä ihmisten välillä leviävistä viruksista. Lähes kaikki altistuvat sille jossain elämänvaiheessa. Lapsilla EBV ei välttämättä aiheuta oireita, mutta aikuisena sairastettu EB-viruksen aiheuttama mononukleoosi voi aiheuttaa vakaviakin oireita.
EBV voi aktivoida HERV-W/MSRV-retroviruksen mononukleoosia sairastavilla. Tämä aktivaatio liittää EB-viruksen MS-taudin patogeneesiin.
Kaksi endogeenistä HERV-W-perheen retrovirusta altistavat MS-taudille:
(1) MS-assosioitunut retrovirus (MSRV) ja (2) ERVWE1, joiden env-proteiineilla on havaittu useita mahdollisesti neuropatogeenisia piirteitä in vitro ja eläinmalleissa.
Vaiheen II kliiniset tutkimukset HERV-Wenv-retroviruksen yhteydestä MS-tautiin ovat käynnissä. HERV-W/MSRV assosiotuu silmiinpistävän selvästi MS-taudin oireiden sekä relapsi- ja remissiovaiheiden kanssa.
HERV-Wenv-proteiinia ilmentyy runsaasti aktiivisissa MS-plakeissa. Varhainen MSRV -löydös selkäydinnesteessä ennustaa MS-taudin ilmaantuvuuden ja etenemisen jopa 10 vuotta ennen kliiniseen MS-tautiin sairastumista.
Tehokkaat MS-hoidot vähentävät MSRV/Syncytin-1/HERV-W-proteiinien ilmentymistä. Epstein-Barr-virus (EBV) aktivoi HERV-W/MSRV:n in vitro ja in vivo-malleisssa potilailla, joilla oli tarttuva mononukleoosi, sekä kontrolleilla, joilla on korkea anti-EBNA1-IgG-tiitteri.
Kaksi EBV/MS-linkkiä: (1) tarttuva mononukleoosi ja (2) korkeat anti-EBNA1-IgG-tiitterit assosioituvat HERV-W/MSRV:n aktivoitumiseen. Tutkimusnäyttö viittaa siihen, että EBV voi toimia MS-taudin laukaisijana vuosia EBV-infektion jälkeen aktivoimalla MSRV-retroviruksen, joka toimii suorana MS-taudin puhkeamiseen ja oireisiin vaikuttavana neuropatogeenisena efektorina ennen MS-tautia ja taudin aikana.
HERV-Wenv-proteiinilla on immunopatogeenisia ja neuropatogeenisia vaikutuksia in vitro ja eläinmalleissa. MSRV-löydöksen jälkeen useat tutkimusryhmät ovat vahvistaneet riippumattomasti HERV-W:n ja MS-taudin välisen vahvan assosiaation MS-potilailla.
Selkäydinnesteen MSRV-löydös rinnastuu MS-taudin puhkeamiseen, etenemiseen ja hoitovasteisiin. In vivo-malleissa optiseen neuriittiin sairastuneilla potilailla selkäydinnesteen MSRV viittaa vahvasti MS-tautiin.
Potilaiden selkäydinnesteestä tehdyt MSRV-löydökset ennustavat MS -taudin alkaessa nopeasti etenevää tautia. Löydöksellä on vahva yhteys siihen, että MS-tauti etenee RRMS-tautimuodosta toissijaisesti eteneväksi SPMS-tautimuodoksi 10 vuoden sisällä. MS -tautia sairastavien genomissa on enemmän MSRV -DNA -kopioita kuin terveillä kontrolleilla.
HERV-W/MSRV:tä voidaan näin pitää vahvana biomarkkerina MS-taudille, sen etenemiselle ja hoitovasteelle.
In vitro-malleissa HERV-W/MSRV/Syncytin-1:n ilmentymistä verisoluissa ja astrosyyteissä säätelevät tulehdusta edistävät sytokiinit. Interferoni-alfa ja interferoni-β estävät sitä. Havainto vahvistaa, että sekä MSRV että Syncytin-1 voidaan aktivoida tulehduksellisessa ympäristössä, kuten havaittiin in vivo MS-mallissa. Havainto viittaa myös siihen, että HERV-Wenvin neurotoksiset ja immuunijärjestelmään liittyvät ominaisuudet vaikuttavat MS-taudin patogeneesiin. Tällaista päätelmää vahvistavat havainnot, joiden mukaan EBV aktivoi HERV-W/MSRV/Syncytin-1-retroviruksia verestä ja aivoista peräisin olevissa soluissa in vitro ja että HERV-W/MSRV aktivoituu in vivo potilailla, joilla on tarttuva mononukleoosi.
Havainnot vahvistavat, että kaksi pääyhteyttä Epstein-Barr-viruksen ja MS-taudin välillä (tarttuva mononukleoosi ja korkeat anti-EBNA-1-IgG-tiitterit) rinnastuvat neuropatogeenisen HERV-W/MSRV:n aktivoitumiseen. EBV on siis hyvin todennäköisesti yhteydessä MS-taudin puhkeamiseen myöhemmällä iällä. Lisäksi HERV-W/MSRV voi olla yhdistävä linkki MS-taudin puhkeamiseen vaikuttavien tekijöiden (esim. sikiöaikaiset matalat D-vitamiinitasot, taudille altistavat geenit jne.) sekä neurodegeneraatioon johtavan immunopatogeenisen kaskadin välillä. (2)
Virusten yhteyttä autoimmuunitauteihin on tutkittu paljon. Harmillisen harvat ymmärtävät, että myös lievät ja oireettomat infektiot voivat johtaa krooniseen sairastumiseen. SARS-CoV-2 voi laukaista autoreaktiivisen immunologisen prosessin, jossa seurauksena on parantumaton autoimmuunitauti. Toistaiseksi SARS-CoV-2-virus on niin uusi, että emme vielä tiedä minkälaisia pitkäaikaisoireita koronainfektio voi aiheuttaa. Kevytmielinen ja vähättelevä suhtautuminen lieviinkin infektioihin voi olla virhe.
Jyväskylän yliopiston tutkijoilta ehdotus mekanismiksi, jolla virusinfektio aiheuttaa autoimmuunitaudin
Leona Gilbertin tutkimusryhmä sai näyttöä virusinfektion autoimmuunitautiin liittävästä mekanismista hiirillä tehdyissä kokeissa. Kokeissa havaittiin virusinfektion aikana tapahtuvan solu- ja kudosvaurion liittyvän autoimmuunireaktioon eli elimistön oman immuunijärjestelmän hyökkäykseen elimistön omaa DNA:ta vastaan.
Autoimmuunitautien puhkeamisen täsmällinen mekanismi ei ole tiedossa. Tiedetään, että perinnöllinen alttius ja yksi tai useampi ympäristötekijä voi johtaa sairastumiseen.
Eräitä yleisiä bakteeri- ja virusinfektioita on yhdistetty autoimmuunisairauksiin. Esimerkiksi ihmisen parvovirus B19 on yhdistetty nivelreuman kaltaiseen autoimmuunisairauteen ja EBV MS-tautiin.
Parvovirus B19 on hyvin yleinen virus, jonka aiheuttama infektio voi olla oireeton tai aiheuttaa lieviä flunssan kaltaisia oireita.
Ihmisen parvovirus B19 NS1-proteiinin tiedetään aiheuttavan apoptoottista solukuolemaa. Infektion aikaan patogeeni voi aiheuttaa liiallisen määrän solukuolemia ja se kuormittaa immuunijärjestelmää.
Parvovirusinfektiossa muodostuvat apoptoottiset kappaleet johtivat hiirillä immuunivasteen aktivoitumaan omaa DNA:ta vastaan
Leona Gilbertin mukaan virusinfektion seurauksena muodostuneet apoptoottiset kappaleet, joissa on mukana sekä viruksen NS1-proteiinia että isäntäsolun rakenteita, saivat aikaan autoimmuunireaktion. Tutkimuksessa autoimmuunireaktio johti solu- ja kudosvaurioihin hiirien aivoissa, sydämessä, munuaisessa ja maksassa. Linkki artikkeliin: https://doi.org/10.1093/infdis/jiy614
COVID-19
SARS-CoV-2- viruksen deltavariantin tarttuvuusluku (R0)on samaa luokkaa vesirokon kanssa (8,0-9,5). Molemmat virustaudit leviävät herkästi väestössä aerosoli-, pisara- ja kosketustartuntoina.
Deltavariantin HIT (Herd Immunity Treshold) – eli taso, jolla laumasuoja saavutetaan on 80-89. Tämä tarkoittaa, että 80-89 %:lla väestöstä pitäisi olla immuniteetti, että viruksen leviäminen väestössä estyisi. Laumasuojan saavuttamista ei enää pidetä mahdollisena. Deltavariantin leviämisen pysäyttämiseksi ei voi tehdä juuri mitään. On mahdollista, että deltavariantti, delta+ tai epsilonvariantti läpäisee koko väestön aiheuttaen rokotetuille kuitenkin lievemmän infektion kuin rokottamattomille. Infektion kesto vaikuttaa mahdollisiin jälkioireisiin.
Deltavariantti leviää lapsilla ja nuorilla, mutta myös rokotuksen saaneilla aikuisilla. Rokotusten antama suoja deltavarianttia vastaan on 42-76 % (Pfizer & Moderna). Rokotukset estävät tehokkaasti sairaalahoitoa vaativat vakavat infektiot. Hiljattain julkaistun tutkimuksen mukaan 97 % sairaalahoitoa vaativista potilaista ja 99,99 % koronaan kuolleista oli rokottamattomia.
Lähes kaikki koronainfektioon sairastuneista toipuvat täysin muutamassa viikossa. Osalla jopa taudin lievänä tai oireettomana sairastaneista tautiin liittyvät oireet voivat palata ensimmäisen toipumisjakson jälkeen ja jatkua kuukausia varsinaisen infektion jälkeen. Toistaiseksi kukaan ei tiedä aiheuttaako koronainfektio pysyviä oireita.
Koronan pitkäaikaisvaikutuksia ei vielä tunneta riittävän hyvin. Sairastettu koronatauti aiheuttaa kuitenkin mitattavia ja havaittavia neurologisia, psykologisia ja kognitiivisia oireita, jotka joissain tapauksissa voivat kroonistua pitkäkestoisiksi tai pysyviksi.
Aivojen lisäksi korona voi vahingoittaa keuhkoja, sydäntä, maksaa ja munuaisia. On mahdollista ellei peräti todennäköistä, että tauti voi laukaista jonkin vielä tuntemattoman autoimmuunitaudin nuorilla, joilla on kyseiselle autoimmuunitaudille geneettinen alttius. Tämä nähdään kuitenkin vasta vuosien päästä, sillä autoimmuunitaudit kehittyvät usein hitaasti ja vähäoireisina kunnes oireiden kirjo johtaa positiiviseen diagnoosiin. Virusinfektiot voivat myös vaikuttaa solun tumassa sijaitsevaan DNA:han ja muuttaa soluja pahanlaatuisiksi, kuten on havaittu eräiden ihmisten papilloomavirusten kohdalla.
Lievienkin infektioiden aiheuttamat autoimmuunitaudit voivat pilata nuoren tulevaisuuden.
Covid-19: pitkäkestoisia oireita
COVID-19-oireet voivat toisilla jatkua useita kuukausia. Infektio vahingoittaa keuhkoja, sydäntä ja aivoja, mikä lisää pitkäaikaisten terveysongelmien riskiä. Jatkuvat oireet viittaavat COVID-19-infektion jälkeiseen oireyhtymään eli ”pitkään koronaan”.
Iäkkäillä, lihavilla ja yleissairailla varsinaisen infektion jälkeen jatkuvat COVID-19-oireeet ovat todennäköisempiä kuin nuoremmilla ja terveemmillä, mutta myös nuoret ja terveet voivat tuntea olonsa huonoksi viikkoja tai kuukausia tartunnan jälkeen. Yleisiä merkkejä ja oireita, jotka viipyvät ajan myötä, ovat:
- hengästyminen & hengitysvaikeudet
- yleinen uupumus
- yskä
- nivelkivut
- rintakivut
- muisti-, keskittymis ja univaikeudet
- lihas- ja päänsäryt
- nopea ja hakkaava syke
- haju- ja makuaistin menettäminen
- ahdistuneisuus ja masennus
- kuume
- huimaus seistessä
COVID-19 vaikuttaa ensisijaisesti keuhkoihin, mutta se voi vahingoittaa myös monia muita elimiä. Nämä elinvauriot lisäävät pitkäkestoisten ja pysyvien terveysongelmien riskiä.
Elimiä, joihin COVID-19 voi vaikuttaa, ovat:
Sydän: Sydänkuvat osoittavat koronainfektion aiheuttavan pysyviä vaurioita sydänlihakselle. Sydän voi vahingoittua myös ihmisillä, jotka ovat sairastaneet lievän tai oireettoman koronan. Tämä lisää sydämen vajaatoiminnan sekä muiden sydänkomplikaatioiden riskiä.
Keuhkot: Koronainfektioon liittyvä keuhkokuume voi aiheuttaa pitkäaikaisia vaurioita keuhkoihin. Keuhkoihin muodostuva arpikudos johtaa usein pitkäaikaisiin hengitysvaikeuksiin.
Aivot: Koronainfektio voi aiheuttaa aivohalvauksia, kohtauksia ja Guillain-Barren oireyhtymää, joka aiheuttaa ohimeneviä halvauksia myös nuorilla sairastuneilla. COVID-19 voi lisätä riskiä sairastua Parkinsonin- tai Alzheimerin tautiin.
Eräillä sairastuneilla esiintyy lisäksi monisysteemistä tulehduksellista oireyhtymää (multisystem inflammatory syndrome), jossa tulehdus leviää moniin kudoksiin ja elimiin.
Veritulpat ja verisuoniongelmat: Koronainfektio vaikuttaa veren hyytymiseen ja johtaa usein verihyytymien muodostumiseen. Suuret verihyytymät voivat aiheuttaa sydänkohtauksia ja aivohalvauksia, mutta suurin osa koronainfektion aiheuttamista sydänvaurioista johtuu hyvin pienistä hyytymistä, jotka tukkivat pieniä verisuonia (kapillaareja) sydänlihaksessa.
Muita veren hyytymisen vaikutuksille alttiita kehon osia ovat keuhkot, jalat, maksa ja munuaiset. Koronainfektio heikentää verisuonia ja aiheuttaa niiden vuotamista, mikä edistää mahdollisesti pitkäaikaisia maksa- ja munuaisvaurioita.
Mieliala- ja ja uupumisoireet: Potilaat, joilla on vakavia oronaoireita, voivat joutua tehohoidossa hengityskoneeseen, mikä lisää traumaperäisen stressihäiriön, masennuksen ja ahdistuksen riskiä.
Koska koronainfektion pitkäkestoisia oireita ja mahdollisia jälkitauteja ei vielä tunneta kovinkaan hyvin, tutkijat tekevät valistuneita arvauksia vastaavien virusinfektioiden, kuten SARSin perustella. Monilla SARSin sairastaneilla esiintyy kroonista väsymysoireyhtymää. Myös Covid-19 johtaa joillain potilailla krooniseen väsymysoireyhtymään. Tälle on ominaista äärimmäinen väsymys, joka pahenee liikunnan ja henkisen toiminnan seurauksena, eikä helpota edes levätessä.
Infektio voi laukaista autoimmuunitaudin
Infektioiden yhteyttä autoimmuunitauteihin on tutkittu paljon. Koronaviruksen deltavariantin vuoksi koronan mahdollinen vaikutus jonkin autoimmuunitaudin puhkeamiseen on ajankohtainen ja tärkeä.
Väheksyvä suhtautuminen SARS-CoV-2-viruksen aiheuttamiin infektioihin on lyhytnäköistä, piittaamatonta ja todennäköisesti pitkällä aikavälillä hyvin haitallista. Nyt tehtävien valintojen laajemmat yhteiskunnalliset seuraukset nähdään vasta vuosien tai vuosikymmenten jälkeen.
Autoimmunireaktio
Autoimmunireaktiolla tarkoitetaan immuunivastetta, jossa kehon oma puolustusjärjestelmä tunnistaa omia kudoksia virheellisesti vieraaksi ja hyökkää niitä vastaan. Geneettisten tekijöiden lisäksi ympäristötekijöillä (erityisesti viruksilla, bakteereilla ja muilla taudinaiheuttajilla) uskotaan olevan merkittävä rooli autoimmuunitautien kehittymisessä.
Tässä katsauksessa tarkastellaan mekanismeja, joilla patogeeni voi aktivoida immuunijärjestelmän virheellisen toiminnan. Lisäksi tutustutaan todisteisiin, jotka liittävät infektiot autoimmuunitauteihin ja luodaan katsaus eläinmalleihin, joita on sovellettu patogeenien laukaiseman infektion ja autoimmuunitautien välisen yhteyden selvittämiseksi.
Infektiosta autoimmuunitautiin
Autoimmuunitauteja tunnetaan yli 80 [1]. Monet tekijät, kuten geenimuutokset, ikä, sikiöaikaiset alhaiset D-vitamiinitasot ja ympäristö edistävät immiinijärjestelmän herkistymistä omille kudoksille.
Virukset, bakteerit ja muut infektioita aiheuttavat taudinaiheuttajat voivat tutkimusten perusteella toimia autoimuunitaudin laukaisevina ympäristötekijöinä.
MHC
|
MHC-proteiinit ovat MHC-geeniperheen (major histocompatibility complex) koodaamia selkärankaisten solujen solupinnan glykoproteiineja. Ihmisen MHC-proteiineja kutsutaan myös HLA-antigeeneiksi (human-leucocyte-associated antigens), koska ne tunnistettiin ensimmäisenä leukosyyttien pinnalta. |
|
MHC-proteiineja koodaa noin 20 geeniä, joista useimmat ovat erittäin polymorfisia: geeneistä on tunnistettu yli 2 000 eri alleelia. Tämän vuoksi on epätodennäköistä, että kahdella eri yksilöllä (lukuun ottamatta identtisiä kaksosia) olisi sama yhdistelmä MHC-alleeleja. |
|
MHC-molekyylejä on kahta tyyppiä: luokan I MHC- ja luokan II MHC-molekyylit. Luokan I MHC-proteiineja ilmennetään lähes kaikissa selkärankaisten solutyypeissä, ja ne esittelevät antigeenejä sytotoksisille T-soluille. Luokan II MHC-proteiineja ilmennetään pääasiassa soluissa, jotka ovat vuorovaikutuksessa auttaja-T-solujen kanssa, kuten dendriittisoluissa, makrofageissa ja B-lymfosyyteissä. |
|
MHC-proteiinit toimivat immunologisessa puolustuksessa sitoen antigeeninä toimivan proteiinin pilkkoutumisen seurauksena syntyneitä peptidifragmentteja ja kuljettaen niitä antigeeniä esittelevän solun (dendriittisolu naiivien T-solujen tapauksessa) pinnalle, jossa ne esitellään yhdessä muiden stimulatoristen signaalien kanssa T-soluille. Tämän seurauksena aktivoituneet efektori-T-solut tunnistavat saman peptidi-MHC-kompleksin kohdesolunsa pinnalla, mikä voi sytotoksisten T-solujen tapauksessa olla mikä tahansa infektoitunut elimistön solu, auttaja-T-solujen tapauksessa B-solu, sytotoksinen T-solu, infektoitunut makrofagi tai dendriittisolu itse. Solunetti |
Antigeenejä esittelevät solut, kuten dendriittisolut, kaappaavat antigeenejä ja prosessoivat ne peptideiksi, jotka viedään MHC-molekyyleihin (Major Histocompatibility Complex)esitettäväksi T-soluille klonotyyppisten T-solureseptorien (TCR) kautta.
Sytolyyttiset (soluja hajottavat) T -solut voivat hajottaa kohdekudoksen soluja (MHC- I), kun taas T -auttajasolut (Th) vapauttavat sytokiinejä, jotka aktivoivat makrofageja, monosyyttejä ja B -soluja (MHC – II) tai vaikuttavat suoraan kohdekudokseen. B-soluilla on pintareseptoreita, jotka voivat sitoa antigeenejä.
Vastaanotettuaan signaaleja Th-soluista B-solut erittävät antigeeneille spesifisiä vasta-aineita (immunoglobuliineja, eli vasta-aineina toimivia proteiineja, joiden molekyyli koostuu kahdesta raskasketjusta ja kahdesta kevytketjusta ja jotka jakaantuvat raskaiden ketjujen rakenteen perusteella ryhmiin IgA, IgD, IgE, IgG ja IgM ). Vasta-aine voi sitoutua suoraan patogeeniin tai makrofageihin ja aktivoida niitä samanaikaisesti Fc -reseptorin välityksellä.
Eräät patogeenit sisältävät rakenteita (esim. glykoproteiineja), jotka ovat aminohapposekvenssiltään tai rakenteeltaan samankaltaisia omien antigeeniemme kanssa. Jos taudinaiheuttajan rakenne muistuttaa riittävästi omien kudostemme rakennetta (Molecular Mimicry), immuunijärjestelmä voi tulkita omat kudokset vieraiksi aineiksi ja herkistyä omille kudoksille.
Molecular mimicry-efektissä omien kudosten ja taudinaiheuttajien rakenteen samankaltaisuus aktivoi T- ja B-soluja, jotka yleensä herkistyvät vain taudinaiheuttajalle. Immuunivasteet ovat ristiinreaktiivisia itselleen ja johtavat kudosvaurioihin sekä muiden immuunijärjestelmän osien aktivoitumiseen.
Taudinaiheuttaja voi myös johtaa tautiin epitoopin (antigeenimolekyylin osa, jonka immuunijärjestelmä tunnistaa ja johon se reagoi) leviämisen kautta. Tässä mallissa immuunivaste pysyvälle patogeenille tai jatkuva patogeenin suora hajoaminen aiheuttaa vaurioita omalle kudokselle. Antigeeniä esittelevät solut (APC) esittelevät aurioituneesta kudoksesta vapautuneita antigeenejä ja tämä käynnistää itsespesifisen omiin kudoksiin kohdistuvan immuunivasteen.
’Sivullisen aktivaatio’ kuvaa autoimmuunisolujen epäsuoraa tai epäspesifistä aktivoitumista, jonka aiheuttaa infektion aikana esiintyvä tulehduksellinen ympäristö. Dominoefekti voi ilmetä, jolloin immuunijärjestelmän yhden osan epäspesifinen aktivointi johtaa muiden osien aktivoitumiseen.
Lopuksi infektio voi johtaa autoimmuuniin käsittelemällä ja esittämällä ”salaisia antigeenejä”. Toisin kuin hallitsevat antigeenitekijät, subdominantit salaiset antigeenit ovat normaalisti näkymättömiä immuunijärjestelmälle. Tulehduksellinen ympäristö, joka syntyy infektion jälkeen, voi saada aikaan lisääntyneen proteaasituotannon ja vapautettujen itse-epitooppien erilaisen käsittelyn antigeenejä esittelevien solujen toimesta.
Kuva1
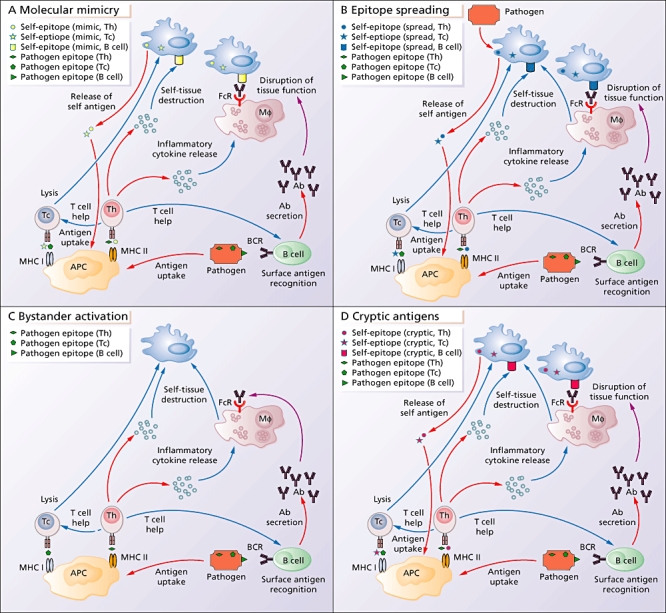
Mekanismit, joilla taudinaiheuttajat voivat aiheuttaa autoimmuunisairauksia.
(a) Molekyylinen matkiminen tapahtuu, kun patogeenistä johdetut epitoopit ovat ristireaktiivisia itse johdettujen epitooppien kanssa. Antigeeniä esittelevät solut (APC) ottavat patogeenistä johdetut epitoopit ja esittävät ne sytolyyttisille T-soluille (Tc) luokan I tärkeimmän histokompatibiliteettikompleksin (MHC) kautta tai auttaja-T-soluille (Th) MHC-luokan II kautta. T-solut, jotka aktivoivat patogeeniset epitoopit, jotka ovat ristireaktiivisia itse-epitooppien kanssa, voivat sitten vahingoittaa omien kudosten hajoamisen (Tc) tai sytokiinien (Th) vapautumisen kautta.
Aktivoitujen Th -solujen vapauttamat sytokiinit voivat aktivoida makrofageja (Mφ) tai tarjota apua B -soluille. B-solun B-solureseptori (BCR) tunnistaa patogeenistä peräisin olevat pinta-antigeenit, mikä laukaisee vasta-aineiden erityksen. Nämä vasta-aineet voivat aiheuttaa vahinkoa sitoutumalla kudosten pinnalla oleviin ristireaktiivisiin epitooppeihin ja häiritsemällä kudosten toimintaa, tai vasta-aineen Fc-osa voi sitoutua samanaikaisesti Mc:n Fc-reseptoriin (FcR); tämä saa Mφ:n tuottamaan kudosta vahingoittavia sytokiinejä. Vaurioitunut kudos vapauttaa enemmän ristireaktiivisia antigeenejä, jotka APC:t ottavat käyttöön ja lisäävät vaurioita.
(b) Epitoopin leviämisessä immuunivaste pysyvälle patogeenille tai oman kudoksen suora hajoaminen pysyvän patogeenin vaikutuksesta vahingoittaa omaa kudosta. Vaurioituneesta kudoksesta vapautuneet antigeenit ottavat APC:t, ja tämä käynnistää immuunivasteen, joka kohdistuu omiin antigeeneihin.
(c) Sivullisen aktivoinnissa immuunijärjestelmän eri osat reagoivat hyökkääviin patogeeneihin. Tämän vasteen aiheuttama tulehduksellinen ympäristö vahingoittaa omaa kudosta epäspesifisellä antigeenillä ja lisäksi laukaisee immuunisolujen epäspesifisen aktivaation.
(d) Toisin kuin hallitsevat antigeenitekijät, subdominantit salaiset antigeenit ovat normaalisti näkymättömiä immuunijärjestelmälle. Tulehduksellinen ympäristö, joka syntyy infektion jälkeen, voi lisätä proteaasituotantoa ja vapautuneiden itseepitooppien erilaista käsittelyä APC:ssä.
Tässä katsauksessa keskustelemme käytettävissä olevista todisteista eräiden patogeenien osallistumisesta autoimmuunisairauksien puhkeamiseen ja pahenemiseen. On todisteita siitä, että immuunijärjestelmän eri osat osallistuvat moniin mekanismeihin sekä ihmisten sairauksissa että eläinmalleissa.
Coxsackievirus B
| Coxsackievirus kuuluu mm. kuumetta ja lihassärkyjä aiheuttaviin enteroviruksiin, jotka voivat joskus aiheuttaa myös aivokalvotulehduksen, aivotulehduksen tai sydänlihastulehduksen; ks. enterovirus |
Coxsackievirus B (CVB) on yleisin tarttuvaa sydänlihastulehdusta aiheuttava virus. Virus ja viruksen RNA voidaan eristää potilaan sydämestä [2–4]. CVB3 voi aiheuttaa sydänlihastulehduksen hiirillä; useimmissa hiirikannoissa virustitteri saavuttaa huippunsa infektion jälkeisenä päivänä 4 eikä sitä voida havaita 14 päivän kuluttua [5].
Taudin krooniselle vaiheelle (28. päivästä eteenpäin) on tunnusomaista mononukleaaristen solujen tunkeutuminen sydänlihakseen ja vasta -aineiden tuotanto sydämen myosiinia vastaan, jotka viruksen puuttuessa käynnistävät autoimmuunisairauden patofysiologisen mekanismin taudin tässä vaiheessa.
In vitro virus voi tartuttaa ja hajottaa sydämen myosyyttejä [6] ja CVB -infektio aiheuttaa sydänlihaksen tuhoutumisen SCID -hiirissä (joilta puuttuvat T- ja B -solut), mikä osoittaa, että virus voi suoraan tartuttaa ja hajottaa soluja [7,8].
Tämä vaurio voi johtaa autoimmuunireaktioon epitoopin leviämisen kautta. Hiirillä syntyy virusspesifisiä vasta-aineita pian infektion jälkeen, minkä jälkeen muodostuu vasta-aineita useille sydämen proteiineille, kuten myosiinille, tropomyosiinille ja aktiinille [9–11]. T-soluilla on myös tärkeä rooli [12–15].
CD8+ T -solujen ehtyminen lisää sydänlihastulehdusta tartunnan saaneilla hiirillä, mikä osoittaa tämän osajoukon tärkeyden hiirissä [16]. Neutraloivat anti-mCVB3-monoklonaaliset vasta-aineet (mAb), jotka saattoivat aiheuttaa sydämen patologian, kun ne siirrettiin hiiriin, olivat myös ristireaktiivisia sydämen myosiinille ja sydämen fibroblastien pintaepitoopeille, mikä viittaa molekylaarisen matkimiseen mahdollisena mekanismina [17, 18].
Tartunnan saaneiden hiirten T -solukloonit lisääntyvät vasteena sydämen myosiinille [19,20]. Kaikki tutkimukset eivät ole onnistuneet havaitsemaan ristireaktiivisia T- tai B-soluja tai matkivia sekvenssejä viruksen kapsidissa [21]. On kuitenkin havaittu, että geneettisesti vastustuskykyisten hiirien tuumorinekroositekijä (TNF) -α- tai interleukiini (IL) -1 -käsittely voisi tehdä hiiristä alttiita sydänsairauksille, mikä viittaa siihen, että sivullisen aktivaatio voi olla autoimmuunimekanismi.
CVB3 -infektio lisää soluproteiinien ubikvitinaatiota [9–11], ja tämä lisääntynyt solujen hajoaminen voi myös johtaa salaisten epitooppien vapautumiseen. Vaikka nämä tutkimukset osoittavat, että monet autoimmuunimekanismit voivat johtaa kardiomyopatiaan tartunnan saaneilla hiirillä, on edelleen epävarmaa, johtuuko autoimmuunisairaus ihmisillä havaitusta patologiasta [22–24].
Streptococcus pyogenes: A-streptokokki
| Streptokokki A eli Streptococcus pyogenes on beetahemolyyttinen grampositiivinen kokkibakteeri. Pyogenes viittaa bakteerin kykyyn tuottaa märkää eli aiheuttaa märkiviä infektioita. Bakteerista käytetään kirjallisuudessa usein lyhennettä GAS (Group A Streptococcus). |
S. pyogenes -infektio voi johtaa sydämen tulehdukseen, ja lymfosyyttien osallistumista sydämen patologiaan pidetään todennäköisenä [25, 26]. Tutkimukset ovat osoittaneet, että bakteerimateriaalit ja DNA voivat säilyä isäntäkudoksessa muutaman vuoden tartunnan jälkeen, joten on mahdollista, että jatkuva immuniteetti bakteereja vastaan voi johtaa elimen sivuvaurioon [23].
Pääasiassa pidetään todennäköisenä, että autoimmuunireaktion aiheuttaa molekyylinen matkiminen. Myosiini on tunnistettu hallitsevaksi autoantigeeniksi sydämessä, ja myosiinireaktiivisen mAb:n, joka on peräisin akuutista reumaattisesta kuumeesta kärsivistä potilaista, osoitettiin olevan ristireaktiivisia sekä M-proteiinille (ryhmän A streptokokkien tärkein virulenssitekijä) [27] kuin streptokokille hiilihydraatti-epitooppi N-asetyyliglukosamiini [28].
Samanlainen ristireaktiivisuus havaittiin mAb:llä, joka oli peräisin hiiriltä, jotka oli immunisoitu S. pyogenes -kalvoilla [29,30]. Ristireaktiivista mAb: tä on havaittu muille sydämen proteiineille, kuten tropomyosiinille ja laminiinille [31,32].
T-solukloonit reumaattisten sydänsairauksien potilaiden sydänvaurioista sekä niiden perifeerisen veren mononukleaariset solut (PBMC) voivat tunnistaa samanaikaisesti streptokokki-M-proteiinin ja sydänkudoksesta peräisin olevat proteiinit, kuten myosiinin, tropomyosiinin ja laminiinin [33–36]. Ihmisen sydämen myosiinilla immunisoiduilla BALB/c-hiirillä kehittyi T-soluja ristireaktiivisesti M-proteiinin kanssa [37], ja M-proteiinilla immunisoitujen rottien T-solulinjat olivat myös ristireaktiivisia myosiinin kanssa [38]. Nämä M-proteiinilla immunisoidut rotat kehittävät sydänvaurioita, mikä on hyvä argumentti siitä, että matkiminen on merkittävä patologinen mekanismi ihmisen reumaattisessa sydänsairaudessa.
Sydänvaurioita voidaan indusoida myös bakteeri-infektion saaneilla kaneilla [39] ja hiirillä, jotka on immunisoitu bakteerikomponenteilla [40].
On arveltu, että [41,42] S. pyogenes -infektio voi aiheuttaa liike- ja käyttäytymishäiriöiden, kuten Sydenhamin chorean (tahdosta riippumattomat pakkoliikkeet), Touretten oireyhtymän ja pakko -oireisen häiriön, kehittymistä [43,44], mutta tästä ei vallitse yksimielisyyttä.
Potilailla, joilla on näitä häiriöitä, on usein vasta-aineita aivojen basaaliganglioille, ja perusaineiden ja S. pyogenes -peräisten proteiinien välinen molekulaarinen matkiminen on edelleen suurin oletettu taudin indusointimekanismi.
Kanit, jotka on immunisoitu streptokokki-M-proteiinilla, kehittivät vasta-aineita ristireaktiiviseksi useiden ihmisen aivoproteiinien kanssa, ja synteettiset M-johdetut peptidit estävät aivojen ristireaktiivisia vasta-aineita Sydenham-koreaa sairastavan potilaan seerumista [45].
Eräs tutkimuspaperi osoitti vasta-aineiden ristireaktiivisuuden S. pyogenes -kalvon ja hermosolusolun välillä potilailla, joilla oli Sydenham-korea [46]. Käyttämällä seerumia, aivo-selkäydinnestettä (CSF) ja Sydenham-chorea-potilaista peräisin olevaa mAb: tä havaittiin kaksoisspesifisiä vasta-aineita, jotka reagoivat sekä S. pyogenes-soluseinän (GlcNAc) immunodominanttisen hiilihydraatti-epitoopin että neuronien pinnalla olevan lysogangliosidi GM1: n kanssa [47] ]. Sama ryhmä osoitti, että streptokokkeihin liittyvien lasten autoimmuunisairauksien neuropsykiatristen häiriöiden potilaiden seerumeista peräisin olevat GlcNAc-reaktiiviset vasta-aineet estettiin lysogangliosidi GM1: llä [48] ja että Sydenham-chorea-potilaiden lysogangliosidi-GM1-reaktiivinen mAb voi myös reagoida solunsisäisen aivoproteiinin beetan kanssa -tubuliini [49].
Eläinmalleja on vähän, mutta Hoffman et al. osoitti, että osa Swiss -Jackson Laboratory (SJL)/J -hiiristä, jotka oli esikäsitelty S. pyogenes -homogenaatilla, kehitti liike- ja käyttäytymishäiriöitä [50]. Näiden hiirien aivoissa havaittiin olevan vasta -ainekerrostumia ja seerumin vasta -aine reagoi useisiin aivojen alueisiin.
Trypanosoma cruzi
Hyönteisten välittämä T. cruzi-loinen aihettaa Chagasin tautia [51,52]. 10–30 prosentille tartunnan saaneista kehittyy tauti, joka etenee kahdessa suuressa kliinisessä vaiheessa, akuutissa ja kroonisessa.
Akuutille vaiheelle on ominaista parasitemia, etenkin sydänlihassoluissa, ja tulehduksellinen infektio tartunnan saaneeseen kudokseen. Tämän jälkeen seuraa oireeton indeterminantti vaihe, joka voi kestää jopa 30 vuotta [53].
Potilaat, jotka etenevät taudin krooniseen vaiheeseen, kärsivät pääasiassa peruuttamattomasta kardiomyopatiasta [54–56]. Tämä viittaa siihen, että kudoksen tuhoutuminen, joka luonnehtii tätä vaihetta, voi olla suurelta osin autoimmuuni. CCC:lle on histopatologisesti tunnusomaista mononukleaaristen solujen infiltraatit. CD8+ T -soluja havaitaan noin kaksi kertaa enemmän kuin CD4+ T -soluja.
Paikallista interferoni (IFN) -γ-, TNF-α-, IL-4- ja IL-6-tuotantoa on raportoitu [57–59]. Lisäksi reaaliaikainen polymeraasiketjureaktio (PCR) -analyysi osoitti IFN-y-indusoituvien kemokiinien ja kemokiinireseptorien selektiivisen ylössäätelyn CCC-sydänkudoksessa [60]. Yhdessä nämä tiedot viittaavat siihen, että tulehduksellisten sytokiinien (erityisesti IFN-γ) välittämä sivullisen kudoksen tuhoaminen voi vaikuttaa CCC-patologiaan. CCC-potilaiden PBMC osoitti sytotoksisuutta ei-tartunnan saaneita sydämen myosyytejä vastaan [61] ja sytokiinituotantoa sydämen kudoshomogenaattia vastaan [62,63], mikä viittaa siihen, että soluvälitteinen vaurio voi olla myös kudosspesifistä.
Vasta-aineita sydänproteiinille Galectin-1 löydettiin CCC-potilaiden seerumeista ja sydänkudoksesta; tasot korreloivat sydänvaurion vakavuuden kanssa, ja mielenkiintoisesti niitä ei ollut kardiomyopatiassa, joka ei liittynyt T. cruzi -infektioon. On myös näyttöä molekyylien matkimisesta CCC:ssä. T. cruzi -proteiinin B13 havaittiin aiheuttavan ristireaktiivisia vasteita sydämen myosiinille sekä immuunijärjestelmän humoraalisesta [64,65] että CD4+ T-soluvarresta [66,67].
Lisäksi ristireaktiivisia vasta-aineita oli läsnä 100%:lla CCC-potilaista, mutta vain 14%:lla oireettomista tartunnan saaneista [65]. Suurin osa CCC:n eläinkokeista käyttää mallina hiirien T. cruzi -infektiota. C3H/HeJ-kannassa kroonisesti infektoituneiden hiirten sydäninfiltraatti koostuu pääasiassa CD8+ T-soluista, jotka erittävät IFN-y: tä ja TNF-a: ta, mikä heijastaa hyvin ihmisen histopatologiaa [68].
Muissa kannoissa CD4+ -T-solut ovat kuitenkin vastuussa patologiasta. Kroonisesti infektoituneet BALB/c- tai CBA -hiiret kehittävät CD4+ T -soluja, jotka lisääntyvät vasteena sydämen myosiinille, mutta eivät sydämen aktiinille [69]. Kroonisesti tartunnan saaneet BALB/c-hiiret hylkivät syngeenisiä sydämiä, ellei niitä hoidettu anti-CD4 (mutta ei anti-CD8) vasta-aineella [70].
CD4+ T-solulinja, joka oli peräisin kroonisesti infektoiduista DBA/2-hiiristä ja joka oli ristireaktiivinen sekä sydän- että T. cruzi -peräisten proteiinien kanssa, kykeni aiheuttamaan voimakkaan sydämen tulehduksen siirrettäessä tartunnan saaneisiin tai sydänimmunisoituihin BALB/c-karvattomiin hiiriin [71 ]. Girones et al. julkaisi tutkimuksen, joka osoitti, että hiiri- ja T. cruzi -peräisten proteiinien välillä oli T- ja B-solujen matkiminen. Tässä he osoittivat, että T. cruzi -infektoitujen hiirten T -solut olivat reaktiivisia sekä T. cruzin SAPA -antigeenille että homologiselle, äskettäin tunnistetulle Cha -autoantigeenille [72]. Näiden T-solujen siirtäminen hiirille tuotti anti-Cha-autovasta-aineita ja sydänvaurioita.
Useat tutkimukset ovat osoittaneet ristireaktiivisia vasta-aineita, jotka tunnistavat sydämen proteiineja, kuten myosiini- ja T. cruzi -antigeenejä [73–77].
Vaikka krooninen vaihe vaikuttaa yleensä sydämeen, osa potilaista kehittää ruoansulatuskanavan motorisia toimintahäiriöitä, pääasiassa enteerisen hermoston neuronien tuhoaminen [78]. On havaittu, että kanilla kohonneet vasta-aineet flagellum-assosioitua pintaproteiinia vastaan T. cruzilla (FL-160) ovat ristireaktiivisia 48 kDa:n proteiinin kanssa, joka löytyy yksinomaan hermokudoksesta [79].
On myös osoitettu, että FL-160:n aminoterminaalia vastaan nostetut vasta-aineet reagoivat eri epitooppiin nisäkkään istuinhermossa kuin vasta-aineet, jotka oli tuotettu karboksyylipäätä vastaan [80]. Tämän ilmeisen matkimisen lääketieteellinen merkitys on epävarma, koska ihmisen seerumien kyky reagoida FL-160:een ei korreloinut kliinisen sairauden kanssa [81].
Muut tutkimukset ovat myös osoittaneet molekyylisiä samankaltaisuuksia T. cruzi -antigeenien ja nisäkkään hermokudoksesta peräisin olevien antigeenien välillä [82,83].
Borrelia burgdorferi
| Borrelia burgdorferi on spirokeettoihin kuuluva bakteeri, joka aiheuttaa borrelioosi-infektiota. Bakteerin luonnollisena isäntänä toimivat pienet jyrsijät, kuten hiiret, mutta sitä levittävät muihin isäntiin, myös ihmisiin, Ixodes-suvun puutiaiset. Borrelia burgdorferi elää puutiaisen keskisuolessa, mutta leviää uuteen isäntään pureman kautta puutiaisen syljen mukana. Bakteeri voi muokata sen pintaproteiineja elämänvaiheen mukaan välttääkseen isännän immuunijärjestelmää. Siirtyessään nisäkäsisäntään yleisimmäksi pintaproteiiniksi vaihtuu VlsE. Tämä proteiini on tärkeä nimenomaan immuunijärjestelmän välttelyssä ja kroonisen infektion syntymisessä. Proteiinia koodaava vls-lokus luo bakteerille antigeenivariaatiota, jolloin antigeenin tunnistaminen vaikeutuu. |
Lymen tautia aiheuttaa punkin aiheuttama spirochete Borrelia burgdorferi (Bb). 60 prosentille hoitamattomista potilaista aiheutuu niveltulehdusta, joka voi kestää useita vuosia, pääasiassa suurissa nivelissä, kuten polvessa [84]. Näillä potilailla on korkeat Bb-spesifisten vasta-aineiden tiitterit, ja Bb-DNA voidaan havaita nivelnesteessä PCR: llä [85].
Potilaiden hoito antibiooteilla yleensä parantaa niveltulehdusta, mikä osoittaa, että sivullisen tulehdusreaktio spirokeetille aiheuttaa varhaisesen Lymen niveltulehduksen [86].
Osalla potilaista infektio etenee akuutista krooniseen niveltulehdukseen antibioottihoidosta ja nivelnesteessä havaittavan Bb -DNA:n puutteesta huolimatta [85–87]. Antibioottiresistentti Lymen niveltulehdus liittyy MHC-luokan II alleeleihin, ihmisen leukosyyttiantigeeniin (HLA) -DRB1 *0401, *0101 ja *0404, mikä osoittaa, että sen mekanismi on T-soluvälitteinen ja erilainen kuin akuutti Lymen niveltulehdus [88].
Solun ja humoraaliset vasteet Bb:n ulkopinnan proteiinille A (OspA) kehittyvät usein pitkittyneiden niveltulehdusten alussa noin 70 prosentilla potilaista, joilla on antibioottiresistentti Lyme-niveltulehdus, [89–92]. T -solu- ja humoraalisten OspA-vasteiden, mutta ei muille spirochete -antigeeneille herkistyneiden vasteiden, havaittiin korreloivan niveltulehduksen ja sen vakavuuden kanssa [92,93].
Erityisesti antibioottiresistentit potilaat reagoivat ensisijaisesti T-soluepitooppiin OspA165–173, ja tähän epitooppiin reagoivat T-solut laajenivat nivelnesteeseen verrattuna perifeeriseen vereen HLA-DRB1*0401 -positiivisilla potilailla [89,94,95] .
Ensimmäisessä tietokonealgoritmihaussa tunnistettiin lymfosyyttitoimintaan liittyvä antigeeni (LFA) 1αL332–340, peptidi, joka on peräisin ihmisen leukosyyttiadheesiomolekyylin kevyestä ketjusta. Homologisena OspA165–173:lle se kykenee sitomaan HLA-DRB1*0401:n [96].
Synoviaalisen nesteen mononukleaariset solut potilailta, joilla oli antibioottiresistentti niveltulehdus, tuottivat IFN-y: tä vasteena sekä OspA165–173:lle että LFA1αL332–340:lle, mikä viittaa siihen, että näiden kahden proteiinin välinen matkiminen voi aiheuttaa niveltulehdukseen liittyvän inflammatorisen reaktion. LFA-1α:ta on myös tunnistettu potilailla, joilla on antibioottiresistentti Lymen niveltulehdus [97].
Tutkimukset osoittivat, että hoitoresistentteillä potilailla LFA1αL332–340 oli heikko agonisti OspA165–173-spesifisille T-soluille ja aiheutti pääasiassa Th2-tyypin sytokiinin IL-13:n erittymistä [98]. LFA1αL332–340 sitoutuu hyvin HLA-DRB*0401:een, mutta ei yleisemmin liitettyyn alleeliin HLA-DRB1*0101 [99].
Lisäksi, vaikka ristireaktiivisia T-soluja tunnistettiin useimmissa potilaissa yhdessä tutkimuksessa, TFA-vasteen LFA1αL332–340-vasteen ja kliinisen tilan välillä ei ollut korrelaatiota [100].
Nämä tutkimukset heikentävät väitettä siitä, että LFA1αL332–340-ristireaktiivisuus on tärkeä antibioottiresistentin Lymen niveltulehduksen patologiassa. Toisaalta Maier et al. tunnisti 15 muuta ihmisen ja hiiren peptidiä, jotka voisivat stimuloida OspA165–173-spesifistä T-solun hybridoomaa [101], joten muut peptidit voivat osoittautua tärkeämmiksi sairauden patologiassa Bb:n kanssa [102–105].
C3H -hiirillä nivelet soluttautuvat neutrofiileihin 10–14 päivää infektion jälkeen ja niveltulehduksen huippuhetkellä (3–5 viikkoa) nivelvauriot osoittavat leukosyyttien tunkeutumista mononukleaarisiin soluihin [103]. C57BL/6-beige-hiirillä, joilla oli heikentynyt makrofagien liikkuvuus ja kemotaksi, kehittyi vaikea niveltulehdus [106], kun taas C57BL/6-hiirillä kehittyy minimaalinen niveltulehdus, ellei niillä ollut puutosta IL-10:stä ja IL-6:sta [107, 108]. Nämä tutkimukset osoittavat, että makrofagipohjaiset anti-inflammatoriset sytokiinit suojaavat näitä hiiriä vakavalta niveltulehdukselta.
Bb-spesifisten T-solujen siirtäminen yksin ilman B-soluja pahentaa ja nopeuttaa niveltulehduksen puhkeamista C57/BL6-SCID-hiirillä [109]. Jyrsijämallit ovat hyödyllisiä vain akuutin Lymen niveltulehduksen tutkimisessa, koska niveltulehdus paranee muutamassa viikossa eikä ole antibioottiresistentti [110].
Kroonista neuroborrelioosia sairastavien potilaiden seerumissa ja selkäydinnesteessä on raportoitu vasta -aineita, jotka reagoivat hermoakseleihin [111], samoin kuin vasta -aineita ja T -soluja, jotka ovat spesifisiä myeliinin perusproteiinille (MBP) [112,113]. Potilaan seerumi, joka oli reaktiivinen aksoneille ja neuroblastoomasoluille, oli myös ristireaktiivinen Bb-flagelliinin kanssa [111, 114].
Seuraavaksi havaittiin, että flagelliinin mAb oli ristireaktiivinen ihmisen lämpöshokkiproteiinin 60 ja neuroblastoomasolulinjojen kanssa [115, 116] ja hidasti neuriittien kasvua viljelmässä [117]. Vasta-aineiden ristireaktiivisuutta on kuvattu myös ihmisen keskushermoston (CNS) proteiinien ja Bb OspA:n välillä [118].
Useat isäntähermon peptidit tunnistettiin ristireaktiivisiksi kroonisen neuroborreliosi-potilaan CSF:n Bb-spesifisten T-solujen kanssa peptidikirjastojen ja biometristen tietojen analyysin avulla [119].
Tutkimukset viittaavat siihen, että sivulliset tulehdusvasteet tarttuvalle taudinaiheuttajalle voivat selittää selkeämmin tämän taudin aiheuttamat keskushermoston komplikaatiot [120–122].
Herpes simplex virus
Herpeettinen stromaalinen keratiitti (HSK) johtuu herpes simplex -viruksen (HSV) aiheuttamasta sarveiskalvon infektiosta ja voi johtaa sokeuteen [123,124]. Vaikka viruslääkkeet eivät estä etenemistä epiteeli-infektiosta stromaaliseen keratiittiin, HSK:n oireita voidaan lievittää immunosuppressiivisilla lääkkeillä, kuten kortikosteroideilla [125], mikä osoittaa, että HSK on autoimmuunisairaus.
Koska taudin tutkimiseen ihmisillä liittyy vaikeuksia, suuri osa HSK:n karakterisoinnista on hyödyntänyt hiiren HSV-1-infektiota. 72 tunnin kuluessa infektiosta muodostuu tulehdusta edistäviä sytokiinejä IL-1 ja IL-6, mikä johtaa neutrofiilien tuloon sarveiskalvon stroomaan [126–129].
Merkittävää on, että SCID -hiirillä, jotka on rekonstituoitu CD4+ T -soluilla ja tyhjennetty neutrofiileistä, esiintyy vähemmän HSK:ta [130]. Makrofagit ja luonnolliset tappaja (NK) -solut tulevat myöhemmin sarveiskalvoon ja voivat edistää sairauden patologiaa suoraan tai tulehduksellisten sytokiinien tuotannon kautta [131–134].
Noin 10 päivän kuluttua tartunnasta alkaa toinen tunkeutumisaalto, joka koostuu pääasiassa neutrofiileistä ja CD4+ T-soluista, mikä on vahvasti riippuvainen IFN-y:n paikallisesta tuotannosta [135, 136]. Mielenkiintoista on, että HSK: n huippu (päivä 14 infektion jälkeen) on 5-7 päivää sen jälkeen, kun tarttuva virus on tyypillisesti havaittavissa, mikä viittaa siihen, että HSK-patologia ei edellytä replikoituvan viruksen läsnäoloa [137,138].
Viruksen DNA:ta on kuitenkin havaittu vielä yli 37 päivää infektion jälkeen ja se voi stimuloida DC:itä ja makrofageja aktivoimaan T-soluja sivullisen aktivoinnin tai salaisten epitooppien avulla [139–141].
Varhaisessa vaiheessa havaittiin, että CD4+ T -solut olivat välttämättömiä HSK:n kehittymiselle [135, 136]. Molekyylien matkiminen todennäköisesti osallistuu prosessiin edellä mainittujen mekanismien lisäksi.
Sarveiskalvon spesifisten immunoglobuliinin (Ig) H-lokuksen epitoopin kanssa ristiin reagoivien T-solukloonien havaittiin myös tunnistavan HSV-1-proteiinista UL6-peptidin [142,143].
Näiden ristireaktiivisten T-solujen siirto aiheutti HSK-leesioita hiirillä, mutta HSV-1-virusmutantit, joilta puuttui UL6-peptidi, eivät aiheuttaneet HSK-leesioita herkistyneillä hiirillä. Muissa tutkimuksissa, joissa käytettiin eri tavoin herkistettyjä hiirikantoja, infektio ei tuottanut T -soluja, jotka olivat reaktiivisia UL6: lle tai IgH: lle [142, 143].
HSK -potilaiden sarveiskalvosta eristetyt T -solulinjat eivät osoittaneet reaktiivisuutta UL6:lle tai muille ihmisen sarveiskalvon antigeeneille [144–146]. Tämä viittaa siihen, että ihmisillä T -solut voivat aiheuttaa patologiaa sivullisen tuhoamisen kautta.
Uveiitti
Uveiitti on ryhmä silmänsisäisiä tulehdussairauksia, jotka voivat sokeuttaa sairastuneen [147]. On todennäköistä, että monet tämän taudin alaryhmät ovat autoimmuunivälitteisiä, osittain siksi, että ne liittyvät vahvasti tiettyihin HLA-alleeleihin [148].
Humoraaliset ja soluvälitteiset vasteet verkkokalvon antigeeneille interfotoreseptorin retinoidia sitovalle proteiinille ja S-antigeenille ovat hyvin mallinnettuja ihmisillä [149 150]. Eläinmallit jyrsijöillä ja kädellisillä (kokeellinen autoimmuuninen uveiitti, EAU) perustuvat näiden proteiinien ruiskuttamiseen Freundin täydelliseen adjuvanttiin. Singh et al. tunnistivat CD4+ T-soluepitoopin ihmisen S-antigeenissä ja useissa virus- ja Escherichia coli -peräisistä peptideistä, joilla oli samanlainen sekvenssi [151, 152].
Näillä jäljitteillä immunisoiduilla Lewis -rotilla havaittiin EAU:lle tyypillisiä kliinisiä ja histologisia ilmenemismuotoja, mukaan lukien tulehdukselliset infiltraatit sairaissa silmissä.
Imusolmukkeista suoritetut proliferaatiomääritykset osoittivat ristireaktiivisia vasteita matkijoiden ja verkkokalvon autoantigeenin välillä. Alkaen eri S-antigeenin CD4+ T-soluepitoopista, Wildner ja Diedrichs-Mohring löysivät jäljitteitä rotaviruksesta ja naudanmaidon kaseiinista [153].
Samassa tutkimuksessa uveiittia sairastavilla potilailla havaittiin lisääntynyt T-solu- ja vasta-ainevaste S-antigeenille ja kahdelle tunnistetulle matkijalle verrattuna terveisiin luovuttajiin. Lukuun ottamatta raporttia uveiitin puhkeamisesta lapsilla echovirus -infektion jälkeen, mitään taudinaiheuttajaa ei ole vielä liitetty epidemiologisesti uveiittiin [154].
Tyypin 1 Diabetes
Tyypin I diabetes (T1D) johtuu haimasolujen autoimmuunisesta tuhoutumisesta autoreaktiivisten T -solujen ja/tai tulehduksellisten sytokiinien vaikutuksesta.
Vaikka T1D:llä on selvä geneettinen komponentti, samamunaisten identtisten kaksosten konkordanssi (tutkittavan henkilön ja hänen verrokkinsa, kuten kaksosen samanlaisuus tutkittavan ominaisuuden suhteen – esim. molemmilla on tutkimuksen kohteena oleva sairauden vaaratekijä) on vain noin 40% [155,156].
Epidemiologiset todisteet viittaavat siihen, että patogeeneillä on rooli taudin synnyssä.
Tyypin 1 diabetekseen sairastumiseen on liitetty monia viruksia [157]. Tutkimukset osoittivat korkeampaa T1D-esiintyvyyttä ihmisillä, joilla on synnynnäinen vihurirokko [158] ja vasta-aineita haiman saarekesoluja vastaan vihurirokko-tartunnan saaneilla potilailla [159].
Sytomegalovirus (CMV) eristettiin T1D-potilaista [160] ja haiman saarekesolujen vasta-aineita havaittiin CMV-tartunnan saaneilla potilailla [161]. On myös havaittu, että sikotauti -infektio edeltää usein tyypin 1 diabeteksen puhkeamista lapsilla [162,163].
Äkillisesti alkanutta diabetesta sairastavien potilaiden haimasta eristetty CVB4 voi aiheuttaa diabeteksen hiirillä [163]. CVB4-spesifisiä IgM-vasta-aineita voidaan havaita lapsilla, joilla on äskettäin diagnosoitu tyypin 1 diabetes [164,165]. On olemassa joitakin todisteita siitä, että CVB4 voi aiheuttaa T1D:tä molekyylisen matkimisen kautta.
T1D-potilaista eristetyt T-solut reagoivat sekä glutamiinihapon dekarboksylaasin (GAD-65) (tunnistettu autoantigeeni T1D:ssä) että proteiinin 2C kanssa CVB4:ssä.
Toisessa tutkimuksessa ei havaittu samanlaista T-solujen ristireaktiivisuutta [166]. Toinen tutkimus puolestaan osoitti ristireaktiivisuutta sekä sairailla potilailla että terveillä verrokeilla [167]. In vitro -tutkimukset viittaavat siihen, että vihurirokkovirus voi vaikuttaa diabeteksen puhkeamiseen tuottamalla vasta-aineita ja CTL-soluja, jotka ovat ristireaktiivisia haiman beetasaarekkeiden kanssa [168,169].
On myös saatu näyttöä siitä, että CMV voi indusoida ristireaktiivisia vasta-aineita ja Th-soluja [161, 170]. In vitro -tutkimukset osoittivat, että sikotauti-virus voi tartuttaa ja replikoitua ihmisen solulinjoissa, indusoida IL-1:n ja IL-6:n vapautumisen ja säätää MHC-luokan I ja luokan II antigeenien ilmentymistä [171–173]. Koska viruksen on myös osoitettu replikoituvan haiman eksokriinisissä soluissa [174], on mahdollista, että sikotauti-viruksen aiheuttama sytokiinien vapautuminen ja HLA n lisäsäätely voivat johtaa autoimmuunireaktioon, joka aiheuttaa haiman β-solujen spontaania tuhoutumista.
T-soluvaste GAD-65:lle näyttää olevan tärkeä taudin patogeneesissä, ja epitoopin leviäminen voi sitten johtaa vasteisiin muihin autoantigeeneihin, kuten insuliiniin [175].
Vaikka yhdessä tutkimuksessa NOD-hiirten immunisointi CVB4: stä peräisin olevalla 2C-proteiinilla indusoiduilla T-soluilla ristireagoivat GAD-65: n kanssa (tukee matkimishypoteesia) [176], toisessa tutkimuksessa CVB4-infektio ei aiheuttanut ristireaktiivisia T-soluja [177] ].
Tutkimuksessa, jossa CVB4 nopeutti diabeteksen puhkeamista, havaittiin, että β-soluspesifisten T-solujen kynnystason oli oltava läsnä, jotta tauti kiihtyy [178]. Siten sivullisen aktivointi voi olla todennäköisempi selitys kuin molekyylin matkiminen NOD -mallissa.
BDC2,5 -hiiret ovat siirtogeenisiä diabeettiselle TCR:lle. Näillä hiirillä kehittyy diabetes, joka on samanlainen kuin CVB4-infektion jälkeen havaittu streptotsotosiinihoidon jälkeen (joka vahingoittaa haimaa), mutta ei poly I: C -hoidon (Toll-kaltainen reseptori-3-agonisti) jälkeen. Tämä viittaa siihen, että tässä mallissa salaisten antigeenien vapautuminen virusinfektion jälkeen voi olla diabeteksen induktion mekanismi [179].
Diabeteksen vastustuskykyisten BB (DR-BB) -rottien tartuttaminen Kilhamin rotaviruksella (KRV) aiheuttaa diabetesta noin 30%:lla näistä eläimistä ja insuliinitautia ilman diabetesta vielä 30%:lla [180].
Mielenkiintoista on, että toisin kuin CVB4 hiirillä, KRV ei ole troofinen haimassa, vaan pikemminkin imusolmukkeissa, pernassa ja kateenkorvassa.
Vielä ei täysin ymmärretä, miten tämä virus aiheuttaa diabeteksen tartuttamatta β-soluja, mutta makrofagien inaktivointi estää diabeteksen KRV-tartunnan saaneilla DR-BB-rotilla [181].
On myös näyttöä siitä, että virus voi laukaista aiemmin lepotilassa olevia β-soluspesifisiä T-soluja DR-BB-rotilla [182]. CVB4:n havaittiin aiheuttavan poikkeavuuksia glukoosinsietokokeissa ja heikentäneen insuliinin eritystä patas -apinoilla [183].
Guillain–Barrén oireyhtymä
Covid-19 voi aiheuttaa pitkäkestoisia (tai pysyviä) neurologisia, psykologisia ja kognitiivisia oireita ja Guillain–Barrén oireiyhtymää (GBS). Guillain–Barrén oireyhtymä on infektionjälkeinen immuunivälitteinen ääreishermostosairaus.
Guillain–Barrén oireiyhtymä on paralyyttinen sairaus, joka vaikuttaa sekä myeliiniin että ääreishermoston aksoneihin [184].
Useat tutkimukset ovat vahvistaneet glykolipidivastaisia vasta-aineita potilailla [185]. Taudista on olemassa erilaisia kliinisiä muotoja, jotka voivat korreloida vasta -aineiden kohdentaman glykolipidityypin kanssa.
Yleisimpiä hermokudoksissa esiintyviä glykolipidejä ovat gangliosidit ja cerebrosidit. GBS alkaa päiviä tai viikkoja infektion tai rokotuksen jälkeen [186].
Vaikka GBS:n kehittymiseen voi liittyä monia mikro -organismeja, Campylobacter jejuni on laajimmin tutkittu Guillain–Barrén oireiyhtymään assosioituva patogeeni, koska se usein edeltää diagnoosia. On saatu todisteita siitä, että bakteerien ulomman ytimen lipopolysakkaridi (LPS) voi jäljitellä isäntäganliosideja. GBS:ään liittyvien C. jejuni-serotyyppien LPS:n osoitettiin muistuttavan rakenteellisesti ihmisen gangliosideja [187, 188], ja hiirien, rottien ja kanien alustus edellä mainitulla LPS:llä tuotti vastaavia gangliosidivasta-aineita [189–191].
Tutkimukset ovat osoittaneet, että GBS:ään liittyvät C. jejunin serotyypit sisältävät todennäköisemmin gangliosidimaisia epitooppeja verrattuna serotyyppeihin, jotka on eristetty C. jejuni -infektoiduista potilaista, joilla on maha-suolitulehdus, mutta joilla ei ole neurologisia oireita. [192,193].
Yuki et al. osoitti, että C. jejuni LPS:llä immunisoiduille kaneille kehittyi raajojen heikkous, joka liittyi vasta -aineisiin gangliosidi GM1:tä vastaan sekä samanlainen perifeerisen hermoston patologia kuin GBS:ssä [194].
Nämä vasta-aineet voivat ristireagoida M. pneumoniae -bakteerin glykolipidien kanssa [195, 196].
Myös vasta -aineita GM1:lle on raportoitu [197]. Samoin kuin C. jejuni -infektion jälkeen, Haemophilus influenzae -infektion saaneet potilaat voivat kehittää vasta-aineita bakteeri-LPS:lle, jotka ovat ristireaktiivisia gangliosidin kanssa [198].
Gangliosidimaisen rakenteen läsnäolo H. influenzaen pinnalla viittaa siihen, että molekyylinen matkiminen voi selittää sen yhteyden GBS-induktioon [199, 200].

MS-tauti (multippeli skleroosi)
Multippeliskleroosille (MS) on ominaista keskushermoston aksoneja ympäröivän myeliinivaipan tuhoutuminen [201]. Demyelinaatioon liittyy kohonneita CD4+ T -solujen tasoja, jotka ovat spesifisiä tärkeimmille myeliiniproteiineille, ja taudin uskotaan yleensä olevan autoimmuuni [202–204].
MS-taudin laukaisevaa mekanismia ei vielä täysin ymmärretä. Sairastumiseen liittyy 100-200 geenialleelia, alhaiset sikiöaikaiset D-vitamiinitasot, sekä yksi tai useampi laukaiseva ympäristötekijä.
Relapsoivassa-remittoivassa tautimuodossa (RRMS) pahenemisvaiheet liittyvät vahvasti eksogeenisiin infektioihin ja aivan erityisesti ylähengitystieinfektioihin.
Ainakin 24 virustautia on liitetty MS-taudin patogeneesiin [205,206]. Suurin osa assosiaatioista on ollut epäsuoria, mutta joissakin tutkimuksissa on löydetty todisteita ihmisen kudoksen erityisistä patogeeneistä.
Tyypin 6 herpesviruksen antigeenejä löydettiin MS -plakeista, mutta ei muiden neurologisia häiriöitä sairastavien kudoksista [207].
Muiden neurologisia sairauksia sairastavien potilaiden CSF:ään (selkäydinnesteeseen) verrattuna MS -potilaiden selkäydinnesteessä osoitettiin olevan korkeampi Chlamydia pneumoniae -bakteerin taso [208].
In vitro -tutkimukset ovat myös vahvistaneet yhteyden infektioita aiheuttavien patogeenien ja MS-taudin välillä. MS -potilailla havaitaan aktiivisia MBP -spesifisiä T -soluja [209–211]. Potilailla on havaittu kahdeksaa patogeenistä peräisin olevaa peptidiä, mukaan lukien HSV:n, adenoviruksen ja ihmisen papilloomaviruksen epitoopit, jotka kykenevät aktivoimaan MS-potilaista peräisin olevia MBP-spesifisiä T-soluklooneja [212].
Näiden peptidien havaittiin olevan tehokkaimmin esillä HLA-DR2:n alatyypeissä, jotka liittyvät MS-alttiuteen. Huolimatta siitä, että MS-taudin yhdistäminen johonkin yksittäiseen patogeeniin on vaikeaa, vuosien mittaan raportoitu epidemiologinen näyttö vahvistaa, että ympäristötekijöillä on keskeinen rooli sairauden kehittymisessä, ja se viittaa siihen, että kumulatiivinen altistuminen joillekin mikro -organismeille voi vaikuttaa sairauden kehittymiseen [213–216 ].
Hiljattain tehty tutkimus vahvisti, että samamunaisten identtisten kaksosten konkordanssi on 40% tai vähemmän. Thähn yhdenmukaisuuden asteeseen vaikuttivat ympäristötekijät [217].
MS-taudin tutkimiseen käytetään useita erilaisia jyrsijöiden demyelinaatiomalleja, jotka eivät ole identtisiä ihmisen sairauden kanssa. Suurimmat tartuntamallit hiirillä ovat Theilerin hiiren enkefalomyeliittivirus (TMEV), hiiren hepatiittivirus (MHV) ja Semliki Forest -virus (SFV).
Jokaisella on erilliset immunopatologiset mekanismit ja ne kuvaavat erilaisia mahdollisia tapoja, joilla patogeenit voivat indusoida MS -taudin. On olemassa kaksi TMEV-kantaa (TMEV-DA ja TMEV-BeAn), jotka aiheuttavat ensimmäisen akuutin harmaan aineen taudin, jota seuraa krooninen etenevä demyelinaatio selkärangan valkoisessa aineessa. Tämä tunnetaan nimellä TMEV-indusoitu demyelinoiva sairaus (TMEV-IDD) [ 205 218 219].
Vaikka nämä kaksi kantaa aiheuttavat hieman erilaisia sairauksia, TMEV-IDD:n keskeiset ominaisuudet (epänormaali kävely ja spastinen raajan halvaus) pysyvät samoina. Aivonsisäinen (i.c.) viruksen injektio johtaa jatkuvaan keskushermostotulehdukseen; tarttuvan viruksen taso on alhainen kroonisen vaiheen aikana, mutta runsaasti RNA:ta ja virusantigeeniä voidaan havaita koko hiiren elinkaaren ajan [220–222].
Immuunivaste käynnistyy esittämällä pysyviä virusantigeenejä keskushermostossa sijaitsevissa APC-soluissa Th1-tyypin CD4+ T-soluille, mutta reaktiivisuus myeliinille ilmenee vasta kliinisten oireiden ilmaantumisen jälkeen (30–35 päivää infektion jälkeen) [223 –226]. Siten TMEV-IDD johtuu epitoopin leviämisestä viruksen determinantteista oman myeliinin determinantteihin.
Mielenkiintoista on, että SJL-hiirillä reaktiivisuus vaikuttaa useisiin myeliinipeptideihin, jotka alkavat immunodominantti-epitoopista ja leviävät myöhempinä ajankohtina muihin hallitseviin myeliinin determinantteihin hierarkkisesti [226, 227]. Toisin kuin TMEV, hiirillä, joihin on siirrostettu neurotrooppisia MHV -kantoja, tulee yksi merkittävä oireinen jakso (ataksia, takaraajan pareesi, halvaus), josta suurin osa toipuu [228].
Keskushermostotulehdus johtaa immuunisolujen tuloon, joka suurelta osin poistaa viruksen, vaikka pieniä määriä viruksia säilyy [229].
Demyelinaatio alkaa noin viikon kuluttua infektiosta ja saavuttaa huippunsa viikolla 3, minkä jälkeen leesioiden korjaus ja remyelinaatio yleensä tapahtuvat [230–232].
Tarkka demyelinaatiomekanismi tässä mallissa on jonkin verran kiistanalainen, mutta on viitteitä siitä, että mallissa aiheutuu (sivullisen) myeliinin tuhoutumista immuunivasteella, jonka tarkoitus keskushermostossa on virusinfektion hillitseminen.
MHV-tartunnan saaneiden hiirten keskushermostossa ei havaittu todisteita itsespesifisestä immuniteetista [233].
T- ja B-solu-vajavaisilta RAG1-/-hiiriltä, jotka olivat resistenttejä demyelinaatiolle, kehittyi histologinen sairaus [ 234].
Kemokiinireseptorin knock-out-hiiret (CCR5-/-) osoittivat vähentynyttä demyelinaatiota, joka korreloi vähentyneiden makrofagien kanssa. T-solujen tunkeutumista MHV-tartunnan saaneiden hiirten keskushermostoon ei havaittu [235]. CD4-rajoitetuilla hiirillä oli vähemmän vakava sairaus kuin CD8-rajoitetuilla hiirillä [236 237].
Yhteenveto ja ajatuksia
Immuunijärjestelmä on kehittänyt menetelmiä estääkseen isäntäkudoksen tuhoutumisen. Ei ole yllättävää, että vahva immuunivaste voi häiritä tätä tasapainoa ja johtaa autoimmuunreaktioon.
On olemassa merkittäviä todisteita siitä, että erilaiset patogeeniluokat (bakteerit, virukset ja loiset) osallistuvat autoreaktiivisten immuunivasteiden käynnistämiseen tai lisäämiseen. Todisteet infektion aiheuttaman autoimmuuniteetin lopullisesta yhteydestä ovat kuitenkin vahvempia tietyissä sairauksissa kuin toisissa.
Väite infektion aiheuttamasta patologiasta on paljon vahvempi sairauksissa, jotka liittyvät yhteen tai kahteen erityiseen patogeeniin kuin sairauksissa, joilla on useita syy-yhteyksiä.
Esimerkiksi se, että C. jejuni -infektio on yleinen GBS:n edeltäjä, on vahva näyttö siitä, että tämä tauti on infektion aiheuttama. Sitä vastoin sairauksien, kuten tyypin 1 diabetekseen ja MS-tautiin on liitetty kymmeniä patogeenejä, näyttö ei ole lainkaan yksiselitteinen.
Kaikkein vakuuttavin todiste olisi oireiden katoaminen infektion poistumisen myötä. Tämä koskee Lymen tautia, jossa antibioottihoito lievittää akuuttia niveltulehdusta. Kuitenkin, kuten aiemmin tässä artikkelissa esitettiin, on monia tapoja, joilla taudinaiheuttaja voi aiheuttaa taudin myös sen jälkeen, kun infektio on poistettu.
Tapauksissa, joissa epidemiologiset tutkimukset osoittavat, että tietyllä osalla tartunnan saaneista ihmisistä on suurempi autimmuunitautien esiintyvyys verrattuna ihmisiin, jotka eivät ole saaneet tartuntaa, vahvistavat infektion aiheuttamaa autoimmuunisuoja-argumenttia.
Vaikka yhteys S. pyogenes -infektion ja ihmisten neurologisten häiriöiden välillä on epävarma, se että S. pyogenes -homogenaatilla alustetuille hiirille kehittyy liike- ja käyttäytymishäiriöitä, lisää mallin uskottavuutta.
Tapauksissa, joissa on epävarmaa, onko sairauspatologia todella autoimmuuni (kuten uveiitti ja sydänlihastulehdus CVB -infektion jälkeen), eläinmalleilla on ollut ratkaiseva rooli sairauden indusoinnin mahdollisten mekanismien selvittämisessä.
Tietojen puutteet voi olla kyseessä tapauksissa, joissa todisteet infektion ja autoimmuuniteetin yhteydestä ovat vähäisiä tai ristiriitaisia. Toiset ihmiset voivat olla alttiimpia autoimmuunitaudeille tietyn infektion jälkeen kuin toiset. Jäljittelevät peptidit, jotka ovat peräisin eri tartunta -aineista, voivat saada aikaan tietyn autoimmuunisairauden riippuen tartunnan saaneen yksilön kyvystä esittää erilaisia epitooppeja eri HLA -molekyyliensä yhteydessä.
Näyttö COVID-19 potentiaalisista pitkäaikaisoireista lisääntyy jatkuvasti. Jo nyt tiedetään, että se voi aiheuttaa pitkäkestoisia neurologisia, psykologisia ja kognitiivisia oireita. Pysykää terveinä! Iloista alkavaa syksyä.
Viitteet
1. Selgrade MK, Cooper GS, Germolec DR, Heindel JJ. Linking environmental agents and autoimmune disease: an agenda for future research. Environ Health Perspect. 1999;107(Suppl. 5):811–3. [PMC free article] [PubMed] [Google Scholar]
2. Woodruff JF. Viral myocarditis. Am J Pathol. 1980;101:425–84. A review. [PMC free article] [PubMed] [Google Scholar]
3. Bowles NE, Richardson PJ, Olsen EG, Archard LC. Detection of Coxsackie-B-virus-specific RNA sequences in myocardial biopsy samples from patients with myocarditis and dilated cardiomyopathy. Lancet. 1986;1:1120–3. [PubMed] [Google Scholar]
4. Pauschinger M, Doerner A, Kuehl U, et al. Enteroviral RNA replication in the myocardium of patients with left ventricular dysfunction and clinically suspected myocarditis. Circulation. 1999;99:889–95. [PubMed] [Google Scholar]
5. Fairweather D, Kaya Z, Shellam GR, Lawson CM, Rose NR. From infection to autoimmunity. J Autoimmun. 2001;16:175–86. [PubMed] [Google Scholar]
6. Herzum M, Ruppert V, Kuytz B, Jomaa H, Nakamura I, Maisch B. Coxsackievirus B3 infection leads to cell death of cardiac myocytes. J Mol Cell Cardiol. 1994;26:907–13. [PubMed] [Google Scholar]
7. McManus BM, Chow LH, Wilson JE, et al. Direct myocardial injury by enterovirus: a central role in the evolution of murine myocarditis. Clin Immunol Immunopathol. 1993;68:159–69. [PubMed] [Google Scholar]
8. Chow LH, Beisel KW, McManus BM. Enteroviral infection of mice with severe combined immunodeficiency. Lab Invest. 1992;66:24–31. Evidence for direct viral pathogenesis of myocardial injury. [PubMed] [Google Scholar]
9. Si X, Wang Y, Wong J, Zhang J, McManus BM, Luo H. Dysregulation of the ubiquitin–proteasome system by curcumin suppresses coxsackievirus B3 replication. J Virol. 2007;81:3142–50. [PMC free article] [PubMed] [Google Scholar]
10. Luo H, Zhang J, Cheung C, Suarez A, McManus BM, Yang D. Proteasome inhibition reduces coxsackievirus B3 replication in murine cardiomyocytes. Am J Pathol. 2003;163:381–5. [PMC free article] [PubMed] [Google Scholar]
11. Luo H, Zhang J, Dastvan F, et al. Ubiquitin-dependent proteolysis of cyclin D1 is associated with coxsackievirus-induced cell growth arrest. J Virol. 2003;77:1–9. [PMC free article] [PubMed] [Google Scholar]
12. Woodruff JF, Woodruff JJ. Involvement of T lymphocytes in the pathogenesis of coxsackie virus B3 heart disease. J Immunol. 1974;113:1726–34. [PubMed] [Google Scholar]
13. Hashimoto I, Komatsu T. Myocardial changes after infection with Coxsackie virus B3 in nude mice. Br J Exp Pathol. 1978;59:13–20. [PMC free article] [PubMed] [Google Scholar]
14. Guthrie M, Lodge PA, Huber SA. Cardiac injury in myocarditis induced by Coxsackievirus group B, type 3 in Balb/c mice is mediated by Lyt 2 + cytolytic lymphocytes. Cell Immunol. 1984;88:558–67. [PubMed] [Google Scholar]
15. Huber SA. Coxsackievirus-induced myocarditis is dependent on distinct immunopathogenic responses in different strains of mice. Lab Invest. 1997;76:691–701. [PubMed] [Google Scholar]
16. Henke A, Huber S, Stelzner A, Whitton JL. The role of CD8+ T lymphocytes in coxsackievirus B3-induced myocarditis. J Virol. 1995;69:6720–8. [PMC free article] [PubMed] [Google Scholar]
17. Gauntt CJ, Arizpe HM, Higdon AL, et al. Molecular mimicry, anti-coxsackievirus B3 neutralizing monoclonal antibodies, and myocarditis. J Immunol. 1995;154:2983–95. [PubMed] [Google Scholar]
18. Gauntt CJ, Higdon AL, Arizpe HM, et al. Epitopes shared between coxsackievirus B3 (CVB3) and normal heart tissue contribute to CVB3-induced murine myocarditis. Clin Immunol Immunopathol. 1993;68:129–34. [PubMed] [Google Scholar]
19. Huber SA. Autoimmunity in myocarditis: relevance of animal models. Clin Immunol Immunopathol. 1997;83:93–102. [PubMed] [Google Scholar]
20. Huber SA, Moraska A, Cunningham M. Alterations in major histocompatibility complex association of myocarditis induced by coxsackievirus B3 mutants selected with monoclonal antibodies to group A streptococci. Proc Natl Acad Sci USA. 1994;91:5543–7. [PMC free article] [PubMed] [Google Scholar]
21. Rose NR, Hill SL. The pathogenesis of postinfectious myocarditis. Clin Immunol Immunopathol. 1996;80:S92–9. [PubMed] [Google Scholar]
22. Tam PE, Fontana DR, Messner RP. Coxsackievirus B1-induced chronic inflammatory myopathy: differences in induction of autoantibodies to muscle and nuclear antigens by cloned myopathic and amyopathic viruses. J Lab Clin Med. 2003;142:196–204. [PubMed] [Google Scholar]
23. Whitton JL, Feuer R. Myocarditis, microbes and autoimmunity. Autoimmunity. 2004;37:375–86. [PubMed] [Google Scholar]
24. Schwimmbeck PL, Bigalke B, Schulze K, Pauschinger M, Kuhl U, Schultheiss HP. The humoral immune response in viral heart disease: characterization and pathophysiological significance of antibodies. Med Microbiol Immunol. 2004;193:115–9. [PubMed] [Google Scholar]
25. Bengtsson E, Birke G, Wingstrand H. Acute non-specific myocarditis in scarlet fever and acute haemolytic tonsillitis A clinical investigation of 3,069 cases of scarlet fever, 798 cases of acute tonsillitis, and 333 cases of haemolytic streptococcus carriers. Cardiologia. 1951;18:360–74. [PubMed] [Google Scholar]
26. Friedman I, Laufer A, Ron N, Davies AM. Experimental myocarditis: in vitro and in vivo studies of lymphocytes sensitized to heart extracts and group A streptococci. Immunology. 1971;20:225–32. [PMC free article] [PubMed] [Google Scholar]
27. Cunningham MW, McCormack JM, Talaber LR, et al. Human monoclonal antibodies reactive with antigens of the group A Streptococcus and human heart. J Immunol. 1988;141:2760–6. [PubMed] [Google Scholar]
28. Adderson EE, Shikhman AR, Ward KE, Cunningham MW. Molecular analysis of polyreactive monoclonal antibodies from rheumatic carditis: human anti-N-acetylglucosamine/anti-myosin antibody V region genes. J Immunol. 1998;161:2020–31. [PubMed] [Google Scholar]
29. Mertens NM, Galvin JE, Adderson EE, Cunningham MW. Molecular analysis of cross-reactive anti-myosin/anti-streptococcal mouse monoclonal antibodies. Mol Immunol. 2000;37:901–13. [PubMed] [Google Scholar]
30. Cunningham MW, McCormack JM, Fenderson PG, Ho MK, Beachey EH, Dale JB. Human and murine antibodies cross-reactive with streptococcal M protein and myosin recognize the sequence GLN-LYS-SER-LYS-GLN in M protein. J Immunol. 1989;143:2677–83. [PubMed] [Google Scholar]
31. Fenderson PG, Fischetti VA, Cunningham MW. Tropomyosin shares immunologic epitopes with group A streptococcal M proteins. J Immunol. 1989;142:2475–81. [PubMed] [Google Scholar]
32. Galvin JE, Hemric ME, Ward K, Cunningham MW. Cytotoxic mAb from rheumatic carditis recognizes heart valves and laminin. J Clin Invest. 2000;106:217–24. [PMC free article] [PubMed] [Google Scholar]
33. Ellis NM, Li Y, Hildebrand W, Fischetti VA, Cunningham MW. T cell mimicry and epitope specificity of cross-reactive T cell clones from rheumatic heart disease. J Immunol. 2005;175:5448–56. [PubMed] [Google Scholar]
34. Fae KC, da Silva DD, Oshiro SE, et al. Mimicry in recognition of cardiac myosin peptides by heart-intralesional T cell clones from rheumatic heart disease. J Immunol. 2006;176:5662–70. [PubMed] [Google Scholar]
35. Raizada V, Williams RC, Jr., Chopra P, et al. Tissue distribution of lymphocytes in rheumatic heart valves as defined by monoclonal anti-T cell antibodies. Am J Med. 1983;74:90–6. [PubMed] [Google Scholar]
36. Guilherme L, Oshiro SE, Fae KC, et al. T-cell reactivity against streptococcal antigens in the periphery mirrors reactivity of heart-infiltrating T lymphocytes in rheumatic heart disease patients. Infect Immun. 2001;69:5345–51. [PMC free article] [PubMed] [Google Scholar]
37. Cunningham MW, Antone SM, Smart M, Liu R, Kosanke S. Molecular analysis of human cardiac myosin-cross-reactive B- and T-cell epitopes of the group A streptococcal M5 protein. Infect Immun. 1997;65:3913–23. [PMC free article] [PubMed] [Google Scholar]
38. Quinn A, Kosanke S, Fischetti VA, Factor SM, Cunningham MW. Induction of autoimmune valvular heart disease by recombinant streptococcal m protein. Infect Immun. 2001;69:4072–8. [PMC free article] [PubMed] [Google Scholar]
39. Murphy GE, Swift HF. The induction of rheumatic-like cardiac lesions in rabbits by repeated focal infections with group A streptococci; comparison with the cardiac lesions of serum disease. J Exp Med. 1950;91:485–98. [PMC free article] [PubMed] [Google Scholar]
40. Cromartie WJ, Craddock JG. Rheumatic-like cardiac lesions in mice. Science. 1966;154:285–7. [PubMed] [Google Scholar]
41. Singer HS, Giuliano JD, Hansen BH, et al. Antibodies against human putamen in children with Tourette syndrome. Neurology. 1998;50:1618–24. [PubMed] [Google Scholar]
42. Pavone P, Bianchini R, Parano E, et al. Anti-brain antibodies in PANDAS versus uncomplicated streptococcal infection. Pediatr Neurol. 2004;30:107–10. [PubMed] [Google Scholar]
43. Kurlan R. Tourette’s syndrome and ‘PANDAS’: will the relation bear out? Pediatric autoimmune neuropsychiatric disorders associated with streptococcal infection. Neurology. 1998;50:1530–4. [PubMed] [Google Scholar]
44. Snider LA, Swedo SE. Post-streptococcal autoimmune disorders of the central nervous system. Curr Opin Neurol. 2003;16:359–65. [PubMed] [Google Scholar]
45. Bronze MS, Dale JB. Epitopes of streptococcal M proteins that evoke antibodies that cross-react with human brain. J Immunol. 1993;151:2820–8. [PubMed] [Google Scholar]
46. Husby G, van de Rijn I, Zabriskie JB, Abdin ZH, Williams RC., Jr. Antibodies reacting with cytoplasm of subthalamic and caudate nuclei neurons in chorea and acute rheumatic fever. J Exp Med. 1976;144:1094–110. [PMC free article] [PubMed] [Google Scholar]
47. Kirvan CA, Swedo SE, Heuser JS, Cunningham MW. Mimicry and autoantibody-mediated neuronal cell signaling in Sydenham chorea. Nat Med. 2003;9:914–20. [PubMed] [Google Scholar]
48. Kirvan CA, Swedo SE, Snider LA, Cunningham MW. Antibody-mediated neuronal cell signaling in behavior and movement disorders. J Neuroimmunol. 2006;179:173–9. [PubMed] [Google Scholar]
49. Kirvan CA, Cox CJ, Swedo SE, Cunningham MW. Tubulin is a neuronal target of autoantibodies in Sydenham’s chorea. J Immunol. 2007;178:7412–21. [PubMed] [Google Scholar]
50. Hoffman KL, Hornig M, Yaddanapudi K, Jabado O, Lipkin WI. A murine model for neuropsychiatric disorders associated with group A beta-hemolytic streptococcal infection. J Neurosci. 2004;24:1780–91. [PMC free article] [PubMed] [Google Scholar]
51. Soares MB, Santos RR. Immunopathology of cardiomyopathy in the experimental Chagas disease. Mem Inst Oswaldo Cruz. 1999;94(Suppl. 1):257–62. [PubMed] [Google Scholar]
52. Leon JS, Engman DM. The significance of autoimmunity in the pathogenesis of Chagas heart disease. Front Biosci. 2003;8:e315–22. [PubMed] [Google Scholar]
53. Cunha-Neto E, Bilate AM, Hyland KV, Fonseca SG, Kalil J, Engman DM. Induction of cardiac autoimmunity in Chagas heart disease: a case for molecular mimicry. Autoimmunity. 2006;39:41–54. [PubMed] [Google Scholar]
54. Sartori AM, Shikanai-Yasuda MA, Amato Neto V, Lopes MH. Follow-up of 18 patients with human immunodeficiency virus infection and chronic Chagas’ disease, with reactivation of Chagas’ disease causing cardiac disease in three patients. Clin Infect Dis. 1998;26:177–9. [PubMed] [Google Scholar]
55. Pereira JB, Wilcox HP, Coura JR. The evolution of chronic chagasic cardiopathy. Rev Soc Bras Med Trop. 1992;25:101–8. I. The influence of parasitemia. [PubMed] [Google Scholar]
56. Elias FE, Vigliano CA, Laguens RP, Levin MJ, Berek C. Analysis of the presence of Trypanosoma cruzi in the heart tissue of three patients with chronic Chagas’ heart disease. Am J Trop Med Hyg. 2003;68:242–7. [PubMed] [Google Scholar]
57. Higuchi ML, De Morais CF, Pereira Barreto AC, et al. The role of active myocarditis in the development of heart failure in chronic Chagas’ disease: a study based on endomyocardial biopsies. Clin Cardiol. 1987;10:665–70. [PubMed] [Google Scholar]
58. Abel LC, Rizzo LV, Ianni B, et al. Chronic Chagas’ disease cardiomyopathy patients display an increased IFN-gamma response to Trypanosoma cruzi infection. J Autoimmun. 2001;17:99–107. [PubMed] [Google Scholar]
59. Reis MM, Higuchi Mde L, Benvenuti LA, et al. An in situ quantitative immunohistochemical study of cytokines and IL-2R+ in chronic human chagasic myocarditis: correlation with the presence of myocardial Trypanosoma cruzi antigens. Clin Immunol Immunopathol. 1997;83:165–72. [PubMed] [Google Scholar]
60. Cunha-Neto E, Dzau VJ, Allen PD, et al. Cardiac gene expression profiling provides evidence for cytokinopathy as a molecular mechanism in Chagas’ disease cardiomyopathy. Am J Pathol. 2005;167:305–13. [PMC free article] [PubMed] [Google Scholar]
61. Teixeira AR, Teixeira G, Macedo V, Prata A. Trypanosoma cruzi-sensitized T-lymphocyte mediated 51CR release from human heart cells in Chagas’ disease. Am J Trop Med Hyg. 1978;27:1097–107. [PubMed] [Google Scholar]
62. Todd CW, Todd NR, Guimaraes AC. Do lymphocytes from Chagasic patients respond to heart antigens? Infect Immun. 1983;40:832–5. [PMC free article] [PubMed] [Google Scholar]
63. Mosca W, Plaja J, Hubsch R, Cedillos R. Longitudinal study of immune response in human Chagas’ disease. J Clin Microbiol. 1985;22:438–41. [PMC free article] [PubMed] [Google Scholar]
64. Gruber A, Zingales B. Trypanosoma cruzi: characterization of two recombinant antigens with potential application in the diagnosis of Chagas’ disease. Exp Parasitol. 1993;76:1–12. [PubMed] [Google Scholar]
65. Cunha-Neto E, Duranti M, Gruber A, et al. Autoimmunity in Chagas disease cardiopathy: biological relevance of a cardiac myosin-specific epitope crossreactive to an immunodominant Trypanosoma cruzi antigen. Proc Natl Acad Sci USA. 1995;92:3541–5. [PMC free article] [PubMed] [Google Scholar]
66. Cunha-Neto E, Coelho V, Guilherme L, Fiorelli A, Stolf N, Kalil J. Autoimmunity in Chagas’ disease. J Clin Invest. 1996;98:1709–12. Identification of cardiac myosin-B13 Trypanosoma cruzi protein crossreactive T cell clones in heart lesions of a chronic Chagas’ cardiomyopathy patient. [PMC free article] [PubMed] [Google Scholar]
67. Abel LC, Kalil J, Cunha Neto E. Molecular mimicry between cardiac myosin and Trypanosoma cruzi antigen B13: identification of a B13-driven human T cell clone that recognizes cardiac myosin. Braz J Med Biol Res. 1997;30:1305–8. [PubMed] [Google Scholar]
68. Lannes-Vieira J. Trypanosoma cruzi-elicited CD8+ T cell-mediated myocarditis: chemokine receptors and adhesion molecules as potential therapeutic targets to control chronic inflammation? Mem Inst Oswaldo Cruz. 2003;98:299–304. [PubMed] [Google Scholar]
69. Rizzo LV, Cunha-Neto E, Teixeira AR. Autoimmunity in Chagas’ disease: specific inhibition of reactivity of CD4+ T cells against myosin in mice chronically infected with Trypanosoma cruzi. Infect Immun. 1989;57:2640–4. [PMC free article] [PubMed] [Google Scholar]
70. dos Santos RR, Rossi MA, Laus JL, Silva JS, Savino W, Mengel J. Anti-CD4 abrogates rejection and reestablishes long-term tolerance to syngeneic newborn hearts grafted in mice chronically infected with Trypanosoma cruzi. J Exp Med. 1992;175:29–39. [PMC free article] [PubMed] [Google Scholar]
71. Ribeiro-Dos-Santos R, Mengel JO, Postol E, et al. A heart-specific CD4+ T-cell line obtained from a chronic chagasic mouse induces carditis in heart-immunized mice and rejection of normal heart transplants in the absence of Trypanosoma cruzi. Parasite Immunol. 2001;23:93–101. [PubMed] [Google Scholar]
72. Girones N, Rodriguez CI, Carrasco-Marin E, Hernaez RF, de Rego JL, Fresno M. Dominant T- and B-cell epitopes in an autoantigen linked to Chagas’ disease. J Clin Invest. 2001;107:985–93. [PMC free article] [PubMed] [Google Scholar]
73. Oliveira MF, Bijovsky AT, Carvalho TU, de Souza W, Alves MJ, Colli W. A monoclonal antibody to Trypanosoma cruzi trypomastigotes recognizes a myosin tail epitope. Parasitol Res. 2001;87:1043–9. [PubMed] [Google Scholar]
74. Giordanengo L, Guinazu N, Stempin C, Fretes R, Cerban F, Gea S. Cruzipain, a major Trypanosoma cruzi antigen, conditions the host immune response in favor of parasite. Eur J Immunol. 2002;32:1003–11. [PubMed] [Google Scholar]
75. McCormick TS, Rowland EC. Trypanosoma cruzi: cross-reactive anti-heart autoantibodies produced during infection in mice. Exp Parasitol. 1989;69:393–401. [PubMed] [Google Scholar]
76. Leon JS, Daniels MD, Toriello KM, Wang K, Engman DM. A cardiac myosin-specific autoimmune response is induced by immunization with Trypanosoma cruzi proteins. Infect Immun. 2004;72:3410–7. [PMC free article] [PubMed] [Google Scholar]
77. Leon JS, Godsel LM, Wang K, Engman DM. Cardiac myosin autoimmunity in acute Chagas’ heart disease. Infect Immun. 2001;69:5643–9. [PMC free article] [PubMed] [Google Scholar]
78. Meneghelli UG. Chagasic enteropathy. Rev Soc Bras Med Trop. 2004;37:252–60. [PubMed] [Google Scholar]
79. Van Voorhis WC, Eisen H. FL-160: a surface antigen of Trypanosoma cruzi that mimics mammalian nervous tissue. J Exp Med. 1989;169:641–52. [PMC free article] [PubMed] [Google Scholar]
80. Van Voorhis WC, Barrett L, Koelling R, Farr AG. FL-160 proteins of Trypanosoma cruzi are expressed from a multigene family and contain two distinct epitopes that mimic nervous tissues. J Exp Med. 1993;178:681–94. [PMC free article] [PubMed] [Google Scholar]
81. Van Voorhis WC, Schlekewy L, Trong HL. Molecular mimicry by Trypanosoma cruzi: the F1-160 epitope that mimics mammalian nerve can be mapped to a 12-amino acid peptide. Proc Natl Acad Sci USA. 1991;88:5993–7. [PMC free article] [PubMed] [Google Scholar]
82. Petry K, Eisen H. Chemical characterization of epitopes common to Trypanosoma cruzi and mammalian nervous cells. Mem Inst Oswaldo Cruz. 1988;83(Suppl. 1):498–501. [PubMed] [Google Scholar]
83. Gea S, Ordonez P, Cerban F, Iosa D, Chizzolini C, Vottero-Cima E. Chagas’ disease cardioneuropathy: association of anti-Trypanosoma cruzi and anti-sciatic nerve antibodies. Am J Trop Med Hyg. 1993;49:581–8. [PubMed] [Google Scholar]
84. Steere AC, Schoen RT, Taylor E. The clinical evolution of Lyme arthritis. Ann Intern Med. 1987;107:725–31. [PubMed] [Google Scholar]
85. Nocton JJ, Dressler F, Rutledge BJ, Rys PN, Persing DH, Steere AC. Detection of Borrelia burgdorferi DNA by polymerase chain reaction in synovial fluid from patients with Lyme arthritis. N Engl J Med. 1994;330:229–34. [PubMed] [Google Scholar]
86. Steere AC, Levin RE, Molloy PJ, Kalish RA, Abraham JH, 3rd, Liu NY, Schmid CH. Treatment of Lyme arthritis. Arthritis Rheum. 1994;37:878–88. [PubMed] [Google Scholar]
87. Carlson D, Hernandez J, Bloom BJ, Coburn J, Aversa JM, Steere AC. Lack of Borrelia burgdorferi DNA in synovial samples from patients with antibiotic treatment-resistant Lyme arthritis. Arthritis Rheum. 1999;42:2705–9. [PubMed] [Google Scholar]
88. Malawista SE. Resolution of Lyme arthritis, acute or prolonged: a new look. Inflammation. 2000;24:493–504. [PubMed] [Google Scholar]
89. Chen J, Field JA, Glickstein L, Molloy PJ, Huber BT, Steere AC. Association of antibiotic treatment-resistant Lyme arthritis with T cell responses to dominant epitopes of outer surface protein A of Borrelia burgdorferi. Arthritis Rheum. 1999;42:1813–22. [PubMed] [Google Scholar]
90. Lengl-Janssen B, Strauss AF, Steere AC, Kamradt T. The T helper cell response in Lyme arthritis: differential recognition of Borrelia burgdorferi outer surface protein A in patients with treatment-resistant or treatment-responsive Lyme arthritis. J Exp Med. 1994;180:2069–78. [PMC free article] [PubMed] [Google Scholar]
91. Kalish RA, Leong JM, Steere AC. Association of treatment-resistant chronic Lyme arthritis with HLA-DR4 and antibody reactivity to OspA and OspB of Borrelia burgdorferi. Infect Immun. 1993;61:2774–9. [PMC free article] [PubMed] [Google Scholar]
92. Kalish RA, Leong JM, Steere AC. Early and late antibody responses to full-length and truncated constructs of outer surface protein A of Borrelia burgdorferi in Lyme disease. Infect Immun. 1995;63:2228–35. [PMC free article] [PubMed] [Google Scholar]
93. Akin E, McHugh GL, Flavell RA, Fikrig E, Steere AC. The immunoglobulin (IgG) antibody response to OspA and OspB correlates with severe and prolonged Lyme arthritis and the IgG response to P35 correlates with mild and brief arthritis. Infect Immun. 1999;67:173–81. [PMC free article] [PubMed] [Google Scholar]
94. Meyer AL, Trollmo C, Crawford F, et al. Direct enumeration of Borrelia-reactive CD4 T cells ex vivo by using MHC class II tetramers. Proc Natl Acad Sci USA. 2000;97:11433–8. [PMC free article] [PubMed] [Google Scholar]
95. Steere AC, Gross D, Meyer AL, Huber BT. Autoimmune mechanisms in antibiotic treatment-resistant lyme arthritis. J Autoimmun. 2001;16:263–8. [PubMed] [Google Scholar]
96. Gross DM, Forsthuber T, Tary-Lehmann M, et al. Identification of LFA-1 as a candidate autoantigen in treatment-resistant Lyme arthritis. Science. 1998;281:703–6. [PubMed] [Google Scholar]
97. Akin E, Aversa J, Steere AC. Expression of adhesion molecules in synovia of patients with treatment-resistant lyme arthritis. Infect Immun. 2001;69:1774–80. [PMC free article] [PubMed] [Google Scholar]
98. Trollmo C, Meyer AL, Steere AC, Hafler DA, Huber BT. Molecular mimicry in Lyme arthritis demonstrated at the single cell level: LFA-1 alpha L is a partial agonist for outer surface protein A-reactive T cells. J Immunol. 2001;166:5286–91. [PubMed] [Google Scholar]
99. Steere AC, Falk B, Drouin EE, Baxter-Lowe LA, Hammer J, Nepom GT. Binding of outer surface protein A and human lymphocyte function-associated antigen 1 peptides to HLA-DR molecules associated with antibiotic treatment-resistant Lyme arthritis. Arthritis Rheum. 2003;48:534–40. [PubMed] [Google Scholar]
100. Kalish RS, Wood JA, Golde W, et al. Human T lymphocyte response to Borrelia burgdorferi infection: no correlation between human leukocyte function antigen type 1 peptide response and clinical status. J Infect Dis. 2003;187:102–8. [PubMed] [Google Scholar]
101. Maier B, Molinger M, Cope AP, et al. Multiple cross-reactive self-ligands for Borrelia burgdorferi-specific HLA-DR4-restricted T cells. Eur J Immunol. 2000;30:448–57. [PubMed] [Google Scholar]
102. Barthold SW, Moody KD, Terwilliger GA, Duray PH, Jacoby RO, Steere AC. Experimental Lyme arthritis in rats infected with Borrelia burgdorferi. J Infect Dis. 1988;157:842–6. [PubMed] [Google Scholar]
103. Barthold SW, Beck DS, Hansen GM, Terwilliger GA, Moody KD. Lyme borreliosis in selected strains and ages of laboratory mice. J Infect Dis. 1990;162:133–8. [PubMed] [Google Scholar]
104. Ma Y, Seiler KP, Eichwald EJ, Weis JH, Teuscher C, Weis JJ. Distinct characteristics of resistance to Borrelia burgdorferi-induced arthritis in C57BL/6N mice. Infect Immun. 1998;66:161–8. [PMC free article] [PubMed] [Google Scholar]
105. Schaible UE, Kramer MD, Museteanu C, Zimmer G, Mossmann H, Simon MM. The severe combined immunodeficiency (scid) mouse. A laboratory model for the analysis of Lyme arthritis and carditis. J Exp Med. 1989;170:1427–32. [PMC free article] [PubMed] [Google Scholar]
106. Barthold SW, de Souza M. Exacerbation of Lyme arthritis in beige mice. J Infect Dis. 1995;172:778–84. [PubMed] [Google Scholar]
107. Anguita J, Rincon M, Samanta S, Barthold SW, Flavell RA, Fikrig E. Borrelia burgdorferi-infected, interleukin-6-deficient mice have decreased Th2 responses and increased lyme arthritis. J Infect Dis. 1998;178:1512–5. [PubMed] [Google Scholar]
108. Brown JP, Zachary JF, Teuscher C, Weis JJ, Wooten RM. Dual role of interleukin-10 in murine Lyme disease: regulation of arthritis severity and host defense. Infect Immun. 1999;67:5142–50. [PMC free article] [PubMed] [Google Scholar]
109. McKisic MD, Redmond WL, Barthold SW. Cutting edge: T cell-mediated pathology in murine Lyme borreliosis. J Immunol. 2000;164:6096–9. [PubMed] [Google Scholar]
110. Sigal LH. Lyme disease: a review of aspects of its immunology and immunopathogenesis. Annu Rev Immunol. 1997;15:63–92. [PubMed] [Google Scholar]
111. Sigal LH, Tatum AH. Lyme disease patients’ serum contains IgM antibodies to Borrelia burgdorferi that cross-react with neuronal antigens. Neurology. 1988;38:1439–42. [PubMed] [Google Scholar]
112. Wang WZ, Fredrikson S, Sun JB, Link H. Lyme neuroborreliosis: evidence for persistent up-regulation of Borrelia burgdorferi-reactive cells secreting interferon-gamma. Scand J Immunol. 1995;42:694–700. [PubMed] [Google Scholar]
113. Garcia-Monco JC, Coleman JL, Benach JL. Antibodies to myelin basic protein in Lyme disease. J Infect Dis. 1988;158:667–8. [PubMed] [Google Scholar]
114. Sigal LH. Cross-reactivity between Borrelia burgdorferi flagellin and a human axonal 64,000 molecular weight protein. J Infect Dis. 1993;167:1372–8. [PubMed] [Google Scholar]
115. Dai Z, Lackland H, Stein S, et al. Molecular mimicry in Lyme disease: monoclonal antibody H9724 to B. Biochim Biophys Acta. 1993;1181:97–100. burgdorferi flagellin specifically detects chaperonin-HSP60. [PubMed] [Google Scholar]
116. Fikrig E, Berland R, Chen M, Williams S, Sigal LH, Flavell RA. Serologic response to the Borrelia burgdorferi flagellin demonstrates an epitope common to a neuroblastoma cell line. Proc Natl Acad Sci USA. 1993;90:183–7. [PMC free article] [PubMed] [Google Scholar]
117. Sigal LH, Williams S. A monoclonal antibody to Borrelia burgdorferi flagellin modifies neuroblastoma cell neuritogenesis in vitro: a possible role for autoimmunity in the neuropathy of Lyme disease. Infect Immun. 1997;65:1722–8. [PMC free article] [PubMed] [Google Scholar]
118. Alaedini A, Latov N. Antibodies against OspA epitopes of Borrelia burgdorferi cross-react with neural tissue. J Neuroimmunol. 2005;159:192–5. [PubMed] [Google Scholar]
119. Hemmer B, Gran B, Zhao Y, et al. Identification of candidate T-cell epitopes and molecular mimics in chronic Lyme disease. Nat Med. 1999;5:1375–82. [PubMed] [Google Scholar]
120. Pachner AR, Cadavid D, Shu G, et al. Central and peripheral nervous system infection, immunity, and inflammation in the NHP model of Lyme borreliosis. Ann Neurol. 2001;50:330–8. [PubMed] [Google Scholar]
121. Ramesh G, Alvarez AL, Roberts ED, et al. Pathogenesis of Lyme neuroborreliosis: Borrelia burgdorferi lipoproteins induce both proliferation and apoptosis in rhesus monkey astrocytes. Eur J Immunol. 2003;33:2539–50. [PubMed] [Google Scholar]
122. Steiner I. Treating post Lyme disease: trying to solve one equation with too many unknowns. Neurology. 2003;60:1888–9. [PubMed] [Google Scholar]
123. Liesegang TJ. Epidemiology of ocular herpes simplex. Arch Ophthalmol. 1989;107:1160–5. Natural history in Rochester, Minn, 1950 through 1982. [PubMed] [Google Scholar]
124. Liesegang TJ. Classification of herpes simplex virus keratitis and anterior uveitis. Cornea. 1999;18:127–43. [PubMed] [Google Scholar]
125. Heiligenhaus A, Steuhl KP. Treatment of HSV-1 stromal keratitis with topical cyclosporin A: a pilot study. Graefes Arch Clin Exp Ophthalmol. 1999;237:435–8. [PubMed] [Google Scholar]
126. Fenton RR, Molesworth-Kenyon S, Oakes JE, Lausch RN. Linkage of IL-6 with neutrophil chemoattractant expression in virus-induced ocular inflammation. Invest Ophthalmol Vis Sci. 2002;43:737–43. [PubMed] [Google Scholar]
127. Lausch RN, Chen SH, Tumpey TM, Su YH, Oakes JE. Early cytokine synthesis in the excised mouse cornea. J Interferon Cytokine Res. 1996;16:35–40. [PubMed] [Google Scholar]
128. Staats HF, Lausch RN. Cytokine expression in vivo during murine herpetic stromal keratitis. Effect of protective antibody therapy. J Immunol. 1993;151:277–83. [PubMed] [Google Scholar]
129. Tumpey TM, Chen SH, Oakes JE, Lausch RN. Neutrophil-mediated suppression of virus replication after herpes simplex virus type 1 infection of the murine cornea. J Virol. 1996;70:898–904. [PMC free article] [PubMed] [Google Scholar]
130. Thomas J, Gangappa S, Kanangat S, Rouse BT. On the essential involvement of neutrophils in the immunopathologic disease: herpetic stromal keratitis. J Immunol. 1997;158:1383–91. [PubMed] [Google Scholar]
131. Hendricks RL, Tumpey TM, Finnegan A. IFN-gamma and IL-2 are protective in the skin but pathologic in the corneas of HSV-1-infected mice. J Immunol. 1992;149:3023–8. [PubMed] [Google Scholar]
132. Bauer D, Mrzyk S, Van Rooijen N, Steuhl KP, Heiligenhaus A. Incidence and severity of herpetic stromal keratitis: impaired by the depletion of lymph node macrophages. Exp Eye Res. 2001;72:261–9. [PubMed] [Google Scholar]
133. Habu S, Akamatsu K, Tamaoki N, Okumura K. In vivo significance of NK cell on resistance against virus (HSV-1) infections in mice. J Immunol. 1984;133:2743–7. [PubMed] [Google Scholar]
134. Zisman B, Hirsch MS, Allison AC. Selective effects of anti-macrophage serum, silica and anti-lymphocyte serum on pathogenesis of herpes virus infection of young adult mice. J Immunol. 1970;104:1155–9. [PubMed] [Google Scholar]
135. Bouley DM, Kanangat S, Wire W, Rouse BT. Characterization of herpes simplex virus type-1 infection and herpetic stromal keratitis development in IFN-gamma knockout mice. J Immunol. 1995;155:3964–71. [PubMed] [Google Scholar]
136. Tang Q, Hendricks RL. Interferon gamma regulates platelet endothelial cell adhesion molecule 1 expression and neutrophil infiltration into herpes simplex virus-infected mouse corneas. J Exp Med. 1996;184:1435–47. [PMC free article] [PubMed] [Google Scholar]
137. Streilein JW, Dana MR, Ksander BR. Immunity causing blindness: five different paths to herpes stromal keratitis. Immunol Today. 1997;18:443–9. [PubMed] [Google Scholar]
138. Halford WP, Gebhardt BM, Carr DJ. Persistent cytokine expression in trigeminal ganglion latently infected with herpes simplex virus type 1. J Immunol. 1996;157:3542–9. [PubMed] [Google Scholar]
139. Gangappa S, Babu JS, Thomas J, Daheshia M, Rouse BT. Virus-induced immunoinflammatory lesions in the absence of viral antigen recognition. J Immunol. 1998;161:4289–300. [PubMed] [Google Scholar]
140. Maggs DJ, Chang E, Nasisse MP, Mitchell WJ. Persistence of herpes simplex virus type 1 DNA in chronic conjunctival and eyelid lesions of mice. J Virol. 1998;72:9166–72. [PMC free article] [PubMed] [Google Scholar]
141. Lundberg P, Welander P, Han X, Cantin E. Herpes simplex virus type 1 DNA is immunostimulatory in vitro and in vivo. J Virol. 2003;77:11158–69. [PMC free article] [PubMed] [Google Scholar]
142. Zhao ZS, Granucci F, Yeh L, Schaffer PA, Cantor H. Molecular mimicry by herpes simplex virus-type 1: autoimmune disease after viral infection. Science. 1998;279:1344–7. [PubMed] [Google Scholar]
143. Panoutsakopoulou V, Sanchirico ME, Huster KM, et al. Analysis of the relationship between viral infection and autoimmune disease. Immun. 2001;15:137–47. [PubMed] [Google Scholar]
144. Verjans GM, Remeijer L, Mooy CM, Osterhaus AD. Herpes simplex virus-specific T cells infiltrate the cornea of patients with herpetic stromal keratitis: no evidence for autoreactive T cells. Invest Ophthalmol Vis Sci. 2000;41:2607–12. [PubMed] [Google Scholar]
145. Koelle DM, Reymond SN, Chen H, et al. Tegument-specific, virus-reactive CD4 T cells localize to the cornea in herpes simplex virus interstitial keratitis in humans. J Virol. 2000;74:10930–8. [PMC free article] [PubMed] [Google Scholar]
146. Babu JS, Thomas J, Kanangat S, Morrison LA, Knipe DM, Rouse BT. Viral replication is required for induction of ocular immunopathology by herpes simplex virus. J Virol. 1996;70:101–7. [PMC free article] [PubMed] [Google Scholar]
147. Durrani OM, Meads CA, Murray PI. Uveitis: a potentially blinding disease. Ophthalmologica. 2004;218:223–36. [PubMed] [Google Scholar]
148. Martin TM, Kurz DE, Rosenbaum JT. Genetics of uveitis. Ophthalmol Clin North Am. 2003;16:555–65. [PubMed] [Google Scholar]
149. de Smet MD, Yamamoto JH, Mochizuki M, et al. Cellular immune responses of patients with uveitis to retinal antigens and their fragments. Am J Ophthalmol. 1990;110:135–42. [PubMed] [Google Scholar]
150. Doekes G, van der Gaag R, Rothova A, et al. Humoral and cellular immune responsiveness to human S-antigen in uveitis. Curr Eye Res. 1987;6:909–19. [PubMed] [Google Scholar]
151. Singh VK, Yamaki K, Abe T, Shinohara T. Molecular mimicry between uveitopathogenic site of retinal S-antigen and Escherichia coli protein: induction of experimental autoimmune uveitis and lymphocyte cross-reaction. Cell Immunol. 1989;122:262–73. [PubMed] [Google Scholar]
152. Singh VK, Kalra HK, Yamaki K, Abe T, Donoso LA, Shinohara T. Molecular mimicry between a uveitopathogenic site of S-antigen and viral peptides. J Immunol. 1990;144:1282–7. Induction of experimental autoimmune uveitis in Lewis rats. [PubMed] [Google Scholar]
153. Wildner G, Diedrichs-Mohring M. Autoimmune uveitis induced by molecular mimicry of peptides from rotavirus, bovine casein and retinal S-antigen. Eur J Immunol. 2003;33:2577–87. [PubMed] [Google Scholar]
154. Lashkevich VA, Koroleva GA, Lukashev AN, Denisova EV, Katargina LA. Enterovirus uveitis. Rev Med Virol. 2004;14:241–54. [PubMed] [Google Scholar]
155. Kaprio J, Tuomilehto J, Koskenvuo M, et al. Concordance for type 1 (insulin-dependent) and type 2 (non-insulin-dependent) diabetes mellitus in a population-based cohort of twins in Finland. Diabetologia. 1992;35:1060–7. [PubMed] [Google Scholar]
156. Kyvik KO, Green A, Beck-Nielsen H. Concordance rates of insulin dependent diabetes mellitus: a population based study of young Danish twins. BMJ. 1995;311:913–7. [PMC free article] [PubMed] [Google Scholar]
157. Jun HS, Yoon JW. A new look at viruses in type 1 diabetes. Diabetes Metab Res Rev. 2003;19:8–31. [PubMed] [Google Scholar]
158. McIntosh ED, Menser MA. A fifty-year follow-up of congenital rubella. Lancet. 1992;340:414–5. [PubMed] [Google Scholar]
159. Ginsberg-Fellner F, Witt ME, Yagihashi S, et al. Congenital rubella syndrome as a model for type 1 (insulin-dependent) diabetes mellitus: increased prevalence of islet cell surface antibodies. Diabetologia. 1984;27(Suppl.):87–9. [PubMed] [Google Scholar]
160. Pak CY, Eun HM, McArthur RG, Yoon JW. Association of cytomegalovirus infection with autoimmune type 1 diabetes. Lancet. 1988;2:1–4. [PubMed] [Google Scholar]
161. Pak CY, Cha CY, Rajotte RV, McArthur RG, Yoon JW. Human pancreatic islet cell specific 38 kilodalton autoantigen identified by cytomegalovirus-induced monoclonal islet cell autoantibody. Diabetologia. 1990;33:569–72. [PubMed] [Google Scholar]
162. Gamble DR. Relation of antecedent illness to development of diabetes in children. BMJ. 1980;281:99–101. [PMC free article] [PubMed] [Google Scholar]
163. Helmke K, Otten A, Willems W. Islet cell antibodies in children with mumps infection. Lancet. 1980;2:211–2. [PubMed] [Google Scholar]
164. Frisk G, Fohlman J, Kobbah M, et al. High frequency of Coxsackie-B-virus-specific IgM in children developing type I diabetes during a period of high diabetes morbidity. J Med Virol. 1985;17:219–27. [PubMed] [Google Scholar]
165. Hyoty H, Hiltunen M, Knip M, et al. A prospective study of the role of coxsackie B and other enterovirus infections in the pathogenesis of IDDM. Diabetes. 1995;44:652–7. Childhood Diabetes in Finland (DiMe) Study Group. [PubMed] [Google Scholar]
166. Schloot NC, Willemen SJ, Duinkerken G, Drijfhout JW, de Vries RR, Roep BO. Molecular mimicry in type 1 diabetes mellitus revisited: T-cell clones to GAD65 peptides with sequence homology to Coxsackie or proinsulin peptides do not crossreact with homologous counterpart. Hum Immunol. 2001;62:299–309. [PubMed] [Google Scholar]
167. Sarugeri E, Dozio N, Meschi F, Pastore MR, Bonifacio E. T cell responses to type 1 diabetes related peptides sharing homologous regions. J Mol Med. 2001;79:213–20. [PubMed] [Google Scholar]
168. Ou D, Mitchell LA, Metzger DL, Gillam S, Tingle AJ. Cross-reactive rubella virus and glutamic acid decarboxylase (65 and 67) protein determinants recognised by T cells of patients with type I diabetes mellitus. Diabetologia. 2000;43:750–62. [PubMed] [Google Scholar]
169. Karounos DG, Wolinsky JS, Thomas JW. Monoclonal antibody to rubella virus capsid protein recognizes a beta-cell antigen. J Immunol. 1993;150:3080–5. [PubMed] [Google Scholar]
170. Hiemstra HS, Schloot NC, van Veelen PA, et al. Cytomegalovirus in autoimmunity: T cell crossreactivity to viral antigen and autoantigen glutamic acid decarboxylase. Proc Natl Acad Sci USA. 2001;98:3988–91. [PMC free article] [PubMed] [Google Scholar]
171. Cavallo MG, Baroni MG, Toto A, et al. Viral infection induces cytokine release by beta islet cells. Immunology. 1992;75:664–8. [PMC free article] [PubMed] [Google Scholar]
172. Prince GA, Jenson AB, Billups LC, Notkins AL. Infection of human pancreatic beta cell cultures with mumps virus. Nature. 1978;271:158–61. [PubMed] [Google Scholar]
173. Parkkonen P, Hyoty H, Koskinen L, Leinikki P. Mumps virus infects beta cells in human fetal islet cell cultures upregulating the expression of HLA class I molecules. Diabetologia. 1992;35:63–9. [PubMed] [Google Scholar]
174. Vuorinen T, Nikolakaros G, Simell O, Hyypia T, Vainionpaa R. Mumps and Coxsackie B3 virus infection of human fetal pancreatic islet-like cell clusters. Pancreas. 1992;7:460–4. [PubMed] [Google Scholar]
175. Tisch R, Yang XD, Singer SM, Liblau RS, Fugger L, McDevitt HO. Immune response to glutamic acid decarboxylase correlates with insulitis in non-obese diabetic mice. Nature. 1993;366:72–5. [PubMed] [Google Scholar]
176. Tian J, Lehmann PV, Kaufman DL. T cell cross-reactivity between coxsackievirus and glutamate decarboxylase is associated with a murine diabetes susceptibility allele. J Exp Med. 1994;180:1979–84. [PMC free article] [PubMed] [Google Scholar]
177. Lawson CM. Evidence for mimicry by viral antigens in animal models of autoimmune disease including myocarditis. Cell Mol Life Sci. 2000;57:552–60. [PubMed] [Google Scholar]
178. Serreze DV, Ottendorfer EW, Ellis TM, Gauntt CJ, Atkinson MA. Acceleration of type 1 diabetes by a coxsackievirus infection requires a preexisting critical mass of autoreactive T-cells in pancreatic islets. Diabetes. 2000;49:708–11. [PubMed] [Google Scholar]
179. Horwitz MS, Ilic A, Fine C, Rodriguez E, Sarvetnick N. Presented antigen from damaged pancreatic beta cells activates autoreactive T cells in virus-mediated autoimmune diabetes. J Clin Invest. 2002;109:79–87. [PMC free article] [PubMed] [Google Scholar]
180. Guberski DL, Thomas VA, Shek WR, et al. Induction of type I diabetes by Kilham’s rat virus in diabetes-resistant BB/Wor rats. Science. 1991;254:1010–3. [PubMed] [Google Scholar]
181. Chung YH, Jun HS, Kang Y, et al. Role of macrophages and macrophage-derived cytokines in the pathogenesis of Kilham rat virus-induced autoimmune diabetes in diabetes-resistant BioBreeding rats. J Immunol. 1997;159:466–71. [PubMed] [Google Scholar]
182. Ellerman KE, Richards CA, Guberski DL, Shek WR, Like AA. Kilham rat triggers T-cell-dependent autoimmune diabetes in multiple strains of rat. Diabetes. 1996;45:557–62. [PubMed] [Google Scholar]
183. Yoon JW, London WT, Curfman BL, Brown RL, Notkins AL. Coxsackie virus B4 produces transient diabetes in nonhuman primates. Diabetes. 1986;35:712–6. [PubMed] [Google Scholar]
184. Willison HJ, Yuki N. Peripheral neuropathies and anti-glycolipid antibodies. Brain. 2002;125:2591–625. [PubMed] [Google Scholar]
185. Ilyas AA, Willison HJ, Quarles RH, et al. Serum antibodies to gangliosides in Guillain–Barré syndrome. Ann Neurol. 1988;23:440–7. [PubMed] [Google Scholar]
186. Joseph SA, Tsao CY. Guillain–Barré syndrome. Adolesc Med. 2002;13:487–94. [PubMed] [Google Scholar]
187. Aspinall GO, Fujimoto S, McDonald AG, Pang H, Kurjanczyk LA, Penner JL. Lipopolysaccharides from Campylobacter jejuni associated with Guillain–Barré syndrome patients mimic human gangliosides in structure. Infect Immun. 1994;62:2122–5. [PMC free article] [PubMed] [Google Scholar]
188. Yuki N, Taki T, Takahashi M, et al. Penner’s serotype 4 of Campylobacter jejuni has a lipopolysaccharide that bears a GM1 ganglioside epitope as well as one that bears a GD1 a epitope. Infect Immun. 1994;62:2101–3. [PMC free article] [PubMed] [Google Scholar]
189. Ang CW, Endtz HP, Jacobs BC, et al. Campylobacter jejuni lipopolysaccharides from Guillain–Barré syndrome patients induce IgG anti-GM1 antibodies in rabbits. J Neuroimmunol. 2000;104:133–8. [PubMed] [Google Scholar]
190. Goodyear CS, O’Hanlon GM, Plomp JJ, et al. Monoclonal antibodies raised against Guillain–Barré syndrome-associated Campylobacter jejuni lipopolysaccharides react with neuronal gangliosides and paralyze muscle-nerve preparations. J Clin Invest. 1999;104:697–708. [PMC free article] [PubMed] [Google Scholar]
191. Wirguin I, Briani C, Suturkova-Milosevic L, et al. Induction of anti-GM1 ganglioside antibodies by Campylobacter jejuni lipopolysaccharides. J Neuroimmunol. 1997;78:138–42. [PubMed] [Google Scholar]
192. Ang CW, Laman JD, Willison HJ, et al. Structure of Campylobacter jejuni lipopolysaccharides determines antiganglioside specificity and clinical features of Guillain–Barré and Miller Fisher patients. Infect Immun. 2002;70:1202–8. [PMC free article] [PubMed] [Google Scholar]
193. Nachamkin I, Liu J, Li M, et al. Campylobacter jejuni from patients with Guillain–Barré syndrome preferentially expresses a GD(1a)-like epitope. Infect Immun. 2002;70:5299–303. [PMC free article] [PubMed] [Google Scholar]
194. Yuki N, Susuki K, Koga M, et al. Carbohydrate mimicry between human ganglioside GM1 and Campylobacter jejuni lipooligosaccharide causes Guillain–Barré syndrome. Proc Natl Acad Sci USA. 2004;101:11404–9. [PMC free article] [PubMed] [Google Scholar]
195. Kusunoki S, Shiina M, Kanazawa I. Anti-Gal-C antibodies in GBS subsequent to mycoplasma infection: evidence of molecular mimicry. Neurology. 2001;57:736–8. [PubMed] [Google Scholar]
196. Ang CW, Tio-Gillen AP, Groen J, et al. Cross-reactive anti-galactocerebroside antibodies and Mycoplasma pneumoniae infections in Guillain–Barré syndrome. J Neuroimmunol. 2002;130:179–83. [PubMed] [Google Scholar]
197. Susuki K, Odaka M, Mori M, Hirata K, Yuki N. Acute motor axonal neuropathy after Mycoplasma infection: evidence of molecular mimicry. Neurology. 2004;62:949–56. [PubMed] [Google Scholar]
198. Koga M, Yuki N, Tai T, Hirata K. Miller Fisher syndrome and Haemophilus influenzae infection. Neurology. 2001;57:686–91. [PubMed] [Google Scholar]
199. Mori M, Kuwabara S, Miyake M, et al. Haemophilus influenzae infection and Guillain–Barré syndrome. Brain. 2000;123:2171–8. [PubMed] [Google Scholar]
200. Mori M, Kuwabara S, Miyake M, et al. Haemophilus influenzae has a GM1 ganglioside-like structure and elicits Guillain–Barré syndrome. Neurology. 1999;52:1282–4. [PubMed] [Google Scholar]
201. Steinman L. Multiple sclerosis: a coordinated immunological attack against myelin in the central nervous system. Cell. 1996;85:299–302. [PubMed] [Google Scholar]
202. Sun JB, Olsson T, Wang WZ, et al. Autoreactive T and B cells responding to myelin proteolipid protein in multiple sclerosis and controls. Eur J Immunol. 1991;21:1461–8. [PubMed] [Google Scholar]
203. Ota K, Matsui M, Milford EL, Mackin GA, Weiner HL, Hafler DA. T-cell recognition of an immunodominant myelin basic protein epitope in multiple sclerosis. Nature. 1990;346:183–7. [PubMed] [Google Scholar]
204. Bernard CC, de Rosbo NK. Immunopathological recognition of autoantigens in multiple sclerosis. Acta Neurol (Napoli) 1991;13:171–8. [PubMed] [Google Scholar]
205. Olson JK, Croxford JL, Miller SD. Virus-induced autoimmunity: potential role of viruses in initiation, perpetuation, and progression of T-cell-mediated autoimmune disease. Viral Immunol. 2001;14:227–50. [PubMed] [Google Scholar]
206. Fujinami RS. Can virus infections trigger autoimmune disease? J Autoimmun. 2001;16:229–34. [PubMed] [Google Scholar]
207. Challoner PB, Smith KT, Parker JD, et al. Plaque-associated expression of human herpesvirus 6 in multiple sclerosis. Proc Natl Acad Sci USA. 1995;92:7440–4. [PMC free article] [PubMed] [Google Scholar]
208. Sriram S, Stratton CW, Yao S, et al. Chlamydia pneumoniae infection of the central nervous system in multiple sclerosis. Ann Neurol. 1999;46:6–14. [PubMed] [Google Scholar]
209. Zhang J, Raus J. Myelin basic protein-reactive T cells in multiple sclerosis: pathologic relevance and therapeutic targeting. Cytotechnology. 1994;16:181–7. [PubMed] [Google Scholar]
210. Wucherpfennig KW, Zhang J, Witek C, et al. Clonal expansion and persistence of human T cells specific for an immunodominant myelin basic protein peptide. J Immunol. 1994;152:5581–92. [PubMed] [Google Scholar]
211. Allegretta M, Nicklas JA, Sriram S, Albertini RJ. T cells responsive to myelin basic protein in patients with multiple sclerosis. Science. 1990;247:718–21. [PubMed] [Google Scholar]
212. Wucherpfennig KW, Strominger JL. Molecular mimicry in T cell-mediated autoimmunity: viral peptides activate human T cell clones specific for myelin basic protein. Cell. 1995;80:695–705. [PMC free article] [PubMed] [Google Scholar]
213. Kurtzke JF. Epidemiologic evidence for multiple sclerosis as an infection. Clin Microbiol Rev. 1993;6:382–427. [PMC free article] [PubMed] [Google Scholar]
214. Kurtzke JF. Multiple sclerosis in time and space – geographic clues to cause. J Neurovirol. 2000;6(Suppl. 2):S134–40. [PubMed] [Google Scholar]
215. Kurtzke JF, Gudmundsson KR, Bergmann S. Multiple sclerosis in Iceland: 1. Evidence of a postwar epidemic. Neurology. 1982;32:143–50. [PubMed] [Google Scholar]
216. Kurtzke JF, Hyllested K. Multiple sclerosis in the Faroe Islands: I. Clinical and epidemiological features. Ann Neurol. 1979;5:6–21. [PubMed] [Google Scholar]
217. Islam T, Gauderman WJ, Cozen W, Hamilton AS, Burnett ME, Mack TM. Differential twin concordance for multiple sclerosis by latitude of birthplace. Ann Neurol. 2006;60:56–64. [PubMed] [Google Scholar]
218. Oleszak EL, Chang JR, Friedman H, Katsetos CD, Platsoucas CD. Theiler’s virus infection: a model for multiple sclerosis. Clin Microbiol Rev. 2004;17:174–207. [PMC free article] [PubMed] [Google Scholar]
219. Kim BS, Palna JP. Immune mechanisms of Theiler’s virus-induced demyelination. Exp Mol Med. 1999;31:115–21. [PMC free article] [PubMed] [Google Scholar]
220. Dal Canto MC, Lipton HL. Ultrastructural immunohistochemical localization of virus in acute and chronic demyelinating Theiler’s virus infection. Am J Pathol. 1982;106:20–9. [PMC free article] [PubMed] [Google Scholar]
221. Lipton HL, Twaddle G, Jelachich ML. The predominant virus antigen burden is present in macrophages in Theiler’s murine encephalomyelitis virus-induced demyelinating disease. J Virol. 1995;69:2525–33. [PMC free article] [PubMed] [Google Scholar]
222. Trottier M, Kallio P, Wang W, Lipton HL. High numbers of viral RNA copies in the central nervous system of mice during persistent infection with Theiler’s virus. J Virol. 2001;75:7420–8. [PMC free article] [PubMed] [Google Scholar]
223. Barbano RL, Dal Canto MC. Serum and cells from Theiler’s virus-infected mice fail to injure myelinating cultures or to produce in vivo transfer of disease. J Neurol Sci. 1984;66:283–93. The pathogenesis of Theiler’s virus-induced demyelination appears to differ from that of EAE. [PubMed] [Google Scholar]
224. Miller SD, Clatch RJ, Pevear DC, Trotter JL, Lipton HL. Class II-restricted T cell responses in Theiler’s murine encephalomyelitis virus (TMEV)-induced demyelinating disease. J Immunol. 1987;138:3776–84. I. Cross-specificity among TMEV substrains and related picornaviruses, but not myelin proteins. [PubMed] [Google Scholar]
225. Clatch RJ, Lipton HL, Miller SD. Characterization of Theiler’s murine encephalomyelitis virus (TMEV)-specific delayed-type hypersensitivity responses in TMEV-induced demyelinating disease: correlation with clinical signs. J Immunol. 1986;136:920–7. [PubMed] [Google Scholar]
226. Miller SD, Vanderlugt CL, Begolka WS, et al. Persistent infection with Theiler’s virus leads to CNS autoimmunity via epitope spreading. Nat Med. 1997;3:1133–6. [PubMed] [Google Scholar]
227. Katz-Levy Y, Neville KL, Padilla J, et al. Temporal development of autoreactive Th1 responses and endogenous presentation of self myelin epitopes by central nervous system-resident APCs in Theiler’s virus-infected mice. J Immunol. 2000;165:5304–14. [PubMed] [Google Scholar]
228. Lavi E, Gilden DH, Wroblewska Z, Rorke LB, Weiss SR. Experimental demyelination produced by the A59 strain of mouse hepatitis virus. Neurology. 1984;34:597–603. [PubMed] [Google Scholar]
229. Knobler RL, Lampert PW, Oldstone MB. Virus persistence and recurring demyelination produced by a temperature-sensitive mutant of MHV-4. Nature. 1982;298:279–80. [PMC free article] [PubMed] [Google Scholar]
230. Wang FI, Hinton DR, Gilmore W, Trousdale MD, Fleming JO. Sequential infection of glial cells by the murine hepatitis virus JHM strain (MHV-4) leads to a characteristic distribution of demyelination. Lab Invest. 1992;66:744–54. [PubMed] [Google Scholar]
231. Takahashi K, Goto N, Matsubara Y, Fujiwara K. Postinflammatory remyelination in the spinal cord of mice infected with mouse hepatitis virus, JHM strain. Jpn J Exp Med. 1987;57:145–51. [PubMed] [Google Scholar]
232. Erlich SS, Fleming JO, Stohlman SA, Weiner LP. Experimental neuropathology of chronic demyelination induced by a JHM virus variant (DS) Arch Neurol. 1987;44:839–42. [PubMed] [Google Scholar]
233. Stohlman SA, Hinton DR. Viral induced demyelination. Brain Pathol. 2001;11:92–106. [PMC free article] [PubMed] [Google Scholar]
234. Wu GF, Perlman S. Macrophage infiltration, but not apoptosis, is correlated with immune-mediated demyelination following murine infection with a neurotropic coronavirus. J Virol. 1999;73:8771–80. [PMC free article] [PubMed] [Google Scholar]
235. Glass WG, Liu MT, Kuziel WA, Lane TE. Reduced macrophage infiltration and demyelination in mice lacking the chemokine receptor CCR5 following infection with a neurotropic coronavirus. Virology. 2001;288:8–17. [PMC free article] [PubMed] [Google Scholar]
236. Wu GF, Dandekar AA, Pewe L, Perlman S. CD4 and CD8 T cells have redundant but not identical roles in virus-induced demyelination. J Immunol. 2000;165:2278–86. [PubMed] [Google Scholar]
237. Lane TE, Liu MT, Chen BP, et al. A central role for CD4(+) T cells and RANTES in virus-induced central nervous system inflammation and demyelination. J Virol. 2000;74:1415–24. [PMC free article] [PubMed] [Google Scholar]
238. Fazakerley JK, Pathak S, Scallan M, Amor S, Dyson H. Replication of the A7(74) strain of Semliki Forest virus is restricted in neurons. Virology. 1993;195(7):627–37. [PubMed] [Google Scholar]
239. Balluz IM, Glasgow GM, Killen HM, Mabruk MJ, Sheahan BJ, Atkins GJ. Virulent and avirulent strains of Semliki Forest virus show similar cell tropism for the murine central nervous system but differ in the severity and rate of induction of cytolytic damage. Neuropathol Appl Neurobiol. 1993;19:233–9. [PubMed] [Google Scholar]
240. Amor S, Scallan MF, Morris MM, Dyson H, Fazakerley JK. Role of immune responses in protection and pathogenesis during Semliki Forest virus encephalitis. J Gen Virol. 1996;77:281–91. [PubMed] [Google Scholar]
241. Mokhtarian F, Swoveland P. Predisposition to EAE induction in resistant mice by prior infection with Semliki Forest virus. J Immunol. 1987;138:3264–8. [PubMed] [Google Scholar]
242. Fazakerley JK, Amor S, Webb HE. Reconstitution of Semliki forest virus infected mice, induces immune mediated pathological changes in the CNS. Clin Exp Immunol. 1983;52:115–20. [PMC free article] [PubMed] [Google Scholar]
243. Subak-Sharpe I, Dyson H, Fazakerley J. In vivo depletion of CD8+ T cells prevents lesions of demyelination in Semliki Forest virus infection. J Virol. 1993;67:7629–33. [PMC free article] [PubMed] [Google Scholar]
244. Keogh B, Atkins GJ, Mills KH, Sheahan BJ. Avirulent Semliki Forest virus replication and pathology in the central nervous system is enhanced in IL-12-defective and reduced in IL-4-defective mice: a role for Th1 cells in the protective immunity. J Neuroimmunol. 2002;125:15–22. [PubMed] [Google Scholar]
245. Keogh B, Atkins GJ, Mills KH, Sheahan BJ. Role of interferon-gamma and nitric oxide in the neuropathogenesis of avirulent Semliki Forest virus infection. Neuropathol Appl Neurobiol. 2003;29:553–62. [PubMed] [Google Scholar]
246. Mokhtarian F, Shi Y, Zhu PF, Grob D. Immune responses, and autoimmune outcome, during virus infection of the central nervous system. Cell Immunol. 1994;157:195–210. [PubMed] [Google Scholar]
247. Smith-Norowitz TA, Sobel RA, Mokhtarian F. B cells and antibodies in the pathogenesis of myelin injury in Semliki Forest virus encephalomyelitis. Cell Immunol. 2000;200:27–35. [PubMed] [Google Scholar]
248. Mokhtarian F, Zhang Z, Shi Y, Gonzales E, Sobel RA. Molecular mimicry between a viral peptide and a myelin oligodendrocyte glycoprotein peptide induces autoimmune demyelinating disease in mice. J Neuroimmunol. 1999;95:43–54. [PubMed] [Google Scholar]
Articles from Clinical and Experimental Immunology are provided here courtesy of British Society for Immunology
The triggering of post-COVID-19 autoimmunity phenomena could be associated with both transient immunosuppression and an inappropriate form of immune reconstitution in susceptible individuals: Carlos A. Cañas (2)
Data support COVID-19 as autoimmunity trigger in patients without preexisting IMIDs
Healio Rheumatology (3)
Autoimmune and inflammatory diseases following COVID-19: Caroline galeotti ja Jagadeesh Barry (4)
COVID-19 may cause long-term autoimmune complications: healtheuropa.eu (5)