Insuliini ja terveys: Neljäs luku
Jatkan insuliinia käsittelevää kirjoitussarjaa syventymällä insuliinin terveysvaikutuksiin erityisesti sydän- ja verisuonitauteihin liittyen. Aiemmissa artikkeleissa (Insuliini ja terveys: Johdanto, Insuliini ja terveys: Hiilihydraatti-insuliinimalli, Insuliini ja terveys: Kolmas luku)käsittelin insuliinin kemiallista rakennetta, aineenvaihduntaa ja biokemiaa yleisellä tasolla.
Aihe on vaikea ja joiltain osin kiistanalainen, joten esittelen tässä kirjoituksessa kaksi hyvin perusteltua näkemystä insuliiniresistenssin syistä. Ne ovat osittain yhteneviä ja osittain ristiriitaisia. Kahden tutkiimuskatsauksen käsittelyn vuoksi teksti on todella pitkä ja paikoin myös vaikeaselkoinen.
Tässä tutkimuskatsauksessa osoitetaan, että:
Heikentynyt ravinnonsaanti edistää hyperlipidemiaa ja insuliiniresistenssiä aiheuttaen hyperglykemiaa. Tämä tila muuttaa solujen metaboliaa ja solunsisäistä signalointia, joka vaikuttaa negatiivisesti soluihin.
Kardiomyosyytissä tämä vaurio voidaan tiivistää kolmeen vaikutukseen:
- muutos insuliinin signalointiin
- kasvanut substraatin saavutettavuus ja
- aineenvaihdunnan muutosten joustamattomuus
Kaikki nämä vaikutukset edistävät solutapahtumia, kuten:
- geeniekspressiomodifikaatiot
- hyperglykemia ja dyslipidemia
- oksidatiivisen stressin ja tulehdusvasteen aktivoituminen,
- endoteelin toimintahäiriöt ja
- kohdunulkoisten lipidien kumuloituminen, joka ylläpitää metabolisen sääntelyn purkamista
Kaiken kaikkiaan insuliiniresistenssi vaikuttaa sydän- ja verisuonitauteihin (CVD) kahden itsenäisen aineenvaihdutareitin kautta:
- ateroomapleksin muodostuminen
- kammion hypertrofia ja diastolinen poikkeavuus
Lyhyesti: Tämä tutkimuskatsaus osoittaa, että korkea verensokeri ja insuliiniresistenssi ovat merkittäviä sydäntautien riskitekijöitä.
Diabeetikoilla on suurempi sydäninfarktin, sydäntautien ja sydänkuolleisuuden riski kuin diabetesta sairastamattomilla. Tätä riskiä ei selitä muut muuttujat, kuten tupakointi, kolesteroli, verenpaine tai kehon rasvan jakautuminen.
Hypo- ja hyperinsulinemiaan liittyvät sairaudet
Insuliinilla on merkittäviä metabolisia vaikutuksia koko kehossa. Haiman Langerhansin saarekkeiden beetasolut säätelevät insuliinin tuotantoa seuraamalla plasman glukoosin, aminohappojen, ketohappojen ja rasvahappojen pitoisuuksia. Insuliini säätelee energiaravinteiden hapettamista energiaksi ja varastointia rasvakudokseen triglyserideina.
Diabetes mellitus (DM1) on insuliinin puutokseen (hypoinsulinemiaan) liittyvä sairaus, jossa elimistön oma immuunijärjestelmä tuhoaa haiman Langerhansin saarekkeiden beetasoluja, mikä nopeasti johtaa elintärkeän insuliinin tuotannon vähenemiseen ja loppumiseen.Tyypin 1 diabetes puhkeaa tavallisesti alle 40-vuotiaana ja usein jo lapsena ennen murrosikää.
Beetasolujen tuhoutuminen on todennäköisesti seurausta beetasolujen yhteen tai useampaan rakenteeseen kohdistuvasta virheellisen tunnistamisen aiheuttamasta autoimmunireaktiosta, jossa elimistön oma immuunijärjestelmä kohdistaa aktivaation omia kudoksia vastaan.
Taudin tarkkaa syytä ei tunneta, mutta sairastuminen edellyttää geneettisen alttiuden sekä yhden tai useamman taudin laukaisevan ympäristömuuttujan. Tyypin 1 diabeteksen saattaa laukaista esimerkiksi sikiöaikainen D-vitamiinin puutos ja yleinen herpes zoster-infektio.
Taudin oireet saadaan hallintaan insuliinikorvaushoidolla. Verensokeripitoisuuden muutosten tarkkailu, tasaisen verensokerin ylläpitäminen, insuliinihoito ja ruokavaliomuutokset minimoivat tyypin 1 diabeteksen pitkän aikavälin komplikaatioita, kuten verisonten ja hermoston vaurioitumista. Insuliinihoito on elinkautinen.
DM2
Tyypin 2 diabetes mellitus (DM2) on useiden vuosien aikana kehittyvä solujen insuliiniherkkyyden heikentymisestä johtuva elintapasairaus. Toisin sanoen kohdekudokset eivät reagoi asianmukaisesti haiman tuottamaan insuliiniin. Seurauksena voi olla hyperinsulinemia, jossa vereen erittyvä runsaskaan insuliini ei avaa soluja glukoosinotolle.
Rasvakudoksen ja elinten adiposyyttien insuliiniherkkyys säilyy yleensä pitkään, joten glukoosi ohjautuu rasvasoluihin lihasten sijaan.
Tyypillisesti DM2 puhkeaa aikuisiässä. Massiivisista tutkimusponnisteluista huolimatta tyypin 2 diabetekseen johtavien tekijöiden tarkkaa luonnetta on ollut vaikea varmistaa. Taudin patogeneesi on selvästi monitekijäinen.
Lihavuutta pidetään riskitekijänä, mutta lihavuus voi itsessään olla diabetesta edeltävä oire insuliiniresistenssistä. Kaikki diabeetikot eivät ole lihavia, mutta monet lihavat sairastavat insuliiniresistenssiä. Insuliiniresistenssi todennäköisesti johtaa aikuistyypin diabetekseen. Insuliiniresistenssin aiheuttama lihavuus ei aina näy ulospäin, sillä se aiheuttaa tavallisesti elinten rasvoittumista ja viskeraalista keskivartalon elimiä ympäröivää läskiä.
Aikuistyypin diabeteksessa haiman kyky syntetisoida ja erittää insuliinia säilyy ainakin taudin varhaisvaiheessa melko normaalina. Insuliinilääkityksestä ei siis taudin varhaisvaiheessa ole sanottavaa hyötyä. Pikemminkin päinvastoin. Tautia hallitaan ruokavaliohoidolla ja verensokeria laskevilla hypoglykeemisillä lääkkeillä.
Tyypin 2 diabetes on kuitenkin etenevä sairaus, jossa insuliinilääkityskin tulee todennäköisesti ajankohtaiseksi jossain vaiheessa, mikäli verensokeri- ja insuliinipitoisuuksia ei ruokavaliolla saada korjattua.
Hyperinsulinemia, eli liiallinen insuliinin eritys on yleisimmin seurausta insuliiniresistenssistä, joka liittyy tyypin 2 diabetekseen tai metaboliseen oireyhtymään. Hyperinsulinemia voi myös johtua haiman insuliinia erittävästä kasvaimesta (insulinooma), mutta se on harvinaista.
Hyperinsulinemia voi olla hengenvaarallinen tila, josssa veren glukoosipitoisuus laskee nopeasti ja aivojen energiansaanti romahtaa (insuliinishokki).
Glukagoni
Glukagonilla on tärkeä rooli veren normaalin glukoosipitoisuuden säätelyssä. Se on insuliinin vastavaikuttaja. Toisin sanoen glukagonin vaikutus veren glukoosipitoisuuteen on päinvastainen insuliinin vaikutukselle. Insuliini on anabolinen hormoni, joka orkestroi energiaravinteiden käyttöä ja varastoimista. Glukagoni on katabolinen hormoni, joka purkaa energiavarastoja, kuten glykogeenejä verenkiertoon.
Glukagoni on lineaarinen peptidi, jossa on 29 aminohappoa. Sen ensisijainen sekvenssi on melkein täysin konservoitunut (identtinen) selkärankaisten keskuudessa, ja se on rakenteellisesti sukua peptidihormonien sekretiiniperheeseelle.
Glukagoni syntetisoidaan proglukagonina ja prosessoidaan proteolyyttisesti glukagonin tuottamiseksi haimasaarien alfasoluissa. Proglukagonia ilmentyy myös suolistossa, jossa sitä ei prosessoida glukagoniksi, vaan glukagonin kaltaisten peptidien perheeksi (enteroglukagoni).
Glukagonin fysiologiset vaikutukset
Glukagonin tärkein vaikutus on stimuloida veren glukoosipitoisuuden nousua.
Kun veren glukoosipitoisuus alkaa laskea normaalin alapuolelle, on välttämätöntä löytää ja pumpata lisää glukoosia vereen. Glukagoni hallitsee kahta keskeistä metaboliareittiä maksassa, mikä johtaa siihen, että elin luovuttaa glukoosia muuhun kehoon:
-
Glukagoni stimuloi maksassa varastoituneen glykogeenin hajoamista.
Kun veren glukoosipitoisuus on korkea, maksa varastoi suuria määriä glukoosia glykogeeneiksi. Maksan glykogeenien koko vaihtelee ihmisten ja elämäntilanteiden välillä, mutta keskimäärin glukoosia varastoituu maksaan noin 200-250 g.
Insuliinin vaikutuksesta osa glukoosista varastoidaan glykogeenin muodossa. Myöhemmin, kun veren glukoosipitoisuus alkaa laskea, glukagonin erittyminen vaikuttaa maksasoluihin aktivoiden entsyymejä, jotka depolymeroivat glykogeenejä glukoosiksi ja vapauttavat glukoosia verenkiertoon.
-
Glukagoni aktivoi maksan glukoneogeneesiä. Glukoneogeneesi on aineenvaihduntakanava, jossa sitruunahappokierron väliaineita, eräitä aminohappoja ja glyserolia muutetaan glukoosiksi.
Glukoneogeneesi tuottaa tarvittaessa kaiken elimistön tarvitseman glukoosin.
Glukagonilla näyttää olevan vähäinen vaikutus triglyseridien lipolyysin tehostamisessa rasvakudoksessa.
Lipolyyttiset hormonit, kuten kortikotropiini, glukagoni ja adrenaliini aktivoivat rasvasolujen lipolyysin, jossa triglyseridejä pilkotaan verenkiertoon vapaiksi rasvahapoiksi ja glyseroliksi.
Insuliini on puolestaan lipolyyttisten entsyymien, kuten hormonisensitiivisen lipaasin (HSL) estäjä. Veren korkea insuliinipitoisuus estää rasvasolujen purkamisen energiakäyttöön.
Glukagonierityksen hallinta
Glukagonin tärkein vaikutus on lisätä veren glukoosipitoisuutta. Glukagonia erittyy hypoglykemian, eli matalan veren glukoosipitoisuuden vaikutuksesta. Kahden muun mekanismin tiedetään laukaisevan glukagonin erityksen:
-
Kohonnut aminohappopitoisuus veressä: Tässä tilanteessa glukagoni edistää ylimääräisten aminohappojen muuntumista glukoosiksi lisäämällä glukoneogeneesiä.
Koska korkea veren aminohappopitoisuus stimuloi myös insuliinin erittymistä, tämä on poikkeuksellinen tilanne, jossa sekä insuliini että glukagoni ovat samanaikaisesti aktiivisia.
- Liikunta: Tässä tapauksessa ei ole täysin selvää, onko todellinen glukoosin erittymisen laukaiseva ärsyke liikunta sinänsä vai liikunnan aiheuttama veren glukoosipitoisuuden lasku.
Glukagonin eritystä estävät korkeat verensokeritasot. Ei ole selvää, heijastako tämä glukoosin suoraa vaikutusta alfasoluun vai ehkä insuliinin vaikutusta, jonka tiedetään vaimentavan glukagonia.
Toinen hormoni, jonka tiedetään estävän glukagonin eritystä, on somatostatiini.
Glukagoniin liittyvät sairaudet
Glukagonin korkeaan tai matalaan eritykseen liittyvät sairaudet ovat hyvin harvinaisia. Alfa-solujen (glukagonomat) syövät ovat eräs sairaus, jonka tiedetään aiheuttavan liiallista glukagonieritystä.
Vaikka insuliinipuutos on selvästi tärkein tekijä tyypin 1 diabetes mellituksessa, on huomattavaa näyttöä siitä, että glukagonin poikkeava eritys edistää taudissa havaittuja metabolisia häiriöitä.
Monilla diabetesta sairastavilla potilailla, joilla mitataan hyperglykeminen verensokeri, on myös kohonnut glukagonipitoisuus veressä, vaikka kohonnut verensokeritaso estää glukagonin eritystä.
Sydän- ja verisuonitaudit: Yleinen näkemys
Vuosikymmenten ajan sydän- ja verisuonitaudit (CVD) ovat olleet johtava kuolinsyy ympäri maailmaa.
Sydän- ja verisuonitauteihin liittyy useita samanaikaisia sairauksia, kuten lihavuus, epänormaalit lipidiprofiilit ja insuliiniresistenssi. Vaikka insuliiniresistenssi ja DM2 hyväksytään vihdoin sydän- ja verisuonitautien itsenäisiksi riskitekijöiksi, yleinen sydänsairauksien malli nojaa vahvasti perinteiseen oppiin rasvojen ja erityisesti tyydyttyneiden rasvojen haitallisuudesta.
Vaikka vapaat rasvahapot näyttävät kasvattavan insuliiniresistenssin riskiä, mekanismi jolla rasvahapot aiheuttavat insuliiniresistenssin, on tuntematon.
Kyse lienee perinteisestä muna-kana-ongelmasta: kumpi oli ensin? Aineenvaihdunnan tasolla syy- ja seuraussuhteet kääntyvät herkästi nurinniskoin.
Insuliiniresistenssistä on ainakin kaksi vaihtoehtoista mallia: a) rasva aiheuttaa insuliiniresistenssia, ja b) insuliiniresistenssi aiheuttaa kehon ja veren rasvapitoisuuden lisääntymistä ja lihomista.
Avaan tässä tutkimuskatsausta, jonka ovat koonneet Valeska Ormazabal, Soumyalekshmi Nair, Omar Elfeky, Claudio Aguayo, Carlos Salomon & Felipe A. Zuñiga. Association between insulin resistance and the development of cardiovascular disease on julkaistu alun perin Cardiovascular Diabetology -lehdessä.
Lopuksi tutustun vielä lyhyesti James J. DiNicolantonion ja James H. O’keefen BMJ-lehdessä julkaistuun artikkeliiin: Added sugars drive coronary heart disease via insulin resistance and hyperinsulinaemia: a new paradigm.
Ensimmäinen tutkimuskatsaus noudattaa nähdäkseni yleistä ja perinteisempää lääke- ja ravintotieteellistä tulkintaa insuliiniresistenssistä ja sen vaikutuksista sydän- ja verisuonitauteihin.
Tämä käsitys on osittain ristiriidassa kasvavan rasvojen aineenvaihduntaa selittävän tutkimusaineiston kanssa. Tieteen periaatteisiin kuuluu tieteen itseään korjaava luonne; paremmin ilmiöitä selittävä evidenssin tukema malli kumoaa heikommin ilmiöitä selittävän mallin. Nähdäkseni tyydyttyneisiin rasvoihin liittyvä paradigma on romahtamassa ja oppi sokereiden haitallisuudesta täsmentyy jatkuvasti.
Kasvavan evidenssin mukaan hyperglykemia ja insuliiniresistenssi ovat sydän- ja verisuoniterveyden kannalta merkittävämpiä riskitekijöitä, kuin LDL.
Jälkimmäinen artikkeli vastaa lähemmin uutta käsitystä insuliiniresistenssista sydän- ja verisuonitautien riskitekijänä. Siinä sydän- ja verisuonitaudit palautuvat hyperglykemiaan, insuliiniresistenssiin ja hyperinsulinemiaan.
Insuliini on avainhormoni, joka toimii solujen aineenvaihdunnan säätelijänä monissa ihmiskehon kudoksissa.
Insuliiniresistenssi määritellään kudosvasteen heikkenemisenä insuliinin stimulaatiolle, joten insuliiniresistenssille on tunnusomaista glukoosin imeytymisen ja hapettumisen häiriöt, glykogeenisynteesin väheneminen ja vähäisemmässä määrin kyky estää lipidien hapettumista ( β-oksidaatiota).
Vapaat rasvahapot ovat hallitseva substraatti, jota aikuisen sydänlihaksessa käytetään ATP:n tuotantoon, mutta sydämen metabolinen verkosto on erittäin joustava ja se voi käyttää muita substraatteja, kuten glukoosia, laktaattia, ketoaineita tai aminohappoja energian tuotantoon.
Substraatilla tarkoitetaan yhdistettä, jota entsyymi- tai muu reaktio muuttaa. Energia-aineenvaihdunnan substraatteja ovat glukoosi, vapaat rasvahapot, ketoaineet ja aminohapot.
Insuliiniresistenssin aikana useat metaboliset muutokset johtavat sydän- ja verisuonitautien riskin lisääntymiseen. Insuliiniresistenssi voi esimerkiksi aiheuttaa glukoosimetabolian epätasapainon, kuten kroonisen hyperglykemian, mikä puolestaan laukaisee oksidatiivisen stressin, joka aiheuttaa soluvaurioihin johtavan tulehdusreaktion.
Insuliiniresistenssi voi myös muuttaa systeemistä lipidimetaboliaa, joka johtaa sitten dyslipidemiaan ja haitallisen lipiditriadin kehittymiseen:
-
korkeat plasman triglyseridipitoisuudet
-
matalat korkean tiheyden lipoproteiinipitoisuudet (HDL)
-
matalatiheyksisten lipoproteiinien lisääntyminen (LDL)
Tämä lipiditriadi yhdessä endoteelin insuliinisignaloinnin toimintahäiriöiden kanssa myötävaikuttaa ateroskleroottisen plakin muodostumiseen.
Insuliiniresistenssin ja sydämen metabolisten muutosten systeemiset seuraukset aiheuttavat vahinkoa ainakin kolmella mekanismilla:
- insuliinisignaloinnin muuttuminen
-
heikentynyt energiasubstraatin aineenvaihdunnan säätely
-
muuttunut substraattien kulku sydänlihakseen
Insuliiniresistenssin vähentämiseen keskittyvät hoidot voivat vähentää sekä sydän- ja verisuonitautien että ateroskleroottisten plakkien muodostumista.
Sydäntautien tausta
Sydän- ja verisuonitauteihin liittyvät patologiset prosessit ja riskitekijät alkavat jo lapsuudessa.
Erityisesti lihavuus, joka liittyy epänormaaliin lipidiprofiiliin nuoremmalla iällä, assosioituu vahvasti insuliiniresistenssin kanssa. Kuten tutkimuksissa korostetaan, monilla tekijöillä, kuten lihavuudella, epänormaalilla lipidiprofiililla ja insuliiniresistenssillä, on keskeinen rooli sydän- ja verisuonitautien (CVD) kehittymisessä.
Fysiologisissa olosuhteissa insuliini stimuloi metabolisten substraattien käyttöä monissa kudoksissa, kuten sydämessä, luurankolihaksissa, maksassa ja rasvakudoksessa.
Kardiomyosyyteissä, eli sydänlihassoluissa insuliini edistää glukoosin ja rasvahappojen imeytymistä, mutta estää β-ksidaation eli rasvahappojen hapettamisen energiaksi.
Haima yrittää kompensoida solujen heikentynyttä insuliiniherkkyyttä erittämällä kasvavia määriä insuliinia, mikä johtaa hyperinsulinemiaan.
Insuliiniresistenssin ja / tai hyperinsulinemian aikana normaali glukoositoleranssi säilyy johtuen joukosta fysiologisia muutoksia, jotka tämä ilmiö aktivoi.
Insuliiniresistenssin ja CVD:n kehittymisriskin välillä on todettu vahva korrelaatio. Useat molekyylimekanismit edistävät insuliiniresistenssin ja CVD:n välistä yhteyttä. Nämä mekanismit sisältävät insuliiniresistenssin roolin ateroskleroosin kehittymisessä, verisuonten (endoteelin) toiminnassa, verenpainetaudissa ja makrofagien lisääntymisessä.
Insuliinisignalointi
Insuliini on voimakas anabolinen hormoni, jolla on laajasti vaikutuksia monentyyppisiin soluihin.
Jotkut insuliinin tärkeimmistä metabolisista vaikutuksista ovat glukoosinoton stimuloiminen luurankolihaksissa ja adiposyyteissä, glykogeenisynteesin edistäminen luurankolihaksissa, maksan glukoosituotannon (glukoneogeneesin) tukahduttaminen ja lipolyysin estäminen adiposyyteissä.
Ruokailun seurauksena insuliinia erittyy haimasta verenkiertoon. Se aiheuttaa kiertävän glukoosin imeytymistä kohdekudoksiin sitoutumalla solujen insuliinireseptoreihin.
Tämä sitoutuminen aktivoi reseptorin autofosforylaation, joka laukaisee alavirran signalointikaskadin fosforyloimalla insuliinireseptorisubstraattien tyrosiinitähteet, IRS (IRS-1 tai IRS-2), mitä seuraa reaktiosarja, jossa fosfatidyyli-inositoli-3-kinaasi (PI3K), fosfoinositidista riippuvainen kinaasi -1, Akt (Akt1 ja Akt2), proteiinikinaasi C (PKC) ja rapamysiinin* nisäkäskohde (mTOR), samoin kuin ribosomaalinen proteiini S6-kinaasi beeta 1 (S6K1) fosforyloituvat.
Substraattitason fosforylaatio
Substraattitason fosforylaatio on soluissa tapahtuva kemiallinen reaktio, jossa syntyy ATP:tä fosfaattiryhmän liittyessä ADP:hen. Reaktio tapahtuu solulimassa glykolyysin yhteydessä sekä aerobisissa että anaerobisissa oloissa.
Substraattitason fosforylaatiossa voi syntyä neljä ATP:tä. Kaksi ATP-molekyyliä syntyy kahden 1,3-bisfosfoglyseraatin luovuttaessa fosfaattiryhmän ADP:lle fosfoglyseraattikinaasientsyymin avulla. Samalla syntyy 3-fosfoglyseraattia. Kaksi ATP:tä syntyy myös, kun fosfoenolipyruvaatti luovuttaa fosfaattiryhmän ADP:lle pyruvaattikinaasientsyymin avulla. Lisäksi syntyy palorypälehappoa.
Substraattitason fosforylaatio toimii myös luustolihaksissa ja aivoissa, joissa on energiaa varastoivaa ja fosfaattiryhmän sisältävää fosfokreatiinia ja kreatiinifosfokinaasientsyymi siirtää fosfaattiryhmän ADP:lle, jolloin tuloksena on ATP:tä. – Wikipedia
*Rapamysiini (sirolimuusi) on immunosuppressiivinen lääke, jota käytetään elinsiirron, varsinkin munuaisensiirron jälkeisen hylkimisreaktion estossa. Se löydettiin alun perin Pääsiäissaarelta (Rapa Nui), mistä tulee nimitys rapamysiini.
Yhdysvaltalaisessa tutkimuksessa sirolimuusi pidensi vanhojen hiirten jäljellä olevaa elinajanodotetta 28–38%:lla. Aine kuitenkin heikentää immuniteettia, joten ihmisille se ei sovi vanhenemisen hidastamiseen.
Rapamysiini lisää henkilön alttiutta saada vaarallinen infektio. Lääkkeen aiheuttama immuunijärjestelmän heikkeneminen voi myös lisätä syöpäriskiä. Lääkkeellä on runsaasti sivuvaikutuksia, kuten hypertensio, nivelkivut, vatsavaivat, kuume, virtsatietulehdus, pahoinvointi, päänsärky, anemia ja hypokalemia. Rapamysiini hidastaa energian kulutusta.
GLUT4
Nämä aineenvaihduntatapahtumat johtavat lisääntyneeseen glukoosinkuljettaja-4:n (GLUT4) siirtymään (translokaatio) solukalvolle, mikä helpottaa glukoosinottoa.
Imeytymisen jälkeen vapaa glukoosi fosforyloituu nopeasti glukoosi-6-fosfaatiksi (G6P), joka myöhemmin siirtyy eri metaboliareiteille.
Insuliinisignalointi tehostaa lipidien varastoitumista rasvasoluihin kahdella mekanismilla, stimuloimalla triglyseridisynteesiä ja estämällä lipolyysin käynnisymistä.
Triglyseridejä varastoidaan lipidipisaroihin, jotka sisältävät lipidipisaraproteiineja, kuten perilipiiniä.
Lipolyysin esto tapahtuu vähentämällä cAMP-tasoja ja estämällä proteiinikinaasi A:n (PKA) -aktiivisuutta, mikä heikentää siten hormoniherkän lipaasin -fosforylaatiota ja perilipiiniä aiheuttaen lipolyysinopeuden laskun.
Adiposyyttien lipidipisaroiden sisältämät triglyseridit hydrolysoituvat rasvahapoiksi, asyyliglyserideiksi ja glyseroliksi aktivoimalla hormoniherkkää lipaasia.
Maksassa insuliini estää glukoosin tuotantoa ja vapautumista estämällä glukoneogeneesin ja glykogenolyysin säätämällä fosfoenolipyruvaattikarboksylaasin (PEPCK) ilmentymistä.
Lisäksi insuliini voi stimuloida glykogeenisynteesiä Akt2-aktivaation, glykogeenisyntaasikinaasi 3:n (GSK3) estämisen ja glykogeenisyntaasin (GS) aktivaation kautta seriinitähteiden desfosforylaation kautta näiden proteiinien NH2- ja COOH-terminaaleissa.
Insuliinin verisuonivaikutukset ovat monimutkaisia: insuliinilla voi olla joko suojaavia tai haitallisia vaikutuksia verisuonistossa.
Insuliinin verisuonia suojaavat vaikutukset liittyvät endoteelin typpioksidisyntaasin (eNOS) aktivaatioon PI3K / Akt-reitin kautta.
Haitallisiin vaikutuksiin sisältyy verisuonten sileän lihassolun (VSMC) lisääntymisen indusointi, verisuonten supistuminen ja proinflammatorinen aktiivisuus.
Nämä verisuonivaikutukset välittyvät mitogeeniaktivoidun proteiinikinaasireitin (MAPK) kautta. Tämä osallistuu vain insuliinin mitogeenisiin vaikutuksiin, mutta ei sen metabolisiin vaikutuksiin. Mitogeeni on yhdiste, joka käynnistää solunjakautumisen.
Insuliiniresistenssi
Yleisen hypoteesin mukaan insuliiniresistenssi määritellään kliiniseksi tilaksi, jossa insuliinilla on odotettua pienempi fysiologinen vaikutus.
Insuliiniresistenssi tarkoittaa tilaa, jossa insuliinin vaikutus heikkenee. Insuliiniresistenssi aiheuttaa verensokerin nousua (hyperglykemia). Insuliiniresistenssi lisää huomattavasti kakkostyypin diabeteksen sekä sydän- ja verisuonisairauksien riskiä.
Muutos voi olla lyhyt- tai pitkävaikutteinen aiheuttajasta riippuen. Resistenssille herkistäviä tekijöitä tunnetaan yli 30, niitä ovat muun muassa lihavuus, tupakointi, asidoosi, alkoholi, korkea verenpaine, raskaus (raskausajan diabetes) ja palovammat. Insuliiniresistenssi on yhteinen nimittäjä monille sairauksille, jotka yleistyvät länsimaissa. Yksi yleisimmistä on metabolinen oireyhtymä.
Insuliiniresistenssi voi johtua häiriöstä insuliinin sitoutumisessa solun insuliinireseptoriin, reseptorien määrän tai toiminnan muutoksesta, glukoosin-sokerin kuljetusproteiinin (GLUT4) määrän tai toiminnan häiriöstä tai glukoosiaineenvaihdunnan häiriöstä solun sisällä. Häiriö on siis glukoosin otossa soluun tai sen aineenvaihdunnassa solun sisällä.
Insuliiniresistenssistä kärsiviä suositellaan valitsemaan matalan glykemiaindeksin ruoka-aineita ja ruokia. Lisäksi heidän kannattaa valita sellaisia ruoka-aineita, joilla on myös matala insuliini-indeksi. – Wikipedia
Glukoosinoton häiriö
Tämä ilmiö johtuu puutteista insuliinin stimuloimassa glukoosinotossa, erityisesti glykogeenisynteesissä, ja vähemmässä määrin glukoosin hapettumisessa. Insuliiniresistenssin vaikutukset eri kudoksiin riippuvat kudosten fysiologisesta ja metabolisesta toiminnasta.
Suuren aineenvaihduntavaikutuksen vuoksi insuliiniresistenssillä on merkittäviä vaikutuksia luurankolihakseen, rasvasoluihin ja maksakudokseen, jotka ovat solunsisäisen glukoosikuljetuksen sekä glukoosi- ja lipidimetabolian pääkohteet.
Luurankolihasten ja rasvasolujen osuus GLUT4 -reseptorien insuliinin stimuloimasta glukoosinotosta ovat noin 60–70%.
Insuliiniresistenssi heikentää maksan ja lihasten glykogeenisynteesiä, lisää proteiinikataboliaa luurankolihaksissa (lihasten kannibalisoiminen energiaksi) ja estää lipoproteiinilipaasiaktiivisuutta adiposyyteissä, mikä johtaa vapaiden rasvahappojen ja tulehduksellisten sytokiinien, kuten IL-6, TNFa sekä kylläisyyshormoni leptiinin, erityksen lisääntymiseen.
Maksan aineenvaihdunta kattaa karkeasti 30% insuliinin stimuloimasta glukoosin metaboliasta. Insuliiniresistenssi heikentää maksan glukoosiaineenvaihduntaa ja rasvahappojen aineenvaihduntaa, mikä puolestaan lisää veren triglyseridipitoisuutta ja VLDL-lipoproteiinien eritystä maksasta.
Insuliiniresistenssi aiheuttaa endoteelisolujen toimintahäiriöitä vähentämällä typpioksidin tuotantoa endoteelisoluissa ja lisäämällä veren hyytymistä estävien tekijöiden vapautumista. Tämä johtaa verihiutaleiden aggregaatioon (puuroutumiseen).
Insuliiniresistenssi vaikuttaa PI3K-reitin metaboliaan, kun taas MAP-kinaasireitti toimii normaalisti. Tämä aiheuttaa insuliinin mitogeenisen vaikutuksen endoteelisoluissa ja kasvattaa ateroskleroosin riskiä.
Veren matalalalla insuliinipitoisuudella ja insuliiniresistenssillä on merkittävä fysiologinen rooli raskauden ja nälkiintymisen aikaisen aineenvaihdunnan säätelyssä.
Ravinnon puutteellisen saannin aiheuttama alhainen glukoosipitoisuus johtaa heikentyneeseen insuliinin eritykseen, mikä helpottaa glukoosin mobilisoitumista maksasta.
Matala insuliinipitoisuus edistää lipolyysin käynnistymistä, jolloin rasvasoluista vapautuu vereen vapaita rasvahappoja ja glyserolia, joita voidaan käyttää ketoaineiden, β-oksidaation ja glukoosin lähtöaineina.
Nämä kompensointimekanismit auttavat ylläpitämään verensokeritasoja poikkeusolosuhteissa, kuten paastolla. Nykyään tiedetään, että aivosolut osaavat tuottaa energiaa ketoaineista, mutta vielä kymmenisen vuotta sitten aivotoiminnan uskottiin edellyttävän tasaista glukoosinsaantia.
β-hydroksibutyraatti on aivojen kuvantamisen ja kognitiivisten testien perusteella erinomainen energianlähde aivosoluille.
Veren punasoluilta puuttuu mitokondriot, joten niiden energianluotanto on glukoosista energiaa tuottavan glykolyysin varassa. Gukoosin puuttuessa ja glykogeenien ehtyessä glukoneogeneesi valmistaa glukoosia veren punasoluille.
Odottavan äidin insuliiniresistenssi sekä glukoosinsaannin turvaavat kompensoivat aineenvaihduntamekanismit varmistavat sikiölle kasvun ja kehityksen kannalta riittävän energian- ja ravinteiden saatavuuden.
Insuliiniresistenssi on avainasemassa metabolisten sairauksien, kuten tyypin 2 diabeteksen patogeneesissä. Insuliiniresistenssi on osallisena useissa muissakin sairauksissa, kuten rintasyövässä, nivelreumassa, munasarjojen monirakkulaoireyhtymässä, alkoholista riippumattomassa rasvamaksassa sekä sydän- ja verisuonitaudeissa. Insuliinimetabolian häiriöt vaikuttavat useimpien elintapasairauksien taustalla.
Ei-hapettavalle aineenvaihduntareitille päätyneiden lipidien liiallinen määrä kardiomyosyyteissä johtaa myrkyllisten lipidilajien (lipotoksiinien) kertymiseen soluihin, mikä muuttaa solujen signalointia ja sydämen rakennetta.
Lipotoksiinit
Lipotoksisuus on metabolinen oireyhtymä, joka johtuu lipidivälituotteiden kertymisestä ei-rasvakudokseen. Tämä johtaa solujen toimintahäiriöihin ja solukuolemaan. Kudoksiin, joihin lipotoksisuus normaalisti vaikuttaa, kuuluvat munuaiset, maksa, sydän ja luurankolihakset.
Lipotoksisuudella uskotaan olevan huomattava merkitys sydämen vajaatoiminnassa, liikalihavuudessa ja diabeteksessa.
Normaaleissa solutoiminnoissa lipidien tuotannon ja niiden hapettumisen tai kuljetuksen välillä on tasapaino.
Lipotoksisissa soluissa tuotettujen lipidien määrän ja energian tuotantoon hapetettujen lipidien määrän välillä on epätasapaino. Soluuntulon jälkeen rasvahapot voidaan muuntaa erityyppisiksi lipideiksi varastointia varten.
Rasvan yleinen varastomuoto, eli triglyseridi koostuu kolmesta glyserolimolekyyliin sitoutuneesta rasvahaposta, ja sitä pidetään neutraalimpana ja vaarattomimpana solunsisäisenä lipidivarastona.
Vaihtoehtoisesti rasvahapot voidaan muuntaa lipidivälituotteiksi, kuten diasyyliglyseroliksi, keramideiksi ja rasva-asyyli-CoA:ksi.
Nämä lipidivälituotteet voivat heikentää solun toimintaa, jota kutsutaan lipotoksisuudeksi
Adiposyytit, solut, jotka normaalisti toimivat kehon lipidivarastona, pystyvät käsittelemään ylimääräisiä lipidejä. Liian suuri lipidien määrä ylikuormittaa soluja ja aiheuttaa lipidien leviämisen ei-rasvasoluihin, joilla ei ole rasvoille tarvittavaa varastotilaa.
Kun ei-rasvasolujen varastointikapasiteetti ylitetään, seurauksena on solujen toimintahäiriö ja / tai solukuolema. Mekanismia, jolla lipotoksisuus aiheuttaa solun kuoleman ja toimintahäiriöitä, ei tunneta hyvin. Apoptoosin syy ja solun toimintahäiriön laajuus liittyvät solutyyppiin sekä ylimääräisten lipidien tyyppiin ja määrään.
Lihavuuden syy-vaikutus lipotoksisuudessa on kiistanalainen aihe. Jotkut tutkijat väittävät, että lihavuudella on suojaavia vaikutuksia lipotoksisuutta vastaan, koska se johtaa ylimääräiseen rasvakudokseen, johon voidaan varastoida ylimääräisiä lipidejä. Toiset väittävät, että lihavuus on lipotoksisuuden riskitekijä. Molemmat osapuolet myöntävät, että runsasrasvainen ruokavalio lisää lipotoksisten solujen määrää.
Henkilöt, joilla on paljon lipotoksisia soluja, sairastuvat yleensä sekä leptiini- että insuliiniresistenssiin. Tälle korrelaatiolle ei kuitenkaan ole löydetty selvää syy-mekanismia.
Häiriöt useilla solun signalointireiteillä, kuten mitokondrioiden toimintahäiriöissä ja endoplasmisen verkkokalvon stressissä, on liitetty lipotoksisuuteen.
Välittäjien, kuten reaktiivisten happilajien (ROS), typpioksidin (NO), keramidin, fosfatidyyli-inositoli-3-kinaasin, diasyyliglyserolin (DAG), PPAR-ydinreseptorien ligandien, leptiinin, on ehdotettu edistävän näitä lipotoksisia vaikutuksia ja lisäävän solujen apoptoosinopeutta.
Insuliiniresistenssi solutasolla
Insuliini vaikuttaa useissa aineenvaihduntaprosesseissa ja toimii signalointijärjestelmänä, joka mahdollistaa tasapainon ravinteiden tarjonnan ja tarpeen välillä.
Insuliiniresistenssissä kohdesolut eivät reagoi veresssä kiertävän insuliinin tavanomaisiin tasoihin, joten normaalia vastetta varten tarvitaan suurempia insuliinipitoisuuksia.
Insuliiniresistentti tila määritellään glukoosin imeytymisen heikkenemisenä lihaksissa ja maksan lisääntyneenä glukoneogeneesinä, mikä johtaa hyperglykemiaan, eli postbrandiaaliseen ja paastonjälkeiseen kohonneeseen verensokeriin.
Insuliiniresistenssiin liittyviä mekanismeja on selitetty monin tavoin, mutta kiistatonta tieteellistä konsensusta insuliiniresistenssin syystä ei taida olla.
Insuliiniresistenssin patogeneesi voidaan kuitenkin ryhmitellä geneettisiin virheisiin, rasvasta peräisin olevaan signaalointiin (kohdunulkoisten rasvojen kertyminen), fyysiseen passiivisuuteen, lihavuuteen ja tulehduksiin.
Insuliiniresistenssi ja geenit
Yksi lähestymistapa sairastumisen selittämiseen on insuliiniresistenssiin johtavan geneettisen virheen analysointi selvittämällä insuliinin signalointiketjuun assosioituvia ehdokasgeenejä. Insuliiniresistenssissä ja tyypin 2 diabeteksessa on havaittu useita muutoksia insuliinin signalointiin liittyvissä geeneissä.
IRS-1- ja IRS-2-geenien poikkeavuudet hiirikokeissa osoittavat, että IRS-1-hiiret ovat insuliiniresistenttejä, mutta eivät hyperglykeemisiä. Hiiret, joilta puuttuu IRS-2-geeni ovat vakavasti hyperglykeemisiä johtuen perifeerisen insuliinin toiminnan poikkeavuuksista ja β-solujen insuliinin erityksen häiriöistä.
Akt1:n häiriö hiirissä ei aiheuta merkittäviä häiriöitä aineenvaihdunnassa, kun taas hiiret, joilta Akt2 on estetty, osoittavat insuliiniresistenssiin viittaavia oireita, jotka fenotyypiltään muistuttavat läheisesti tyypin 2 diabetesta.
Muita mutaatioita, jotka on tunnistettu ja tutkittu tyypin 2 diabetekseen liittyen, ovat mutaatiot insuliinireseptorissa, PI3K:ssa, maksan glukokinaasipromoottorissa, GLUT4, glykogeenisyntaasissa ja proteiinifosfataasi-1:ssä.
Erilaisista tyypin 2 diabetekseen assosioituvista mutaatioista huolimatta, harvat henkilöt ovat diabeettisia geneettisten mutaatioiden vuoksi.
Geneettinen alttius aikuistyypin diabetekseen kuitenkin kasvattaa sairastumisriskiä. Voi myös olla useita muita geneettisiä poikkeamia, joita ei ole vielä tunnistettu ja jotka voivat vaikuttaa insuliiniresistenssin ja tyypin 2 diabeteksen patogeneesiin.
Ympäristötekijät
Lihavuuden aiheuttama vapaiden rasvahappojen (FFA) lisääntyminen verenkierrossa saattaa laukaista insuliiniresistenssin lipidien kertymisen kautta.
Tämä voi aktivoida epätyypillisen PKC:n, joka estää insuliinin solusignaloinnin ja insuliinin stimuloiman glukoosinoton luuston lihaksissa, sekä vähentää insuliinin stimuloimaa maksan glykogeenisynteesiä. Tämä voi johtaa insuliiniresistenssiin ja lisääntyneeseen glukoosin kulkeutumiseen maksassa.
Lisäksi vapaat rasvahapot laukaisevat insuliiniresistenssin aktivoimalla suoraan Tollin kaltaisen reseptorin 4 (TLR4) ja luontaisen immuunivasteen.
Lihavuus liittyy tulehdustekijöihin, joille on tunnusomaista ATM:ien (rasvakudoksen makrofagien) lisääntyminen
Tulehdustekijät lisäävät lipolyysiä ja edistävät maksan triglyseridisynteesiä ja hyperlipidemiaa lisääntyneen rasvahappoesteröinnin vuoksi.
ATM stimuloi tulehdussytokiineja, jotka estävät insuliinin signalointia ja nopeuttavat maksan glukoneogeneesiä sekä postbrandiaalista eli aterianjälkeistä hyperglykemiaa.
Muita insuliiniresistenssiä selittäviä mekanismeja ovat sekä mTOR- että S6K1-reittien aktivaatio. Nämä aktivaatiot aiheuttavat IRS-1: n seriinifosforylaation ja sen jälkeen IRS-1:een liittyvän PI3K-aktiivisuuden vähenemisen. On arveltu, että ravinteiden kyllästysolosuhteissa S6K1 voi säätää negatiivisesti insuliinin signalointia ja herkkyyttä.
Lisäksi IRS-1:n seriinifosforylaatiota on tutkittu eri olosuhteissa. Näyttää siltä, että mTOR-S6K1:stä riippuvaisen mekanismin lisäksi erilaiset seriinikinaasit, kuten c-Jun NH2-terminaalinen kinaasi (JNK), stressillä aktivoidut proteiinikinaasit, tuumorinekroositekijä-alfa (TNF-a) ja PKC voivat edistää IRS:n seriinifosforylaatiota aiheuttaen insuliinisignaalin voimakkuuden vähenemisen metaboliareitillä.
Lihavuuden merkitys insuliiniresistenssissa
Ihmisillä, joiden painoindeksi (BMI) on korkea (BMI ≥ 30 kg / m2), on suurempi sydän- ja verisuonitautien riski verrattuna ihmisiin, joilla on normaali BMI (BMI = 18,8–24,9 kg / m2).
Lihavuus assosioituu insuliiniresistenssiin. Molekyylimekanismi, jolla rasvan lisääntyminen selittäisi insuliiniresistenssin, on kuitenkin epäselvä; lipidien kertymisestä johtuva tulehdus, rasvahappojen hapettumisen estävä vaikutus glukoosin hapettumiseen, lipotoksiinien kertyminen ja adiposytokiinien eritys on kaikki yhdistetty paikallisen ja systeemisen insuliiniresistenssin kehittymiseen.
Lisääntyvä näyttö viittaa siihen, että rasvakoostumuksen heterogeenisuus ja rasvakudoksen jakautuminen voi olla ratkaisevan tärkeää insuliiniresistenssin ja kardiometabolisten häiriöiden kehittymisessä.
Viskeraalinen rasvakudos (VAT) assosioituu vahvasiti insuliiniresistenssin, DM2:n lisääntyvään esiintyvyyteen ja suurempaan sydän- ja verisuonitautien riskiin.
Viskeraalinen rasva liittyy tulehdusta edistävien adiposytokiinien korkeaan tuotantoon, oksidatiiviseen stressiin ja reniini-angiotensiini-aldosteronijärjestelmän (RAAS) aktivaatioon.
Krooninen energian (kalorien) liikasaanti aiheuttaa sisäelinten rasvamassan lisääntymisen, yksittäisten adiposyyttien hypertrofian ja adiposyyttien jakautumisen uusiksi rasvasoluiksi.
Rasvapitoisuuden lisääntyessä adiposyytit vapauttavat kemotaktisia tekijöitä, kuten monosyyttien kemoattraktantiproteiini-1 (MCP-1) ja tuumorinekroositekijä-a (TNFa), jotka moduloivat tulehdusvastetta rasvakudoksessa. MCP-1 aloittaa monosyyttien migraation viskeraaliseen rasvakudokseen ja edistää niiden erilaistumista makrofageiksi.
Makrofagit erittävät suuria määriä TNF-alfaa. Lipolyysi lisääntyy samalla kun insuliinin stimuloiman glukoosin kuljettaja-4 (GLUT4), triglyseridien biosynteesi ja adiposyyttien varastointi viskeraalisessa rasvakudoksessa vähenevät, mikä tämän mallin mukaan johtaa kiertävien veressä triglyseriditasojen nousuun.
Tämä tapahtuma voi johtaa toksisten rasvahappolajien (eli diasyyliglyserolin, keramidin) lipidisaostumiin rasvakudoksessa, haimassa, munuaisten verisuonissa, maksassa, luurankolihaksissa ja sydämessä, mikä johtaa epikardiaalisen rasvakudoksen (EAT) lisääntymiseen.
EAT:n kasvu aiheuttaa sydämen rasvoittumiseen ja massan lisääntymiseen molemmissa kammioissa, mikä johtaa kammion hypertrofiaan, supistumishäiriöön, apoptoosiin, fibroosiin ja heikentyneeseen vasemman kammion diastoliseen toimintaan.
Insuliiniresistenssi ja sydäntaudit
Kohonnneet LDL-tasot, tupakointi, korkea verenpaine ja tyypin 1 ja 2 diabetes ovat tunnettuja sydän- ja verisuonitautien riskitekijöitä, mutta insuliiniresistenssi, hyperglykemia ja inflammaatio voivat myös ennakoida haitallisia sydän- ja verisuonitapahtumia.
Insuliiniresistenssi liittyy aineenvaihdunnan häiriöihin, kuten hypertriglyseridemiaan sekä mataliin HDL-tasoihin. Lisäksi insuliiniresistenssiä on havaittu noin 30%:lla potilaista, joilla on diagnosoitu verenpainetauti (hypertensio).
Vuonna 1996 toteutetussa insuliiniresistenssin ateroskleroositutkimuksessa (IRAS) tutkijat osoittivat suoran yhteyden insuliiniresistenssin ja ateroskleroosin välillä. Jatkotutkimuksessa 2938 potilaan kohortissa määriteltiin insuliiniresistenssi tärkeäksi sydäninfarktin riskitekijäksi.
Vuonna 2012 tehty 65 tutkimuksen ja yhteensä 516 325 henkilön meta-analyysi, osoitti, että HOMA-indeksillä arvioituna insuliiniresistenssi ennustaa hyvin sydän- ja verisuonitauteja.
Archimedes-mallin ja 20–30-vuotiaiden nuorten diabetesta sairastamattomien aikuisten populaation seurannan perusteella tutkijat päätyivät johtopäätökseen, että insuliiniresistenssin estäminen populaatiotasolla voisi vähentää 42% sydäninfarkteista simuloidun 60 vuoden seurantajakson aikana.
Vaikka useat tutkimukset tukevat ajatusta siitä, että sydän- ja verisuonitaudit liittyvät insuliiniresistenssiin, on myös eräitä kiisteltyjä raportteja.
Insuliiniresistenssin lisäksi insuliiniresistenssiin liittyvällä kompensoivalla hyperinsulinemialla voi olla kriittinen rooli ateroskleroottisten plakkien muodostumisessa muuttamalla estrogeenireseptoreihin liittyvää geeniekspressiomallia, kuten eläinmalleissa on havaittu.
Hyperglykemia aiheuttaa muutoksia aineenvaihdunnan- ja solujen toiminnoissa: dyslipidemia (veren huono lipiditasapaino), hypertensio, endoteelin toimintahäiriöt, oksidatiivinen stressi ja muutokset sydämen aineenvaihdunnassa näyttävät liittyvän hyperglykemiaan.
Noin 50–70% sydänlihaksen tarvitsemasta ATP:stä tuotetaan (pitkäketjuisten) rasvahappojen hapetuksella ( β-oksidaatio). Glykolyysin osuus terveessä sydämessä on alle 10% ATP:n kokonaistuotannosta.
Sydän käyttää energiantuotantoon ensisijaisesti pitkäketjuisia rasvahappoja, mutta sydämellä on kyky vaihtaa toiseen energiasubstraattiin ATP:n tuottamiseksi sydämen energiantarpeen varmistamiseksi. Myös substraattikuljettimilla, GLUT4 (glukoosille) ja CD36 (rasvahapoille), on merkitys tässä substraatin käyttöasteen dynaamisessa tasapainossa.
Loukkaantumisen aikana sydän siirtyy rasvahappojen käytöstä energia-substraateina kohti glukoosia, mutta tämä metabolinen joustavuus heikentyy insuliiniresistenssin aikana, jolloin rasvahappo on ainoa polttoaineen lähde.
Tämä muutos indusoi lipidien imeytymisen ja kertymisen lisääntymistä sydämessä tuottaen lipotoksisuutta. Tässä mielessä tasapaino lipidien hajoamisen ja glukoosin hapettumisen välillä voi vähentää diabeettista kardiomyopatiaa.
Insuliiniresistenssi ja dyslipidemia
Insuliiniresistenssin ja tyypin 2 diabeteksen (diabeettinen dyslipidemia) aiheuttamalle dyslipidemialle on tunnusomaista lipidien kolmikko:
- korkeat plasman triglyseriditasot
-
matalat HDL-tasot
-
pienten tiheiden matalatiheyksisten lipoproteiinien (sdLDL) pitoisuuden kasvu sekä liiallinen aterianjälkeinen lipidemia
Hypertriglyseridemia lisää sydän- ja verisuonitautien ilmaantuvuutta miehillä 32% ja naisilla 76%.
10 038 ihmisellä, joilla oli normaali verenpaine tai pre-hypertensio, tehty tutkimus osoitti dyslipidemian olevan vahva ennuste tyypin 2 diabeteksen kehittymiselle.
Usein diabeettinen dyslipidemia kehittyy vuosia ennen tyypin 2 diabetesta, mikä viittaa siihen, että epänormaali lipidimetabolia on varhainen sydän- ja verisuonitautien indikaattori tyypin 2 diabeteksessa.
Lihavuus on maailmanlaajuinen epidemia, joka liittyy läheisesti tyypin 2 diabeteksen sekä sydän- ja verisuonitautien (CVD) kehittymiseen.
Lihavuuteen liittyvä viskeraalinen ja epikardiaalinen rasva ovat sydänsairauksien riskitekijöitä. Lihavuudella on merkittävä vaikutus lipoproteiiniprofiilin ja systeemiseen ja verisuonitulehdukseen sekä endoteelin toimintahäiriöön liittyvien tekijöiden modifioinnissa.
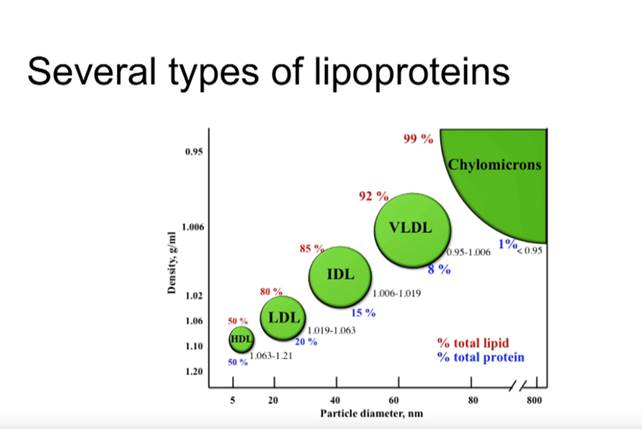
Epänormaalit lipidien ja apolipoproteiinien pitoisuudet voivat aiheuttaa muutoksia lipoproteiinihiukkasten tuotannossa, konversiossa tai kataboliassa.
Nämä muutokset voivat myötävaikuttaa liikalihavuuden lisääntyneeseen basaaliseen lipolyysiin ja rasvahappojen vapautumiseen verenkiertoon, mikä johtaa proaterogeeniseen fenotyyppiin.
Insuliiniresistenssi ja liporoteiinieprofiilien muutokset
VLDL, hyvin matalatiheyksinen lipoproteiini, kootaan ja tuotetaan substraattien saatavuuden perusteella maksassa.
Insuliini säätelee tiukasti VLDL-tuotantoa. Maksan VLDL-tuotanto indusoituu paastotilassa, mikä johtaa lisääntyneeseen VLDL-pitoisuuteen veressä.
Eri lähteistä peräisin olevien lipidien lisääntyminen, kuten verenkierron vapaat rasvahapot, triglyseridipitoisten lipoproteiinien endosytoosi ja de novo lipogeneesi mahdollistavat apoB:n translaation jälkeisen stabiloinnin ja tehostavat VLDL-hiukkasten kokoonpanoa ja eritystä.
Tämä johtaa VLDL:n ja vapaiden rasvahappojen uotantoon. Lipoproteiinit kuljettavat energiaa maksan ja rasvakudoksen välillä. Vastauksena insuliinin eritykseen VLDL-synteesi estetään plasman triglyseriditason rajoittamiseksi. Normaalisti insuliini edistää PI3K-aktivaation avulla apoB:n hajoamista, mutta insuliiniresistenssin aikana tämä hajoaminen on heikentynyt.
Yhdistelmä:
-
käytettävissä olevien rasvahappojen ylimäärä
-
apoB: n rajoitettu hajoaminen
-
apoB: n suurempi stabiloituminenVLDL-synteesin kasvu selittää insuliiniresistenssissä havaitun hypertriglyseridemian
Insuliiniresistenssi vähentää myös lipoproteiinilipaasiaktiivisuutta, joka on tärkeä VLDL-puhdistuman välittäjä. Tällä vaikutuksella on vähäinen vaikutus plasman triglyseriditasoon, vaikka se on myös mekanismi, jota myös muutetaan.
Tyypin 2 diabetesta sairastavilla potilailla VLDL:n, IDL:n ja LDL:n imeytyminen maksassa vähenee, mikä johtaa näiden lipoproteiinien viipymisaikojen pitenemiseen plasmassa.
SdLDL: n muodostuminen ja alentuneet HDL-tasot liittyvät läheisesti insuliiniresistenssiin. Ateroskleroosiriskien (ARIC) prospektiivisessa tutkimuksessa sdLDL: n plasmatasoihin liittyi sepelvaltimotaudin (CHD) riski. Lisäksi VLDL-tasot ovat tärkein LDL-koon ennustaja.
SdLDL: n muodostuminen riippuu sekä kolesteryyliesterin siirtoproteiinin (CETP) että maksan lipaasin osallistumisesta. CETP helpottaa triglyseridien siirtymistä VLDL:stä LDL:ään ja HDL:ään, tuottaa triglyseridipitoisen LDL:n ja johtaa matalaan HDL-C:hen.
Triglyseridipitoinen LDL on maksalipaasin substraatti, mikä lisää triglyseridipitoisen LDL:n lipolyysiä, mikä johtaa sdLDL: n muodostumiseen. Erilaisia mekanismeja on ehdotettu selittämään sdLDL:n lisääntynyttä aterogeenistä vaikutusta.
Näitä mekanismeja ovat:
-
alempi affiniteetti LDL-reseptoriin
-
helpotettu pääsy valtimon seinämään
-
valtimon retentio
-
suuri hapettumisherkkyys
-
pidempi puoliintumisaika
Lisääntyneet sdLDL-tasot edustavat lisääntynyttä määrää aterogeenisiä hiukkasia, mikä ei välttämättä heijastu LDL-tasoilla, koska sdLDL-hiukkaset sisältävät vähemmän kolesterolia.
HDL-hiukkasten triglyseridirikastus CETP:llä yhdistettynä maksalipaasin lipolyyttiseen vaikutukseen johtaa plasman HDL-C:n ja apoA-I:n vähenemiseen, mikä vaikuttaa pienen tiheän HDL:n muodostumiseen ja johtaa näiden hiukkasten lisääntyneeseen kataboliaan.
Vuonna 1932 ei-diabeetikoilla tehdyssä retrospektiivisessä tutkimuksessa raportoitiin, että triglyseridin ja HDL-kolesterolin suhde voi ennustaa insuliiniresistenssin ja metabolisten sairauksien todennäköisyyden. Lisäksi on osoitettu lipidien kerääntymistuotteiden ja triglyseridien glukoosindeksin korrelaatio insuliiniresistenssin ja CVD:n kanssa.
Insuliiniresistenssi johtaa lisääntyneeseen vapaiden rasvahappojen (FFA) vapautumiseen rasvasoluista. Plasman paasto-FFA:n kohonnut suhde insuliinipitoisuuteen on rasvakudoksen insuliiniresistenssi. Rasvakudoksen insuliiniresistenssin on raportoitu olevan riskitekijä aortan venttiilin kalkkeutumisessa, mikä ennustaa sydän- ja verisuonitaudit.
Insuliiniresistenssi, verenpainetauti ja endoteelin häiriöt
Kliiniset tutkimukset ovat osoittaneet, että noin 50 prosentilla hypertensiivisistä koehenkilöistä on komorbidi hyperinsulinemia tai glukoosi-intoleranssi, kun taas vähintään 80 prosentilla tyypin 2 diabetesta sairastavista potilaista on komorbidi hypertensio.
Komorbiditeetti tarkoittaa kahden tai useamman itsenäisen sairauden esiintymistä samanaikaisesti. Komorbidi sairaus tai häiriö voi olla seurausta perussairaudesta tai suorassa yhteydessä siihen. Tämä johtuu usein erilliseksi luokiteltujen ongelmien yhteisestä taustatekijästä.
Komorbidit häiriöt ovat silti usein vaikeammin hoidettavissa kuin yksittäisesti esiintyvät häiriöt, sillä hoitoa suunniteltaessa on otettava huomioon kunkin häiriön yksittäiset ominaispiirteet ja niiden yhdistelmien variaatiot. – Wikipedia
Verenpainetaudin ja diabeteksen yhdistelmää sairastavilla potilailla on selvästi korostunut sydän- ja verisuonitautien riski.
On ehdotettu, että poikkeavuudet vasodilataatiossa, verenkierrossa ja reniini-angiotensiini-aldosteronijärjestelmässä (RAAS) voivat liittyä hypertensioon ja insuliiniresistenssiin. Lisäsyynä verenpainetautiin insuliiniresistentillä potilaalla on sympaattisen hermoston yliaktiivisuus, joka edistää myosyyttien hypertrofiaa, interstitiaalista fibroosia ja heikentynyttä verisuonten supistumista, johon liittyy lisääntynyt myosyyttien apoptoosi (solukuolema).
RAAS-järjestelmässä angiotensinogeeni muuttuu reniiniksi angiotensiini I:ksi, joka sitten ACE:n (angiotensiiniä konvertoivan entsyymin) avulla muutetaan angiotensiini II:ksi (Ang II). Lopuksi Ang II vaikuttaa sekä AT1- että AT2-reseptoreihin. AT1-reseptori välittää kaikki Ang II:n klassiset vaikutukset, kuten verenpaineen nousu, verisuonten supistuminen, lisääntynyt sydämen supistuvuus, munuaisten natriumpitoisuus, veden reabsorptio ja aldosteronin vapautuminen lisämunuaisen kuoren zona glomerulosasta lisämunuaisessa.
Yksi aldosteronin rooleista on lisätä natriumin reabsorptiota distaalisessa nefronissa. Tämän vaikutuksen tarkoituksena on ylläpitää natriumtasapainoa aktivoimalla apikaalisen epiteelin natriumkanava ja basolateraalinen Na +, K + -ATPaasi. Aldosteronilla on kuitenkin vaikutuksia myös munuaisiin, verisuoniin ja sydänlihakseen, millä voi olla patofysiologisia seurauksia.
Tutkimukset ovat osoittaneet, että hyperglykemia lisää angiotensinogeenin, ACE:n ja Ang II:n transkriptiota. Tyypin 2 diabetesta sairastavilla on havaittu RAAS:n ylöspäin säätely sydän- ja verisuonijärjestelmässä. Ylössäädelty RAAS voi vaikuttaa monien diabeettisten komplikaatioiden, kuten mikrovaskulaaristen ja makrovaskulaaristen sairauksien, kehittymiseen. Lisäksi on osoitettu, että Ang II:n ylössäätely ja mineralokortikoidireseptorin aktivointi aldosteronilla voivat edistää insuliiniresistenssia aktivoimalla mTOR – S6K1-signaalinsiirtoreitti indusoimalla fosforylaatio IRS:n seriinitähteissä.
Diabeettisen kardiomyopatian kehittymiseen liittyvät mekanismit
Normaalisti insuliinin signalointi säätelee glukoosin ja lipidien aineenvaihduntaa sydämessä. Insuliiniresistenssi aiheuttaa metabolisen häiriön, joka johtaa korkeaan lipidihapetukseen ja matalaan glukoosihapetukseen.
Reniini-angiotensiini-aldosteronijärjestelmän (RAAS) aktivaatio voi aiheuttaa mitokondrioiden toimintahäiriöitä, endoplasmisen verkkokalvon stressiä ja oksidatiivista stressiä. Tämä voi johtaa epänormaaliin Ca2 + -käsittelyyn ja alhaiseen ATP-tuotantoon, mikä johtaa kardiomyosyyttien kuolemaan.
RAAS:n aktivaatio ja hyperinsulinemia voivat synergistisesti stimuloida MAPK-reittiä, jolla on verisuoniseinää vahingoittava vaikutus, koska se indusoi endoteelin toimintahäiriöitä ja edistää näin ateroskleroosia.
Tutkimuksissa on pohdittu, että insuliinin ja Ang II:n signaalinsiirtoreitit jakavat useita alavirran tehosteita ja kommunikoivat useilla tasoilla. RAAS:n (Ang II ja aldosteroni) ja yliravitsemuksen aktivaatio edistää endoteelin toimintahäiriötä lisäämällä nikotiiniamidiadeniinidinukleotidifosfaatti (NADPH) -oksidaasin välittämää ROS-tuotantoa, mekanismia, joka myös kohottaa verenpainetta.
Itse asiassa ROS johtaa redox-herkkien kinaasien, kuten S6K1:n ja mTOR:n, aktivoitumiseen, aiheuttaen insuliini-PI3K-signalointireitin, fosforylaation kautta IRS-1: n seriinitähteissä. Viimeksi mainittu mekanismi estää Akt-fosforylaation, Glut-4-translokaation sarkolemmaan ja typpioksidin (NO) tuotannon alavirran signaloinnin endoteelissä.
Lisäksi hypertensioon ja tyypin 2 diabetekseen liittyy myös endoteelin esisolujen määrän väheneminen ja toimintahäiriöt, jotka ovat kiertäviä luuytimestä peräisin olevia kantasoluja, joilla on tärkeä rooli verisuonten seinämän endoteelikorjauksessa.
Joissakin kliinisissä ja kokeellisissa tutkimuksissa on osoitettu, että RAAS-esto paransi insuliinin signalointia ja insuliiniherkkyyttä, mutta toisissa ei ole osoitettu mitään hyödyllistä vaikutusta. Tämä ero voidaan selittää joko eroilla kokeiden suunnittelussa tai tutkimuspopulaatioissa.
Yhteenvetona voidaan todeta, että TOR / S6K: n aktivointi RAAS:lla tai yliravitsemuksella johtaa insuliiniresistenssiin, jolla on metabolisia ja biologisia seurauksia. Se johtaa myös heikentyneeseen sydänlihaksen glukoosikäyttöön ja diastolisen rentoutumisen vähenemiseen.
Insuliiniresistenssi ja endoteelin toimintahäiriöt
Funktionaalisen endoteelin eheys on tärkeä verisuonten terveyselementti. Typpioksidia (NO) pidetään kehon tehokkaimpana endogeenisena vasodilataattorina (verisuonten laajentajana), ja NO:n biologisen hyötyosuuden väheneminen on endoteelin toimintahäiriön tunnusmerkki.
Endoteelin toimintahäiriö vaikuttaa sydän- ja verisuonitauteihin, kuten hypertensio, ateroskleroosi ja sepelvaltimotauti, jotka myös aiheutuvat insuliiniresistenssistä.
NO osallistuu verisuonten seinämän homeostaasiin verihiutaleiden aggregaation, leukosyyttien adheesion eston ja anti-inflammatoristen ominaisuuksien avulla. Fysiologisissa olosuhteissa insuliinin NO-tuotannon konstitutiivisella stimulaatiolla voi olla tärkeä rooli verisuonten terveyden ylläpidossa, koska se kykenee rentouttamaan verisuonen sileää lihasta.
Insuliiniresistenssitilassa insuliinin stimuloima NO-synteesi on kuitenkin heikentynyt selektiivisesti ja kompensoiva hyperinsulinemia voi aktivoida MAPK-reitin, mikä johtaa verisuonten supistumiseen, tulehdukseen, lisääntyneeseen natriumin ja veden kertymiseen, mikä johtaa verenpaineen nousuun.
Insuliiniresistenssi endoteelisoluissa lisää protromboottisia tekijöitä, tulehdusta edeltäviä markkereita ja vapaita happiradikaleja, mikä johtaa adheesiomolekyylin 1 (ICAM-1) ja verisuonisolujen adheesiomolekyylin 1 (VCAM-1) solunsisäisten tasojen nousuun.
Endoteelin toiminnan ja insuliinin aineenvaihdunnan välinen suhde on erittäin tärkeä. Tämä johtuu siitä, että insuliiniresistenssin ja endoteelin signaalihäiriöiden välinen yhteys edistää tulehdusta, häiritsee endoteelin tasapainoa vasodilataattorin ja vasokonstriktorimekanismien välillä ja lisää kardiovaskulaarista riskiä.
Tutkimuksessa, joka tehtiin ei-diabeetikoilla, joilla epäillään sydänlihasvaurioita, raportoitiin, että HOMA-IR:llä mitattu insuliiniresistenssi korreloi voimakkaasti endoteelin toimintahäiriöiden ja prognostisen arvon kanssa.
Krooninen hyperglykemia sydän- ja verisuonitaudeissa
Lisääntynyt sydän- ja verisuonitautiriski tyypin 2 diabetesta sairastavilla potilailla on tunnettu jo pitkään. Diabetesta sairastavilla potilailla on lisääntynyt verisuonten sairastuvuus ja kuolleisuus, mikä alentaa heidän elinajanodotettaan noin 5–15 vuodella.
Lisäksi on osoitettu, että sydän- ja verisuonitautien ilmaantuvuus on 2–8 kertaa suurempi tyypin 2 diabetesta sairastavilla henkilöillä kuin diabeetikoilla, ja tämä tauti aiheuttaa suurimman osan kuolemista.
Jälkimmäisen tueksi epidemiologiset ja patofysiologiset tutkimukset viittaavat siihen, että hyperglykemia (kroonisesti korkea verensokeri) voi olla suurelta osin vastuussa sydän- ja verisuonitaudeista.
Verensokerin on raportoitu ennakoivan luotettavasti ateroskleroosia, ja yli 90 mg / dl: n verensokeritaso voi johtaa ateroskleroosiin kaulavaltimossa. Pitkän aikavälin seurantatiedot tyypin 1 ja 2 diabetesta sairastavilta potilailta viittaavat siihen, että hyperglykemia on diabetekseen liittyvien sairauksien ja CVD:n riskitekijä.
Salvin et al. Havaitsi, että yhden yksikön nousu glykosyloidussa hemoglobiinissa tai HbA1C:ssä voi lisätä sydän- ja verisuonitautien riskiä 18%.
Jopa selkeän diabeteksen puuttuessa glukoosihomeostaasin heikkeneminen voi vaikuttaa sydämen autonomiseen toimintaan, mikä johtaa korkeaan sydänsairauksien riskiin.
Hyperglykemian haitalliset vaikutukset kardiomyosyyteihin voidaan selittää ilmiöllä, jota kutsutaan hyperglykeemiseksi muistiksi. Ilmiössä hyperglykeeminen stressi jatkuu pitkään verensokeritason normalisoitumisen jälkeen.
Glukoosivaihtelut ja hyperglykemia laukaisevat tulehdusreaktioita mitokondrioiden toimintahäiriöiden ja endoplasmisen verkkokalvon kautta. Tämä edistää vapaiden reaktiivisten happiradikaalien kertymistä, mikä puolestaan aiheuttaa soluvaurioita.
Hyperglykemia voi myös lisätä tulehdusta edistävien ja hyytymistä estävien tekijöiden ilmentymistä, mikä edistää leukosyyttien tarttumista endoteelisoluihin. Se indusoi apoptoosia ja heikentää typpioksidin vapautumista, mikä johtaa endoteelin toimintahäiriöön. Tästä syystä tulehdus johtaa insuliiniresistenssiin ja β-solujen toimintahäiriöihin, mikä pahentaa edelleen hyperglykemiaa.
Lisäksi glukoosivaihteluiden ja hyperglykemian tuottamat muutokset voivat aiheuttaa pitkäaikaisia epigeneettisiä modifikaatioita NF-KB: n promoottorissa, jonka näyttää vaikuttavan lisääntyneestä oksidatiivisesta stressistä.
Toinen pysyvän hyperglykemian haitallinen vaikutus on pitkälle edenneiden glykaation lopputuotteiden (AGE) sukupolvi, jotka ovat proteiinien ja lipidien ei-entsymaattisia glykaation tuotteita sokereille altistumisen seurauksena.
Yleensä AGE:t kertyvät verisuonen seinämään, mikä vaikuttaa solunulkoisen matriisin (ECM) rakenteelliseen eheyteen (tunnetaan myös nimellä matriisisoluvuorovaikutukset). Jälkimmäinen aiheuttaa endoteelivaurioita ja vähentää NO-aktiivisuutta. Kaiken kaikkiaan AGE:t edistävät diabeettisten komplikaatioiden, kuten retinopatian, nefropatian sekä sydän- ja verisuonitautien etenemistä.
Insuliiniresistenssi ja muutokset sydänmetaboliassa
Sydänseinämän paksuin kerros on sydänlihassoluista koostuva sydänlihas, joten luurankolihassolujen fysiologian tarjoama tieto auttaa selittämään sydämen aineenvaihduntaa.
Nisäkkään sydämen on supistettava lakkaamatta; mikä tarkoittaa, että optimaalisen toiminnan energiantarve on valtava. Tämä on mielenkiintoinen ilmiö, koska sydämen lihaksessa ei ole ATP-varausta.
Energiaa varastoidaan sydämen lihassoluihin kolmessa muodossa:
-
Ensimmäinen on fosfokreatiini (PCr), joka voi nopeasti luovuttaa korkean energian fosfaatit ATP:n tuottamiseksi ADP:stä. PCr: stä saatavissa oleva energia on suhteellisen vaatimaton, sitä käytetään vain erittäin nopeiden harjoitusten aikana
-
Toinen on glykogeeni, joka muodostaa solussa endogeenisen energiamuodon. Lihaksen glykogeenivarastokapasiteetti on rajallinen. Sen etuna on kuitenkin se, että se kuluttaa paljon vähemmän happea kuin rasvahapot ja on helposti saatavilla käytettäväksi polttoaineena lihaksissa.
-
Kolmas muoto on triglyseridit ja vapaat rasvahapot (FFA). Niiden hapettuminen on vähemmän tehokasta verrattuna glykogeeniin, vaikka ne sisältävät enemmän energiaa.
On yleisesti hyväksyttyä, että vapaat rasvahapot ovat hallitsevia substraatteja, joita käytetään aikuisen sydänlihaksessa ATP:n tuotantoon mitokondriossa. Siten 60-70% sydämen työn ylläpitoon tarvittavasta energiasta tulee vapaiden rasvahappojen β-oksidaatiosta. Verenkierron vapaiden rasvahappojen tasot määräävät suurelta osin vapaiden rasvahappojen imeytymisen sydämessä. Kun FFA on imeytynyt, sen metaboliaa säätelee pääasiassa transkriptiotasolla ligandiaktivoitujen transkriptiotekijöiden perhe, nimittäin peroksisomiproliferaattorin aktivaattorireseptori a (PPAR-a).
Sydämen aineenvaihduntaverkosto on ravinnon, paaston ja intensiivisen liikunnan suhteen erittäin joustava energiasubstraattien käytössä. Kardiomyosyytit, eli sydänlihassolut pystyvät käyttämään glukoosia ja laktaattia, aminohappoja, sekä ketoaineita.
Glukoosinottoa välitetään glukoosikuljettimien kautta. Kuljettimia on kahta erilaista tyyppiä, Na2 + -kytketty kantajajärjestelmä ja helpottavat glukoosikuljettimet (GLUT). GLUT1 ja GLUT4 ovat tärkeimmät toimijat sydämen glukoosikuljetuksissa.
GLUT4 edustaa tärkeintä mekanismia, joka säätelee glukoosin sisäänpääsyä sykkivässä sydämessä. GLUT1:llä on vähäisempi rooli, koska se on ensisijaisesti paikallaan plasmamembraanilla ja vastuussa sydämen glukoosin perusinsuliinista.
GLUT4:ää esiintyy enimmäkseen solunsisäisissä rakkuloissa lepovaiheissa ja se siirtyy plasmamembraaniin insuliinistimulaation yhteydessä. Imeytymisen jälkeen vapaa glukoosi fosforyloituu nopeasti glukoosi-6-fosfaatiksi (G6P), joka myöhemmin pääsee moniin metaboliareitteihin.
Glykolyysi edustaa glukoosin aineenvaihdunnan pääreittiä, joka tuottaa pyruvaatin myöhempää hapetusta varten. Glykolyysin ohella G6P voidaan myös kanavoida glykogeenisynteesiin tai pentoosifosfaattireittiin (PPP). PPP on tärkeä NADPH-lähde, jolla on kriittinen rooli solun oksidatiivisen stressin säätelyssä ja jota tarvitaan lipidisynteesiin.
Vastauksena lisääntyneeseen energiantarpeeseen sydämen lihassolut luottavat aluksi hiilihydraattien hapettumiseen. Esimerkiksi stressin, kuten liikunnan, iskemian ja patologisen hypertrofian alaisena, glukoosin substraattipreferenssiä voidaan muuttaa. Stressin aikana GLUT4-ilmentymisen nopea kasvu on varhainen adaptiivinen vaste, joka viittaa siihen, että tämän sopeutumisen fysiologisena tehtävänä on parantaa lihasten glykogeenivarastojen täydennystä.
Kun glykogeenipitoisuus on korkea, sydän käyttää ensisijaisesti glykogeenia energiasubstraatin lähteenä, mutta kun glykogeenivarastot ovat vähäisiä, se muuttuu rasvahappojen hapettumiseksi. Tämä induktio voidaan estää suurella hiilihydraattiruokavaliolla palautumisen aikana. Aineenvaihdunnan hallinta palautumisessa glykogeenitasojen avulla korostaa sen merkitystä aineenvaihdunnan lihasten varaan.
Insuliiniresistenssissä sydän on rikkaassa rasvahappo- ja glukoosiympäristössä. Ylimääräinen insuliini edistää vapaiden rasvahappojen lisääntynyttä imeytymistä sydämessä klusterin erilaistumisproteiinin 36 (CD36) säätelyn seurauksena. Se on voimakas vapaiden rasvahappojen kuljettamiseen ja säätelyyn vaikuttava proteiini. Tämä lisää solunsisäisiä rasvahappoja ja PPAR-a-ilmentymistä. Viimeksi mainittu lisää geeniekspressiota rasvahappojen hapettumisen kolmessa vaiheessa lisäämällä (1) FFA-kuljettajien synteesiä solussa, (2) proteiineja, jotka tuovat FFA:ta mitokondrioon, ja (3) entsyymejä rasvahappojen hapetuksessa.
Toisaalta glukoosin käytön eston takia kardiomyosyytteihin kertyy glykolyyttistä välituotetta, mikä indusoi glukotoksisuutta
Kun diabetes etenee tai kun sydämeen kohdistuu lisärasituksia; metabolista sopeutumista voi esiintyä, ja aineenvaihdunnan joustavuus heikkenee huomattavasti. Sydän heikentää kykyään käyttää rasvahappoja, lisää vapaiden rasvahappojen kulkeutumista ja johtaa lipidien (keramidit, diasyyliglyserolit, pitkäketjuiset asyyli-CoA:t ja asyylikarnitiinit) kertymiseen sydänlihakseen.
Tämä lipidien kertyminen voi vaikuttaa solujen kuolemaan (apoptoosiin), heikentää mitokondrioiden toimintaa, sydämen hypertrofiaa ja supistushäiriöitä. Esimerkiksi diasyyliglyseroli ja rasva-asyylikoentsyymi (CoA) indusoivat epätyypillisen PKC: n aktivaation, mikä johtaa heikentyneeseen insuliinin signalointiin.
Keramidit, jotka yhdistävät lipidien aiheuttaman tulehduksen insuliinin signaloinnin estoon, toimivat lipotoksisten signalointireittien avainkomponentteina. Toisaalta korkea lipidipitoisuus voi aiheuttaa supistushäiriöitä insuliiniresistenssistä riippumatta. Seurauksena oleva sydänlihaksen energiantuotannon vika heikentää myosyyttien supistumista ja diastolista toimintaa. Nämä muutokset aiheuttavat toiminnallisia muutoksia, jotka johtavat kardiomyopatiaan ja sydämen vajaatoimintaan.
Glukoosin puuttuessa maksassa syntyvät ketoaineet pääsevät verenkiertoon, ja elimet, kuten aivot, munuaiset, luurankolihakset ja sydän, käyttävät niitä energiasubstraatteina. Sydänlihaksen polttoaineenvaihdunnan ja bioenergian häiriöt vaikuttavat sydän- ja verisuonitauteihin, koska aikuisen sydän vaatii paljon energiaa supistumiseen.
Sydän- ja verisuonitauteissa sydämen kyky käyttää rasvahappoja, sydämen ensisijaista polttoainetta, on heikentynyt
Tässä tilanteessa sydän käyttää vaihtoehtoisia reittejä, kuten ketoaineita, polttoaineena ATP:n tuotannossa. Edelleen kiistellään siitä, kuinka hyvin sydänlihas sopeutuu tähän energiasubstraatin muutokseen.
Viime aikoina on osoitettu, että syklinen ketoaineiden käyttö energiasubstraattina ylläpitää sydämen nuoruutta vanhoilla hiirillä. Toisaalta on raportoitu, että isokalorinen (yhtäläisen energian sisältävä) ketogeeninen ruokavalio (hyvin vähän hiilihydraatteja ja runsaasti rasvoja ja / tai proteiineja) pidentää elinikää.
Ketogeenisen ruokavalion vaikutus voidaan välittää tukahduttamalla pitkäikäisyyteen liittyvä insuliinin signalointi ja mTOR-reitti sekä aktivoimalla peroksisomiproliferaattorilla aktivoitunut reseptori a (PPARa), pääsäädin, joka kytkee päälle ketogeneesiin osallistuvat geenit.
Useat raportit viittaavat siihen, että ketogeeniseen ruokavalioon voi liittyä sydän- ja verisuonitautien riskitekijöiden, kuten liikalihavuuden, diabeteksen, valtimoverenpaineen ja kolesterolitasojen, esiintyvyyden väheneminen. Toisaalta monien raporttien mukaan sydän- ja verisuonitautien riskitekijöiden väheneminen vastasi painonlaskua käytetystä ruokavaliosta riippumatta.
Muut tekijät, jotka vaikuttavat diabeettisen kardiomyopatian patogeneesiin
Muita diabeettisen kardiomyopatian patogeneesiin vaikuttavia tekijöitä ovat metaboliset poikkeavuudet, joihin liittyy mitokondrioiden toimintahäiriöitä, endoplasman verkkokalvon stressiä ja heikentynyttä Ca2 + -käsittelyä. Reaktiivisten happiradikaalien (ROS) liiallinen tuotanto johtaa proteiini-, DNA- ja kalvovaurioihin. Lisäksi ROS:lla on haitallisia vaikutuksia endoplasmiseen verkkokalvoon.
Oksidatiivinen stressi ja endoplasman verkkokalvon stressi voivat aiheuttaa solunsisäisen Ca2 + -tason nousun. Mitokondrioiden ylimääräinen Ca2 +:n otto johtaa Ca2 +:n ylikuormitukseen ja mitokondrioiden läpäisevyyden siirtymähuokosten avautumiseen, mikä johtaa myöhemmin mitokondrioiden toimintahäiriöihin ja solujen apoptoosiin. Tämä vaikuttaa myös diabeettisen kardiomyopatian patogeneesiin.
Sokerit ohjaavat sepelvaltimotautia insuliiniresistenssin ja hyperinsulinemian kautta: uusi paradigma
‘I know of no single acceptable study that shows a high intake of sugar in a population that is almost entirely free from heart disease.’1—John Yudkin
Sepelvaltimotauti (CHD) aiheuttaa joka kuudennen kuolemantapauksen Yhdysvalloissa. Sepelvaltimotauti johtaa lopulta akuuttiin infarktiin (MI). Yhdysvalloissa tapahtuu vuosittain melkein miljoona akuuttia sydäninfarktia, ja noin 15% potilaista kuolee sydäninfarktin seurauksena.
Oireeton hyperglykemia on sydän- ja verisuonitautien ja infarktin riskitekijä. Hyperglykemia voi kehittyä akuutin infarktin aikana myös potilaille, joilla ei ole diabetesta. Hyperglykemian voi aiheuttaa insuliinin erityksen väheneminen, insuliiniresistenssin kehittyminen sekä katekoliamiinien (adrenaliini, noradrenaliini ja dopamiini), kortisolin ja kasvuhormonin lisääntyminen.
Monilla infarktipotilailla on diagnosoitu tai diagnosoimaton diabetes, jossa akuutti stressi pahentaa diabeettista tilaa ja johtaa hyperglykemiaan. Erään tutkimuksen mukaan 73%:lla akuutin infarktin saaneista potilaista oli epänormaali glukoositoleranssi ja 50%:lla diabetes. 6 kuukauden kuluttua infarktista 43%:lla oli epänormaali glukoositoleranssi, mikä on noin kolminkertainen määrä terveisiin verrokkeihin nähden.
Hyperglykemia ei siis näytä olevan akuutti tai väliaikainen löydös potilailla, joilla on ollut infarkti. Monilla potilaalla on havaittavissa jatkuvasti epänormaali glukoositoleranssi.
Whitehall-tutkimus (prospektiivinen kohorttitutkimus), johon osallistui 18 403 potilasta, osoitti, että verensokeri 2 tuntia suun kautta otetun glukoositoleranssitestin jälkeen liittyi iän mukaan mukautettuun kardiovaskulaariseen kuolleisuuteen 7,5 vuoden jälkeen.
Ei-diabeetikoilla 2 tunnin veri glukoosipitoisuus 96 mg / dl tai korkeampi liittyi kaksinkertaiseeb sydän- ja verisuonitautien kuolleisuuden riskiin.
Suun kautta otettavaan glukoosin aiheuttama korkea insuliinivaste on todettu perifeeristen-, aivo- ja sepelvaltimoiden ateroskleroosipotilailla.
Australian Busseltonissa tehdyssä tutkimuksessa, insuliinipitoisuudet tunnin kuluttua 50 g:n glukoosiannoksen jälkeen korreloivat merkittävästi 60-vuotiaiden ja sitä vanhempien miesten 6 vuoden CVD-ilmaantuvuuteen ja 12-vuotiseen CVD-kuolleisuuteen.
Sekä Helsingin poliisitutkimuksessa että Pariisin siviilipalveluksessa olevien tutkimuksessa paastotilassa otetun 75 g tai 90 g oraalisen glukoosiannoksen jälkeinen insuliinipitoisuuden kasvu korreloi infarkti- ja sydäntautikuolemiin 5 vuotta myöhemmin 30–59-vuotiailla miehillä.
Insuliini-glukoosisuhteella oli selvin yhteys sydän- ja verisuonitauteihin. Kaikissa kolmessa tutkimuksessa insuliinin suhde sydän- ja verisuonitautiin oli riippumaton muista muuttujista, kuten lipidit, verenpaine ja verensokeri.
Puhdistetun sokerin aiheuttama insuliinivaste on jopa tärkkelyksen insuliinivastetta suurempi. Tämä on vakuuttava osoitus siitä, että lisättyjen sokereiden (sakkaroosi sekä runsaasti fruktoosia sisältävä maissisiirappi) liiallinen käyttö voi johtaa lisääntyneeseen sydän- ja verisuonitautieriskiin kohonneiden insuliinitasojen kautta.
Insuliinin ja hiilihydraattehin rooliin aterogeneesissä viittaava näyttö on vahva. Tämä järjestelmä yhdistää ateroskleroosin diabetekseen, lihavuuteen, hyperlipidemiaan ja mahdollisesti verenpainetautiin. (Stout ja Vallance-Owen)
Yli 50 vuoden ajan on ollut tiedossa, että hyperkolesterolemiaa ja hyperlipatemiaa sairastavilla ihmisillä on yleensä epänormaali hiilihydraattien aineenvaihdunta. Kohonneet insuliinitasot johtavat usein hyperlipidemiaan.
Insuliinin on todettu lisäävän lipogeneesiä (glukoosin muuttamista triglyserideiksi, eli varastorasvaksi) ja stimuloivan sileiden lihassolujen lisääntymistä. Hyperinsulinemia on itsenäinen sydänsairauksien riskitekijä. Insuliiniresistenssi ennustaa hyvin kardiovaskulaarisia riskejä. Näin ollen kaikki ruokavalion tekijät, jotka heikentävät glukoosinsietokykyä tai edistävät insuliiniresistenssiä, lisäävät todennäköisesti myös akuutin infarktin, sydän- ja verisuonitautien (CHD) ja CHD-kuolleisuuden riskiä.
Runsaasti lisättyä sokeria (erityisesti teollisesti käsiteltyä fruktoosia) sisältävä ruokavalio johtaa insuliiniresistenssiin. Lisättyjen sokereiden liiallinen kulutus on vaikuttava tekijä CHD- ja CVD-kuolleisuudessa.
Ihmisillä, joiden ruokavaliossa päivittäisestä energiasta alle 10% saadaan lisätyistä sokereista, on lähes kolme kertaa pienempi sydän- ja verisuonitautien riski, kuin ihmisillä, joiden ruokavalio sisältää 25% tai enemmän energiaa lisätyistä sokereista.
Eläin- ja ihmistutkimuksissa on havaittu, että tärkkelyksen, glukoosin tai molempien yhdistelmän isokalorinen (yhtäläisen energiapitoisuuden) korvaaminen sakkaroosilla tai fruktoosilla lisää paastoinsuliinipitoisuutta, heikentää insuliiniherkkyyttä, lisää paastoglukoosipitoisuutta, lisää glukoosi- ja insuliinivasteita sakkaroosikuormitukseen ja vähentää solun insuliiniin sitoutumista.
Toisin sanoen kalori on kalori, mutta lisättyjen sokereiden kulutus on selvästi haitallisempaa kuin tärkkelys ja/tai glukoosi, koska lisätyt sokerit heikentävät insuliiniherkkyyttä ja glukoositoleranssia.
Rottien ruokinta sakkaroosilla johtaa heikentyneeseen glukoositoleranssiin ja rasvakudokseen, joka on vähemmän herkkä insuliinin vaikutuksille.Eläimiltä ja ihmisiltä saadut tiedot viittaavat siis siihen, että lisättyjen sokereiden liiallinen kulutus johtaa insuliiniresistenssiin ja hyperinsulinemiaan.
Akuutin sydäninfarktin aikana sydän siirtyy ensisijaisesta rasvahappojen käytöstä energiana glukoosin käyttämiseen. Koska insuliini helpottaa glukoosinottoa soluihin, insuliiniresistenttien potilaiden ennuste on huonompi.
Insuliiniresistenssin aste liittyy sydäninfarktin vakavuuteen. Sydäninfarktin saanet diabeetikot kuolevat todennäköisemmin kuin ei-diabeetikot. Runsas lisättyä sokeria sisältävä ruokavalio edistää insuliiniresistenssiä ja diabetesta, ja voi siten johtaa sydäninfarkteihin ja lisätä sydänkuolleisuuden riskiä.
Diabeetikoilla on suurempi sydäninfarktin, sydäntautien ja sydänkuolleisuuden riski kuin diabetesta sairastamattomilla. Tätä riskiä ei selitä muut muuttujat, kuten tupakointi, kolesteroli, verenpaine tai kehon rasvan jakautuminen.
Potilailla, joilla on diagnosoitu äskettäin diabetes, on myös suurempi sydäninfarktin riski. Diabeetikoilla on enemmän sepelvaltimoiden ateroskleroosia kuin ei-diabeetikoilla. Erityisesti vasemman sepelvaltimon kapeneminen ja parantuneiden transmuraalisten ventrikulaaristen arpien esiintymistiheys on diabeetikoilla verrokkeja yleisempää.
Framingham-tutkimus osoitti, että diabeetikoilla on likimäärin kolminkertainen riski kuolla sydän- ja verisuonitautiin verrattuna väestöön keskimäärin, sekä lisääntynyt aivohalvauksen, sydänsairauden ja perifeerisen valtimosairauden riski.
Korkeampi verenpaine tai korkeammat lipoproteiiniarvot eivät selitä sydänsairauden lisääntynyttä esiintyvyyttä diabeetikoilla
Runsaasti lisättyä sokeria sisältävän ruokavalion on osoitettu lisäävän diabeteksen esiintyvyyttä, kun taas vähäisempi sokerin saanti assosioituu pienempään diabetesriskiin.
Lisätyt sokerit edistävät insuliiniresistenssiä. Akuutin sydäninfarktiin kokevat ovat todennäköisemmin insuliiniresistenttejä. Lisättyjen sokereiden liiallinen kulutus on sydän- ja verisuonitautien riskitekijä.
Me olemme kasvaneet uskossa, että kohonnut kolesteroli selittää sydän- ja verisuonitautien syntymekanismia, mutta se ei suinkaan ole ainoa tai ehkä edes merkittävin riskitekijä.
Sydänsasairauksissa havaitaan kolesterolin ohella monia muita kliinisiä poikkeavuuksia, kuten kohonnut glukoosi (hyperglykemia), insuliini (hyperinsulinemia), triglyseridit, virtsahappo ja matalat korkean tiheyden lipoproteiinikolesterolin (HDL) tasot. Kaikki nämä CHD-riskitekijät aiheutuvat tai pahenevat ihmisillä ja eläimillä, kun he noudattavat runsaasti sokeria sisältävää ruokavaliota.
Lisättyjen sokereiden liiallinen kulutus on tärkein sydänsairauksien aiheuttaja
Korkean glykeemisen kuorman ruokavalion noudattaminen vain muutaman viikon ajan kasvatti sydäntautien ja perifeeristen verisuonitautien riskitekijöitä kolmanneksella tutkimukseen osallistuneista.
Tämä viittaa siihen, että sokerin liiallinen kulutus ja sitä seuraava insuliiniresistenssi ja / tai hyperinsulinemia lisäävät sydän- ja verisuonitautien sekä monien muiden sairauksien, kuten verenpainetaudin, diabeteksen, lihavuuden ja kihdin riskiä.
Mielenkiintoista on, että tupakoinnin, joka on sydänsairauksien riskitekijä, on todettu aiheuttavan hyperinsuliniaa, mikä viittaa siihen, että sekä lisättyjen sokereiden liiallinen kulutus että tupakointi altistavat sydänsairauksille samalla mekanismilla (hyperinsulinemian kautta; vaikka molemmat aiheuttavat myös inflammaatiota, oksidatiivista stressiä ja lisääntynyttä verihiutaleiden puuroutumista).
Viimeisten 200 vuoden aikana keskimääräinen lisättyjen sokerien saanti on kasvanut vajaasta kahdesta kilosta lähes 60 kiloon vuodessa. Se, että diabeetikoilla on kasvanut okklusiivisen valtimosairauden riski, ja että ei-diabeetikoilla, joilla on verisuonisairaus, on myös selvästi kohonneet insuliinitasot, viittaa siihen, että insuliiniresistenssilla on merkittävä vaikutus sydäntautien patogeneesissä.
Kun otetaan huomioon, että runsaasti lisättyä sokeria sisältävä ruokavalio voi aiheuttaa ihmisille insuliiniresistenssin ja hyperinsulinemian, ja toisaalta lisättyjen sokerien vähentäminen voi parantaa näitä aineenvaihdunnan häiriöitä, on vakuuttavaa näyttöä siitä, että lisättyjen sokereiden (runsaasti fruktoosia sisältävä maissisiirappi ja sakkaroosi) runsas saanti on keskeinen sydäntautien vaikuttaja.
Puhdistettu sokeri verrattuna rasvaan, tärkkelykseen, glukoosiin tai tärkkelyksen ja glukoosin yhdistelmään, edistää suurempia haittoja ihmisen glukoositoleranssille ja insuliiniherkkyydelle.
Vieläkin uskotaan, että tärkein ruokavalion sydän- ja verisuonitautien riskiä kasvattava yksittäinen ravintoaine on tyydyttynyt rasva. Lisättyjen sokerien (sakkaroosi- tai pöytäsokeri ja runsasfruktoosinen maissisiirappi) liialliseen kulutukseen liittyy myös lisääntynyt sydän- ja verisuonitautien riski sekä sydän- ja verisuonitaudeista johtuva kuolleisuus.
Korkean glykeemisen kuorman lisättyjä sokereita sisältävä ruokavalio kasvattaa sydäntautien riskitekijöitä jo muutaman viikon aikana. Vielä tärkeämpää on, että ruokavalion, jossa on vähän lisättyjä sokereita ja puhdistettuja hiilihydraatteja, on havaittu korjaavan nämä aineenvaihduntahäiriöt.
Todisteet osoittavat, että lisätyt sokerit kasvattavat sydän- ja verisuonitautien riskiä enemmän kuin tyydyttyneet rasvat, jotka itse asiassa ovat viimeisimpien tutkimusten mukaan sydänterveyden kannalta neutraaleja. Asiasta on siis vähintään kaksi perusteltua mielipidettä. Sokereiden haitallisuutta korostava näyttö on lisääntynyt ja tyydyttyneiden rasvojen maine on vastaavasti puhdistunut.
 Lihavuuden yleistyminen
Lihavuuden yleistyminen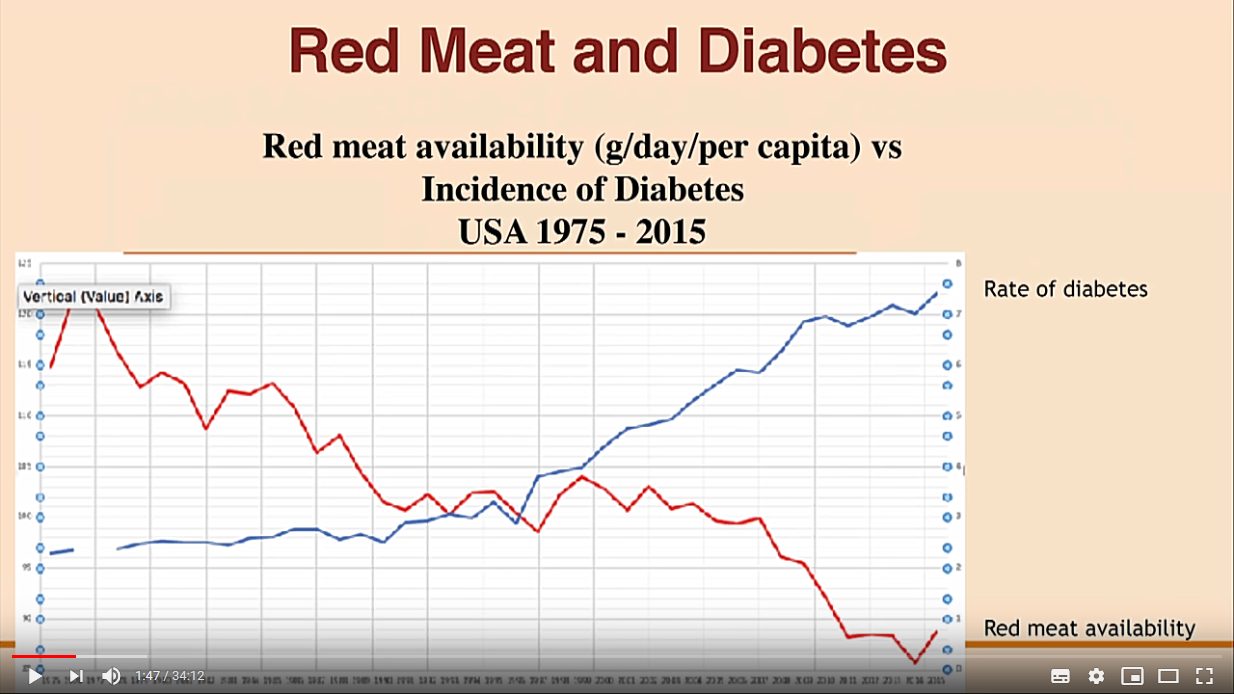

 60– ja 70-luvuilla rasvojen terveysvaikutuksista tehtiin kiinnostavia kontrolloituja satunnaistettuja tutkimuksia (CRT). Nämä tutkimukset eivät kuitenkaan mahtuneet vallitsevaan hypoteesiin kovien rasvojen haitallisuudesta, joten ne niiden annettiin unohtua.
60– ja 70-luvuilla rasvojen terveysvaikutuksista tehtiin kiinnostavia kontrolloituja satunnaistettuja tutkimuksia (CRT). Nämä tutkimukset eivät kuitenkaan mahtuneet vallitsevaan hypoteesiin kovien rasvojen haitallisuudesta, joten ne niiden annettiin unohtua.



