90 päivän ketohaaste! Sokeri- ja rasva-arvot paranevat 90 päivän ketogeenisellä dieetillä
Sukelsin ketoosiin melkein vuosi sitten. Tähän vuoteen on mahtunut monta syrjähyppyä ja horjahdusta, mutta myös ihmeellisiä onnistumisia painon, verensokerin ja verenpaineen osalta. Kesän harkitsemattomien ruoka- ja bissejammailujen seurauksena painoni kääntyi kasvuun ja energiatasoni romahtivat. Viimeisen kuukauden aikana olen ottanut itseäni niskasta kiinni ja palannut ketogeenisen ruokavalion perusteisiin. Paino on sen jälkeen pudonnut nopeasti alle 8o kilon. Energiaa minussa on on taas kuin pienessä kylässä.
Pankkitili on yhtä tyhjä kuin tyhjyyttään ammottava jääkaappi, mutta minua se hymyilyttää, sillä taivaarannassa näy huolen häivääkään. Tällaisen mielialan voi selittää kaksi asiaa: a) olen flipannut viri-viri-tööt-tööt-maailmaan, tai
b) metabolinen muutos glukoosiaineenvaihdunnasta rasva-aineenvaihduntaan vaikuttaa fysiologisesti myös mielialaan, koska:
- ketooosin stimuloima autofagia siivoaa neuroneita haitallisista kuona-aineista ja tehostaa hermosolujen energiantuotantoa,
- lipolyysi vapauttaa tasaisesti vapaita rasvahappoja energiasubstraateiksi solujen käyttöön,
- sydän työskentelee tyytyväisesti rasvahapoilla ja aivosolut betahydroksibutyraatilla,
- metabolinen muutos syntetisoi keskushermostoa yliaktiivisena pitävästä glutamaatista keskushermostoa rauhoittavaa GABAa
- stressihormoni-kortisolin tasot laskevat ketogeenisellä ruokavaliolla
Ketogeeninen ruokavalio parantaa tutkimusten ja omien kokemusteni perusteella veren sokeri-, insuliini- ja rasva-arvoja. Hiilihydraatteja rajoittamalla verenpaine ja paino putoavat. Oma verenpaineeni oli aamulla 111/73/78, verensokeri 5,4 mmol/l ja paino 79,0 kg.
Vähähiilihydraattiset ruokavaliot ovat tehokkaita strategioita insuliiniresistenssin parantamiseksi. Insuliiniherkkyyden heikkeneminen on merkki insuliiniresistenssistä, joka on tyypin 2 diabeteksen ja monien muiden elintapasairauksien taustalla piilotteleva kantasyy.
Tässä kuvattujen kliinisten potilaskertomusten tarkoituksena on osoittaa ne merkitykselliset muutokset, joita havaittiin 90 päivän vähähiilihydraattisten (LCHF) ketogeenisten ruokavalion noudattamisen seurauksena18-45 vuotiailla naispuolisilla tyypin 2 diabeetikoilla.
Yksitoista naista, joiden painoindeksi oli keskimäärin 36,3, ja joilla oli hiljattain diagnosoitu yli 6,5% (8,9%) HbA1c-tyypin perusteella tyypin 2 diabetes, osallistui kontrolloituun ruokavaliointerventioon, jossa ruokavalion hiilihydraatit rajoitettiin alle 30 grammaan päivässä 90 päivän ajaksi.
| Glykatoitunut hemoglobiini (A1C, HbA1c, Hb1c, HGA1C) on punasoluissa esiintyvä hemoglobiinin (Hb) muoto, jonka pitoisuuden mittausta veressä käytetään arvioimaan kolmen viimeisimmän kuukauden aikaista keskimääräistä verensokeritasoa. Testin keskiarvo on rajoittunut kolmeen kuukauteen, sillä normaalia hemoglobiinia ja A1C:tä sisältävien punasolujen elinikä ihmisissä on noin 4 kuukautta. |
| A1C-koetta voidaan käyttää esimerkiksi diabeteksen totemiseen. A1C:tä muodostuu diabeteksessa ilmenevässä hyperglykemiassa normaalia enemmän hemoglobiinin reagoidessa hallitsemattomasti veren glukoosin kanssa ei-entsymaattisen glykaation kautta. A1C-testit mittaavat hemoglobiiniin sitoutuneen beta-N-1-deoksi fruktosyylin määrää. |
| A1C:n yksikkönä käytetään usein millimoolia beta-N-1-deoksi fruktosyyliä sitovaa hemoglobiini A:ta (A1C) per mooli normaalia hemoglobiini A:ta. Yksikkö on siis mmol/mol. A1C-arvon mittaus ei edellytä paastoamista. |
| Suomessa normaali A1C-arvo eli viitearvo on kaikille ihmisryhmille 20–42 mmol/mol. 42–482 mmol/mol voi merkitä sitä, että henkilö potee esidiabetesta. Arvo, joka on yli 482 mmol/mol, merkitsee sitä, että henkilöllä on ehkä tyypin 1 diabetes tai tyypin 2 diabetes. Diabetes voidaan tarvittaessa varmentaa esimerkiksi A1C-testistä erillisellä sokerirasituskokeella. Nieltyä diabeteslääkitystä käyttävien tulisi pyrkiä A1C-arvoon, joka on alle 532 mmol/mol ja insuliinia käyttävien arvoon, joka on 53–582 mmol/mol. 69–752 mmol/mol taas merkitsee taas sitä, että potilaan diabetes on huonosti hallinnassa. – Wikipedia |
Intervention tavoitteena oli määrittää HbA1c:n muutosaste, kun taas toissijaisiin tuloksiin sisältyi muutokset painossa, verenpaineessa ja veren rasva-arvoissa.
Vapaaehtoisten paino laski 90 vuorokauden ketogeenisen ruokavalion noudattamisen aikana merkittävästi. Myös systolinen ja diastolinen verenpaine laskivat. HbA1c putosi lähtöarvosta keskimäärin terveeseen 5,6-tasoon.
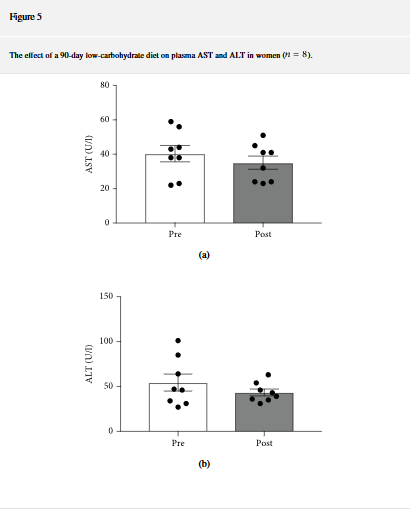
Koehenkilöiden veren rasva-arvoista suurin osa, kuten HDL-kolesteroli, triglyseridit ja TG: HDL -suhde muuttuivat parempaan suuntaan. Koehenkilöiden LDL-kolesterolin pitoisuus ei muuttunut merkittävästi. Maksan terveyden markkereiden, AST:n ja ALAT:n muutoksia mitattiin kahdeksalta potilaalta, eivätkä ne osoittaneet merkittäviä muutoksia.
Nämä havainnot viittaavat siihen, että lyhytaikainen ketogeeninen interventio, joka korostaa proteiinia ja rasvaa ruokavalion hiilihydraattien kustannuksella, voi kääntää diabeteksen diagnoosin, kuten HbA1c määrittelee. Veren sokeri- ja rasva-arvojen lisäksi interventio alensi koehenkilöiden painoa ja verenpainetta.
1. Johdanto
Insuliiniresistenssi on globaalisti yleisin aineenvaihduntasairaus [1]. Hyperglykemia, hyperinsulinemia ja insuliiniresistenssi vaikuttavat lähes kaikkien elintapasairauksien taustalla. Insuliiniresistenssia sairastaa jo puolet aikuisista Yhdysvalloissa [2], Aasiassa [3] ja Lähi-idän maissa [4].
Hämmästyttävän yleisyytensä lisäksi insuliiniresistenssi lisää monien kroonisten sairauksien, kuten sydän- ja verisuonitautien [5], dementian [6] ja syövän riskiä.
Insuliiniresistenssin maailmanlaajuinen yleistyminen pitäisi pysäyttää pikaisesti. Insuliiniresistenssi on sairastuneelle inhimillinen taakka, mutta se rasittaa myös yhteiskuntaa, taloutta ja terveydenhoidon kantokykyä. On aika miettiä strategioita tämän epidemian tukahduttamiseksi.
Metabolisen oireyhtymän, aikuistyypin diabeteksen, alkoholista riippumattoman rasvamaksan sekä sydän-ja verisuonitautien ja monien muiden insuliiniresistenssiin liittyvien vaivojen vähentäminen väestötasolla säästää yhteiskunnalle pitkän pennin.
Insuliiniresistenssistä johtuvien aineenvaihduntasairauksien terapiaan käytetään laajasti erilaisia sosiaali- ja terveyspalveluja sekä farmakologisia hoitoja. Monet lääkehoidot pyrkivät estämään glukoosin imeytymistä ohutsuolesta verenkiertoon (esim. α-glukosidaasin estäjät) tai lisäämään glukoosin erittymistä munuaisin (esim. SGLT2-estäjät, jotka vähentävät glukoosin takaisinimeytymistä munuaisissa, jolloin glukoosia poistuu virtsan mukana).
Lääkehoidoilla on lähes aina sivuvaikutuksia. Niin myös α-glukosidaasilla ja SGLT2-estäjillä, jotka voivat aiheuttaa potilaille mm. osmoottista ripulia [8] ja virtsatieinfektioita [9].
Nämä lääkkeet kyllä laskevat veren sokeri- ja insuliinipitoisuutta, millä on suotuisia vaikutuksia insuliiniresistenssiin, mutta lääkkeiden sivuoireet eivät houkuta lääkekuurin täsmälliseen noudattamiseen, etenkään, jos aikuistyypin diabetes ja insuliiniresistenssi eivät oireile.
Farmakologisisesti verensokeria lasketaan estämällä glukoosin imeytymistä tai edistämällä glukoosin poistumista virtsan mukana. Järkevä tapa hoitaa insuliiniresistenssia ja siihen liittyviä sairauksia on ksinkertaisesti vähentää glukoosin saantia.
Vaihtoehto lääkehoidoille on elämäntaparemppa, jossa glukoosinlähteitä, eli hiilihydraatteja rajoitetaan tuntuvasti. Tämä lähestymistapa on tunnettu menetelmä insuliiniresistenssin hoitona [10].
Ravinnon sisältämät hiilihydraatit kohottavat verensokeria ja veren insuliinipitoisuutta. Tehokas ruokavaliostrategia rakentuu proteiinien ja rasvojen varaan. Niillä on vain vähäinen vaikutus veren sokeri- ja insuliiniitasoihin [11]. Tämän pilottitutkimuksen tarkoituksena oli selvittää, riittääkö 90 päivän vähähiilihydraattinen ruokavalion muutos parantamaan insuliiniresistenssin ja tyypin 2 diabeteksen markkereita.
2. Materiaalit ja menetelmät
2.1. Osallistujat
Koehenkilöitä rekrytoitiin Provon ja Oremin alueelta Utahin osavaltiossa. Retrospektiivisen kaavion tarkastelun hyväksyi Brigham Youngin yliopiston institutionaalinen arviointilautakunta.
Sisältökriteerit olivat ikä 18-45 vuotta ja äskettäin diagnosoitu tyypin 2 diabetes mellitus HbA1c: n perusteella (6,5% tai korkeampi), samoin kuin kaikki metabolisen oireyhtymän piirteet, mukaan lukien hypertensio ja dyslipidemia.
Poissulkemisperusteisiin sisältyivät lääkkeiden käyttö, aiemmat sairausdiagnoosit, raskaus ja hoitotyö. Lähtötason verikokeet tehtiin seulontakäynnillä. Koehenkilöt eivät saaneet rahallista korvausta.
2.2. Interventio
Koehenkilöille tarjottiin henkilökohtaista tukea ja opetusmateriaalia viikkokäynneillä koko interventiotutkimuksen ajan. Viikkokäynnit koostuivat ruokavalion noudattamisen seuraamisesta ja ketonimittauksista.
Ketogeenisen ruokavalion noudattaminen vahvistettiin viikoittaisilla testeillä sen varmistamiseksi, että plasman ketonit (Precision Xtra, Abbott, Chicago IL) olivat vähintään 0,5 mmol / l (taulukko 1; keskiarvo viikolla 1; keskiarvo viikolla 12:) .
Oppimateriaalit, kuten luettelo vältettävistä ja sallituista elintarvikkeista sekä henkilökohtaiset käynnit koehenkilöiden luona suunniteltiin lisäämään koehenkilöiden ymmärrystä vähän hiilihydraatteja ja runsaasti rasvaa sisältävän ruokavalion perusteista ja tukemaan ketogeenisen ruokavalion noudattamista.
Koehenkilöitä kannustettiin noudattamaan yksinkertaista sääntöä ”kontrolloi hiilihydraatit” (noin 5 % päivittäisestä energiasta), ”priorisoi proteiinit” (noin 20-25 % päivittäisestä energiasta) ja ”täytä rasvalla” (noin 70-75% päivittäisestä energiasta).
Ruokavalion keskeinen osa oli rajoittaa hiilihydraattien saantia enintään 30 grammaan päivässä. Koehenkilöitä kannustettiin syömään vapaasti proteiinia ja rasvaa: liha, munat ja juusto kuuluivat suositeltuihin ravintoaineisiin. Koehenkilöitä kannustettiin liikkumaan koko tutkimuksen ajan.
Taulukko 1
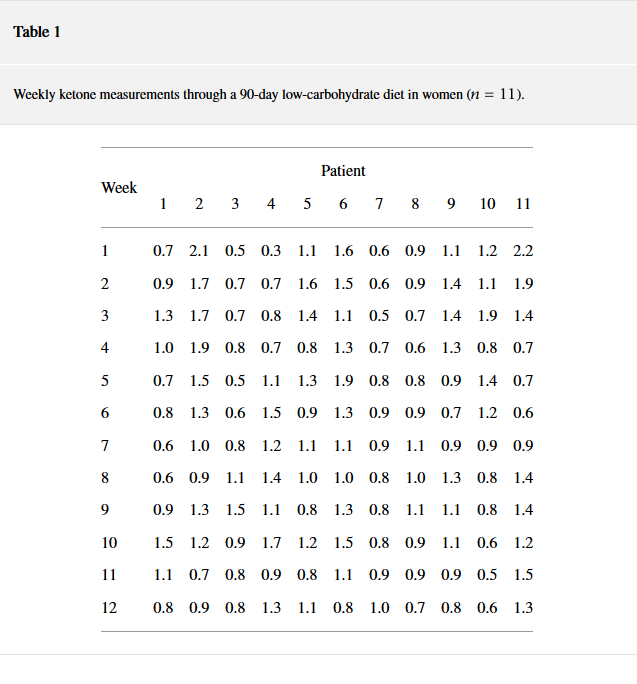
2.3. Mitä mitattiin?
Keskeisiä muuttujia olivat paino, verenpaine ja verilaboratoriotestit 12 tunnin paaston jälkeen. Ketonitasot arvioitiin viikoittain, kun taas kaikki muut tulokset arvioitiin tutkimusjakson alussa ja lopussa. Kaikki arvioinnit teki lääkäri ja kaikki verianalyysit suoritettiin samassa laboratoriossa.
3. Tulokset
3.1. Paino ja painoindeksi
Koehenkilöt olivat keskimäärin 38,3 +/- 2,6 -vuotiaita valkoihoisia naisia. Naiset painoivat keskimäärin 85,7 +/-3,2 kg. Naisten painoindeksi oli 90 päivän intervention alussa 36,3 +/- 1,4 kg/m2. Kaikki koehenkilöt laihtuivat 90 päivän ruokavaliointervention aikana huomattavasti: koehenkilöiden keskipaino oli kokeen loputtua 76,7 +/- 3,2 kg. Vastaavasti keskimääräinen painoindeksi oli kokeen jälkeen 32,7 +/-1,5 kg/m2. Kuvat 1 a ja b

3.2. Systolinen ja diastolinen verenpaine
Koehenkilöiden verenpaine laksi ruokavalion aikana. Intervention alussa koehenkilöiden keskimääräinen systolinen verenpaine oli 134,0 +/-1,6 ja diastolinen verenpaine 89,9 +/- 1,3 mmHg.päivän ketogeenisen ruokavaliointervention päätyttyä koehenkilöiden verenpaine oli laskenut 123,3 +/- 1,1 (p< 0,0001), 82,6 +/-1,0 mmHg (p <0,005. Kuva 2 a ja b

Glykoitunut hemoglobiini
Glykoituneen hemoglobiinin (HbA1c) tasot ovat merkityksellisiä indikaattoreita pitkäaikaisesta korkeasta verensokerista ja osoittavat siten diabeteksen vakavuutta. Koska glukoosipitoisuudet ovat jatkuvasti koholla, glukoosi voi sitoutua epäentsymaattisesti punasolujen hemoglobiiniin.
Perinteisesti diabeettinen alue HbA1c:lle on 6,5%, ja diabeettiset strategiat keskittyvät ensisijaisesti saamaan HbA1c:n lähelle tai alle kyseisen raja-arvon. Kaikilla koehenkilöillä diagnosoitiin diabetes, ja keskimääräinen HbA1c oli 8,9 +/-0,4 %. 90 päivän kuluessa LCHF-interventiosta HbA1c laski tasolle 5,6 +/-0,3 % (p < 0,0001). Kuva 3

3.4. Veren rasva-arvot (lipidit)
Verikokeilla mitataan yleensä prototyyppiset veren lipidit, joihin kuuluvat LDL-kolesteroli, HDL-kolesteroli ja triglyseridit.
Jokaisen näistä on perinteisesti uskottu muuttavan sydänsairauksien riskiä. Siltä osin kuin sydänsairaudet ovat yleisiä tyypin 2 diabeteksessa [12], glykeemisen statuksen ja veren lipidien yhteys on ymmärrettävä.
Samoin kuin HbA1c: kohdalla, ruokavalion vaikutus veren lipideihin oli huomattava. Vaikka LDL-kolesterolin lasku (kuva 4 a) ei ollut merkittävä, triglyseridit (TG: kuva 4 b) laskivat merkittävästi (p < 0,005), kun taas HDL-kolesterolin pitoisuus veressä lisääntyi (kuva 4 c). Triglyseridi : HDL-suhde laski merkittävästi tasolta 4,6 +/-0,8 tasolle 1,6 +/- 0,2 (kuva 4 d); (p<0,005). Erityisen huomionarvoista on, että Triglyseridi : HDL-suhteen ja sydänsairauksien välinen korrelaatio on vahvempi kuin LDL:n ja sydänsairauksien välinen korrelaatio Se on siis varsin hyvä indikaattori sydän- ja verisuonitautien riskistä [13].

3.5. Maksa-arvot
Insuliiniresistenssi ja tyypin 2 diabetes liittyvät moniin maksasairauksiin. ASAT- ja ALAT-pitoisuudet plasmassa mittaavat maksan terveyttä. Nämä mitattiin kahdeksalta potilaalta (kuva 5 a ja b). 90 päivän ketogeeninen ruokavaliointerventio ei vaikuttanut merkittävästi maksa-arvoihin.
4. Ajatuksia
Tämän tutkimuskatsauksen motiivina on esittää kestoltaan rajoitetun (90 päivää) ketogeenisen ruokavalion vaikutusta glykeemisiin HbA1c-arvoihin interventioryhmässä, jonka koehenkilöillä oli hiljattain diagnosoitu tyypin 2 diabetes.
Tutkimuksessa havaittiin, että vähän hiilihydraatteja sisältävä ketogeeninen ruokavalio, jossa hiilihydraattien osuus oli noin 5% päivittäisestä energiansaannista, johti merkittävään HbA1c-arvon putoamiseen diabeettiselta tasolta (8,9%) standardiin (5,6%) vain 90 päivässä.
Lisäksi interventio johti merkittäviin parannuksiin kaikissa muissa kardiometabolisissa markkereissa, mukaan lukien paino, BMI, verenpaine ja triglyseridi (TG): HDL-suhde.
Tässä tutkimuksessa on merkityksellisiä rajoituksia, jotka on huomioitava. Ensinnäkin raportin otoskoko on todella pieni (11). Toiseksi interventioon valikoitui diabeetikkoja, jotka olivat motivoituneita noudattamaan vähähiilihydraattista ruokavaliota. .
Toisaalta pidempien ja paljon suurempien tutkimusten tulokset osoittavat, että hiilihydraattirajoitus tuottaa samanlaisia, vaikkakin vähemmän dramaattisia tuloksia. Äskettäin Hallberg et al. [14] havaitsi suhteellisen merkittävän laskun HbA1c:ssä, TG: ssä ja muissa lipideissä satunnaistamattomassa tutkimuspopulaatiossa yhden vuoden aikana.
Samanlaisia havaintoja havaitsivat Westman et al. [15] vain 24 viikon keston aikana tutkimuksessa, jossa hyödynnettiin tutkimuksen kohteiden satunnaistamista. Jälleen hiilihydraatilla rajoitetulla ryhmällä oli merkittävästi suurempi HbA1c-arvon lasku (-1,5% vs. 0,5%) verrattuna korkeamman hiilihydraatin ryhmään.
Yhteistä tutkimuksille on interventioryhmän saama tuki ja opetus. Yhtä hyviin tuloksiin ei ole päästy tutkimuksissa, joissa interventioryhmä ei saa asianmukaista koulutusta ja tukea.
Hiilihydraattirajoitusten käyttö diabeteksen hoidossa on kuitenkin jo niin vakiintunut ja hyväksytty, että jopa American Diabetes Association totesi äskettäin julkaistussa diabeteshoitojen päivityksessä (Standards of Medical Care in Diabetes): ”Tutkimukset osoittavat, että vähähiilihydraattiset ruokavaliot voivat johtaa parempaan glykemiaan ja vähentää antihyperglykeemisten lääkkeiden tarvetta tyypin 2 diabetesta sairastavilla henkilöillä”[17].
Pasman insuliinipitoisuuksien puute tässä tutkimuksessa estää vetämästä lopullisia johtopäätöksiä insuliiniresistenssistä. Ryhmämme tulevat tutkimukset korjaavat tämän puutteen paneutumalla perusteellisemmin ketogeenisen intervention vaikutuksiin insuliiniherkkyyteen.
Tämän pilottitutkimuksen koehenkilöillä havaitut lipidimuutokset heijastavat kuitenkin insuliiniherkistävää vaikutusta siltä osin kuin TG: HDL-suhde, jonka uskotaan viittaavan insuliiniresistenssiin [18, 19], laski merkittävästi.
HbA1c:n vaikutus diabeteksesta johtuviin vakaviin lisäsairauksiin, kuten neuropatiaan [20], nefropatiaan [21] ja erityisesti sydän- ja verisuonitauteihin [22], pyritään farmakologisesti estämään alentamalla glukoosia ja HbA1c:tä insuliinia lisäämällä joko insuliinihoidon tai insuliinin eritystä lisäävien lääkkeiden avulla.
Keskittyminen HbA1c:hen ja glykeemiseen säätelyyn sekä intensiiviset pyrkimykset glukoosin HbA1c:n alentamiseen nostamalla keinotekoisesti insuliinia nykyisen tyypin 2 diabetekselle tyypillisen hyperinsulinemian yläpuolelle johtavat kuolleisuuden lisääntymiseen [23].
Tämä on tärkeä näkökohta. Ketogeeninen ruokavalio helppona ja turvallisena kliinisenä interventiona laskee HbA1c:tä pahentamatta hyperinsulinemiaa. Tässä mielessä hiilihydraatteja rajoittava lähestymistapa on intuitiivinen, suositeltava ja tehokas tapa saada tyypin 2 diabetes remissioon.
Viitteet
- M. G. Saklayen, “The global epidemic of the metabolic syndrome,” Current Hypertension Reports, vol. 20, no. 2, p. 12, 2018. View at: Publisher Site | Google Scholar
- A. Menke, S. Casagrande, L. Geiss, and C. C. Cowie, “Prevalence of and trends in diabetes among adults in the United States, 1988-2012,” JAMA, vol. 314, no. 10, pp. 1021–1029, 2015. View at: Publisher Site | Google Scholar
- C. Hu and W. Jia, “Diabetes in China: epidemiology and genetic risk factors and their clinical utility in personalized medication,” Diabetes, vol. 67, no. 1, pp. 3–11, 2018. View at: Publisher Site | Google Scholar
- B. Abuyassin and I. Laher, “Diabetes epidemic sweeping the Arab world,” World Journal of Diabetes, vol. 7, no. 8, pp. 165–174, 2016. View at: Publisher Site | Google Scholar
- C. Wang, F. Li, J. Guo, C. Li, D. Xu, and B. Wang, “Insulin resistance, blood glucose and inflammatory cytokine levels are risk factors for cardiovascular events in diabetic patients complicated with coronary heart disease,” Experimental and Therapeutic Medicine, vol. 15, no. 2, pp. 1515–1519, 2018. View at: Publisher Site | Google Scholar
- S. M. de la Monte and J. R. Wands, “Alzheimer’s disease is type 3 diabetes-evidence reviewed,” Journal of Diabetes Science and Technology, vol. 2, no. 6, pp. 1101–1113, 2008. View at: Publisher Site | Google Scholar
- J. S. Kasper and E. Giovannucci, “A meta-analysis of diabetes mellitus and the risk of prostate cancer,” Cancer Epidemiology, Biomarkers & Prevention, vol. 15, no. 11, pp. 2056–2062, 2006. View at: Publisher Site | Google Scholar
- R. J. Playford, C. Pither, R. Gao, and S. J. Middleton, “Use of the alpha glucosidase inhibitor acarbose in patients with ‘Middleton syndrome’: normal gastric anatomy but with accelerated gastric emptying causing postprandial reactive hypoglycemia and diarrhea,” Canadian Journal of Gastroenterology, vol. 27, no. 7, pp. 403-404, 2013. View at: Publisher Site | Google Scholar
- K. M. Johnsson, A. Ptaszynska, B. Schmitz, J. Sugg, S. J. Parikh, and J. F. List, “Urinary tract infections in patients with diabetes treated with dapagliflozin,” Journal of Diabetes and its Complications, vol. 27, no. 5, pp. 473–478, 2013. View at: Publisher Site | Google Scholar
- W. C. Knowler, E. Barrett-Connor, S. E. Fowler et al., “Reduction in the incidence of type 2 diabetes with lifestyle intervention or metformin,” The New England Journal of Medicine, vol. 346, no. 6, pp. 393–403, 2002. View at: Publisher Site | Google Scholar
- F. Q. Nuttall and M. C. Gannon, “Plasma glucose and insulin response to macronutrients in nondiabetic and NIDDM subjects,” Diabetes Care, vol. 14, no. 9, pp. 824–838, 1991. View at: Publisher Site | Google Scholar
- G. Reaven, “Intensive blood pressure/glucose control in type 2 diabetes: why is it so difficult to decrease coronary heart disease?” Journal of Human Hypertension, vol. 13, pp. S19–S23, 1999. View at: Publisher Site | Google Scholar
- P. L. da Luz, D. Favarato, J. R. Faria-Neto Jr., P. Lemos, and A. C. Chagas, “High ratio of triglycerides to HDL-cholesterol predicts extensive coronary disease,” Clinics, vol. 63, no. 4, pp. 427–432, 2008. View at: Publisher Site | Google Scholar
- S. J. Hallberg, A. L. McKenzie, P. T. Williams et al., “Effectiveness and safety of a novel care model for the management of type 2 diabetes at 1 year: an open-label, non-randomized, controlled study,” Diabetes Therary, vol. 9, no. 2, pp. 583–612, 2018. View at: Publisher Site | Google Scholar
- E. C. Westman, W. S. Yancy Jr., J. C. Mavropoulos, M. Marquart, and J. R. McDuffie, “The effect of a low-carbohydrate, ketogenic diet versus a low-glycemic index diet on glycemic control in type 2 diabetes mellitus,” Nutrition & Metabolism, vol. 5, no. 1, 2008. View at: Publisher Site | Google Scholar
- N. Iqbal, M. L. Vetter, R. H. Moore et al., “Effects of a low-intensity intervention that prescribed a low-carbohydrate vs. a low-fat diet in obese, diabetic participants,” Obesity, vol. 18, no. 9, pp. 1733–1738, 2010. View at: Publisher Site | Google Scholar
- American Diabetes Association, “Standards of medical care in diabetes—2019 abridged for primary care providers,” Clinical Diabetes, vol. 37, no. 1, pp. 11–34, 2019. View at: Publisher Site | Google Scholar
- S. J. Kim-Dorner, P. A. Deuster, S. A. Zeno, A. T. Remaley, and M. Poth, “Should triglycerides and the triglycerides to high-density lipoprotein cholesterol ratio be used as surrogates for insulin resistance?” Metabolism, vol. 59, no. 2, pp. 299–304, 2010. View at: Publisher Site | Google Scholar
- M. R. Salazar, H. A. Carbajal, W. G. Espeche, M. Aizpurua, C. A. Dulbecco, and G. M. Reaven, “Comparison of two surrogate estimates of insulin resistance to predict cardiovascular disease in apparently healthy individuals,” Nutrition, Metabolism, and Cardiovascular Diseases, vol. 27, no. 4, pp. 366–373, 2017. View at: Publisher Site | Google Scholar
- F. Xu, L. H. Zhao, J. B. Su et al., “The relationship between glycemic variability and diabetic peripheral neuropathy in type 2 diabetes with well-controlled HbA1c,” Diabetology and Metabolic Syndrome, vol. 6, no. 1, p. 139, 2014. View at: Publisher Site | Google Scholar
- F. Liu, M. Wu, Y. H. Feng et al., “Influence of HbA1c on short-term blood pressure variability in type 2 diabetic patients with diabetic nephropathy,” Journal of Zhejiang University Science B, vol. 14, no. 11, pp. 1033–1040, 2013. View at: Publisher Site | Google Scholar
- E. Selvin, K. Wattanakit, M. W. Steffes, J. Coresh, and A. R. Sharrett, “HbA1c and peripheral arterial disease in diabetes: the Atherosclerosis Risk in Communities study,” Diabetes Care, vol. 29, no. 4, pp. 877–882, 2006. View at: Publisher Site | Google Scholar
- Action to Control Cardiovascular Risk in Diabetes Study Group, H. C. Gerstein, M. E. Miller et al., “Effects of intensive glucose lowering in type 2 diabetes,” The New England Journal of Medicine, vol. 358, no. 24, pp. 2545–2559, 2008. View at: Publisher Site | Google Scholar
- R. Ness-Abramof and C. M. Apovian, “Drug-induced weight gain,” Timely Topics in Medicine. Cardiovascular Diseases, vol. 9, article E31, 2005. View at: Google Scholar
- C. L. Roumie, X. Liu, N. N. Choma et al., “Initiation of sulfonylureas versus metformin is associated with higher blood pressure at one year,” Pharmacoepidemiology and Drug Safety, vol. 21, no. 5, pp. 515–523, 2012. View at: Publisher Site | Google Scholar
Copyright |
| Copyright © 2019 Chase M. Walton et al. This is an open access article distributed under the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original work is properly cited. Chase M. Walton, Katelyn Perry, Richard H. Hart, Steven L. Berry, and Benjamin T. Bikman Metabolism Research Lab, Department of Physiology and Developmental Biology, Brigham Young University, Provo UT, USA, Insulin IQ, Orem UT, USA, Revere Health, Orem UT, USA https://www.hindawi.com/journals/jdr/2019/8681959/ |

