Mikä on paras ruokavalio sydänterveydelle?
Silvia Migliaccio, Caterina Brasacchio, Francesca Pivari, Ciro Salzano, Luigi Barrea, Giovanna Muscogiuri, Silvia Savastano, Annamaria Colao
Kääntänyt, editoinut ja kriittisesti kommentoinut: Sami Raja-Halli
Tiivistelmä
Sydän- ja verisuonitaudit (CVD) ovat yleisin kuolinsyy kehittyneissä maissa. Tutkimuksissa sydän- ja verisuonitaudit assosioituvat usein ravitsemustottumuksiin ja elintapoihin, kuten runsaaseen alkoholinkäyttöön, stressiin ja tupakointiin sekä liian vähäiseen liikuntaan.
Liikunta- ja ruokailutottumuksia korjaamalla sydän- ja verisuonitautien riskiä voi laskea. Ravinto vaikuttaa sydän- ja verisuonitautien riskitekijöihin, kuten veren rasva- ja sokeriprofiileihin, verenpaineeseen ja lihavuuteen. Terveyden optimoimiseksi on kehitelty erilaisia ruokavalioita.
Miten DASH, kasvisruokavalio, ketogeeninen ruokavalio ja japanilainen ruokavalio vaikuttavat sydän- ja verisuonitautien riskiin? Entä millaisia vaikutuksia eri ravintoaineilla on sydämen terveyteen?
Useimmat terveelliset ruokavaliot korostavat samojen ravintoaineiden hyötyjä. Elimistö tarvitsee runsaasti hedelmiä ja vihanneksia, täysjyväviljoja, hyviä rasvoja ja palkokasveja. Tämä on usein kuultu mantra; lisättyä sokeria, punaista ja prosessoitua lihaa sekä runsaasti kovaa rasvaa ja sokereita sisältäviä prosessoituja valmisruokia tulisi välttää.
Yksittäisten ravintoaineiden vaikutukset terveydelle eivät ole yksiselitteisiä. Sen lisäksi, että ravintoaineet vaikuttavat yhdessä ja toisiinsa, ne vaikuttavat hormonitoiminnan välityksellä aineenvaihduntaan, solujen signalointiin, geeniekspressioon, hormonien yms. tuotantoon, elimistön uusiutumiseen ja suolistomikrobiomin välityksellä immuunijärjestelmän toimintaan. Ihminen tarvitsee välttämättä esimerkiksi steroidihormoneja, joiden esiaste on kolesteroli.
Tasapainoisella välttämättömät ravintoaineet sisältävällä ruokavaliolla on kokonaisvaltaisempia ja terveellisempiä vaikutuksia kuin yksittäisillä superfoodeilla. Elimistö on tarkka laadusta, mutta laatua ei määrittele ruoan hinta, vaan elimistön tarvitsemien ravinteiden laatu.
Monien ravintoaineiden yksipuolinen ja liiallinen saanti altistavat aineenvaihdunnan häiriöille. Minkälaisia ravitsemusprotokollia hyödyntäen lihomista, matala-asteista tulehdusta, diabetesta ja sydän- ja verisuonitauteja voidaan ehkäistä?
Tutkimusstrategia
Löysin kiinnostavan ja pätevältä vaikuttavan tutkimuskatsauksen erilaisten ruokavalioiden yhteydestä sydän- ja verisuonitauteihin. Kiinnitin pian huomiota katsauksessa käytettyjen lähteiden heikkoon laatuun. Tiesin, että on olemassa tieteellisesti laadukkaampia, tuoreempia ja arvostetumpia tutkimuksia kuin tässä katsauksessa lähteinä toimivat vanhat ja konservatiiviset tutkimukset.
Päädyin laajentamaan tätä katsausta täsmennyksillä, kriittisillä huomioilla ja viittauksilla tuoreempiin tutkimuksiin. Tämä teki artikkelista hyvin pitkän, mutta myös kattavan.
Kukin tämän tutkimuskatsauksen kirjoittajista haki PubMedistä (MEDLINE)tutkimusraportteja elokuuhun 2019 asti käyttäen erikseen seuraavia hakutermejä: sydän- ja verisuonitaudit, lihavuus, ruokavalio, ravitsemus, glukoosimetabolia, välimeren ruokavalio ( MeDi), ketogeeninen ruokavalio (KD), japanilainen ruokavalio, kasvisruokavalio (VegDiet) ja verenpainetautia ehkäisevä ruokavalio (DASH).
Asiaan liittyvien artikkeleiden ja arvostelujen viiteluetteloita haettiin myös manuaalisesti. Yhteensä haulla tunnistettiin kahdeksansataa tutkimuspaperia, joista 136 valittiin ja sisällytettiin tähän tutkimuskatsaukseen. Minuun määrä teki vaikutuksen.
Johdanto
Sydän- ja verisuonitaudit ovat monitekijäisiä sairauksia, jotka aiheutuvat useista päällekäisistä häiriöistä, kuten liiallisesta viskeraalisesta rasvasta (keskivartalolihavuudesta), kohonneesta verenpaineesta, dyslipidemiasta ja glukoosi-intoleranssista [1]. Nämä lisäävät sydän- ja verisuonitapahtumien, kuten aivohalvauksen ja sydänkohtausten riskiä.
Insuliiniresistenssi ja diabetes luokitellaan itsenäisiksi sydän- ja verisuonitautien riskitekijöiksi. Alkavat sydän- ja verisuonitaudit voivat piileskellä ja kehittyä rauhassa harmittomilta tuntuvien aineenvaihdunnan häiriöiden taustalla. Korkea verensokeri- ja insuliinipitoisuus (hyperinsulinemia) vahingoittavat verisuonia.
Sokerin aiheuttamat verisuonivauriot alkavat pienistä verisuonista, mutta kehon jatkuva tulehdustila ja verisuonivauriot lisäävät kolesterolin ateroskleroottista kumuloitumista myös valtioiden seinämiin. Erityisen haitallista sydän- ja verisuoniterveydelle ovat jatkuva inflammaatio ja glykaation kehittyneet lopputuotteet (AGE:t).
Elintärkeä LDL-kolesteroli muuttuu vahingolliseksi, kun se hapettuu. Oksidoituneet LDL-partikkelit ovat ateroskleroottisia. Sydän- ja verisuonitaudit seuraavat matala-asteista tulehdusta, hyperglykemiaa, dyslipidemiaa ja glykaatiota [2].
Jatkuvasti korkean glykaatiota ja verisuonivaurioita aiheuttavan verensokerin laskemiseksi on yksi ylivoimainen keino: ravinnon sisältämien sokereiden rajoittaminen. Sillä on monia terveydellisiä vaikutuksia matala-asteisen tulehdustilan hillitsemisestä laihtumiseen ja energiametabolian korjaantumiseen.
Glykaation kehittyneet lopputuotteet: glykotoksiinit
Korkean verensokerin aiheuttamista terveysriskeistä glykaatio tunnetaan valitettavan huonosti. Glykaatiota aiheuttaa jatkuvasti korkea verensokeri, joka reagoi muun muassa vapaisiin aminohappoihin, proteiineihin ja rasvahappoihin. Tutuin esimerkki glykaagiosta on aikuistyypin diabetes ja siihen liittyvä pitkäsokerin mittaus, jossa mitataan hemoglobiinin glykaatiota (hemoglobiini (HbA1C).
Glykaatiossa punasolujen hemoglobiinimolekyyleihin kiinnittyy (glykatoituu) glukoosia. Glukoosin kiinnittymisvauhti riippuu veren glukoosin määrästä. Mitä enemmän veressä on sokeria, sitä enemmän sitä tarttuu happea kuljettavien punasolujen hemoglobiiniin. Veren punasolujen glykatoituminen tekee verestä kuvaannollisesti siirappimaista.
Kehittynyt glykaation lopputuote (eng. advanced glycation end-product, AGE) on yleisnimitys suurelle joukolle erilaisia proteiineja tai rasvoja, jotka jotka ovat glykatoituneet ei-entsymaattisesti altistuttuaan joillekin sokereille.
Glykotoksiinit osallistuvat moniin soluja rappeuttaviin sairauksiin, kuten Alzheimerin ja Parkinsonin tauteihin. Niiden tiedetään lisäävän diabeteksen, ateroskleroosin, kroonisen munuaisten vajaatoiminnan, harmaakaihin, lihasheikkouden ja eräiden syöpien riskiä.
Glykotoksiinit vaikuttavat useinpiin kehon solutyypppeihin ja molekyyleihin. Haitallisia AGE:ista tekee niiden kyky reagoida verkkoutumisreaktioiden kautta muun muassa kehon rakenneproteiinien kuten kollageenin ja elastiinin kanssa. Näin glykaation lopputuotteet polymerisoivat proteiineja yhteen suuriksi ryppäiksi estäen niiden normaalia toimintaa. Glykotoksiinit altistavat valtimonkovettumataudille, koska ne ryppäyttävät verisuonten pintojen kollageeniä, minkä seurauksena suonet kovettuvat.
Verisuonien kovettuminen lisää kolesterolin kertymistä suonten sisäpintaan. Glykotoksiinit edistävät LDL:n hapettumista. Hapettunut LDL-kolesteroli on eräs valtimokovettumataudin tärkeimmistä riskitekijöistä.
Glykaation synnyttämät glykotoksiinit lisäävät kehon matala-asteista tulehdusta aktivoimalla syöjäsoluja (makrofageja) RAGE/NF-κB-signalointireitin kautta. AGE:t voivat sitoutua monista soluista löytyviin AGE-reseptoreihin (RAGE), joiden välityksellä ne lisäävät oksidatiivista stressiä ja aiheuttavat makrofagivälitteisiä tulehdusreaktioita. Tämä johtaa tuman transkriptiotekijä kappa B:n (NFκB) aktivoitumiseen, joka puolestaan ohjaa monia tulehdusreaktioihin liittyviä geenejä.
Tulehdusreaktiot liittyvät moniin elämäntapasairauksiin. Esimerkiksi valtimonkovettumatauti alkaa makrofageja houkuttevilla tulehdusreaktioilla. Osa makrofageista muuntuu tulehduskohtaan jääviksi vaahtosoluiksi syödessään hapettunutta LDL-kolesterolia. Nämä toimivat alustana suonen pintaan kerääntyvälle plakille. Plakin kasvaessa verisuoneen voi lopulta muodostua veritulppa.
Korkean verensokerin tuottamat glykotoksiinit vaikuttavat ihon vanhenemiseen kollageenin ja elastiinin välityksellä, mikä lisää ryppyjä ja heikentää ihon joustavuutta. Ihon nuorekkuuden säilyttämiseksi on halpa menetelmä, joka ei edellytä hintavia ihonhoitotuotteita: rajoita sokereita!
Glykotoksiinien ihoa vanhentavat ja rappeuttavat vaikutukset heikentävät haavojen parantumista ja ihon kykyä syntetisoida D-vitamiinia. Nämä ilmiöt liittyvät todennäköisesti useiden soluja rappeuttavien vaikutusten yhteisvaikutukseen, jossa glykaation kehittyneet lopputuotteet osaltaan heikentävät muun muassa solujen DNA:n korjausprosesseja ja DNA-synteesiä, mitokondrioiden energiametaboliaa, solukalvojen lipidien biosynteesiä, hormonien tuotantoa jne.
Sydän- ja verisuonitaudit ovat yleisin kuolinsyy erityisesti teollistuneissa länsimaissa [3]. Suomessa ja Ruotsissa on kuitenkin havaittu, että jatkuvasti lisääntyvä statiinien käyttö sydäntautien ehkäisemiseksi ei ole tilastollisesti laskenut sydänkuolleisuutta. Onko sota kolesterolia vastaan jo hävitty, vai onko vuosikymmeniä haukuttu väärää puuta?
Sydän- ja verisuonitautien ongelma on mutkikkaampi kuin yleisesti tunnustetaan. Sydän- ja verisuonitaudit eivät johdu tyydyttyneistä rasvoista ja kolesterolista. Eivät ainakaan yksin niistä. Jatkuvasti korkea verensokeri ja veren kohonneet triglyseridipitoisuudet altistavat varmasti sydän- ja verisuonitaudeille. Kuitenkin vain tyydyttynyt rasva on nostettu tikunnokkaan. Miksi?
Se on harmillista, koska runsaasti hiilihydraatteja sisältävä ravinto ylläpitää veren korkeita triglyseriditasoja lisäämällä maksan de novo lipogeneesiä. Runsaasti rasvaa sisältävä ruokavalio itse asiassa laskee veren triglyseridejä, nostaa HDL-kolesterolia, mutta ei juuri vaikuta LDL-kolesterolin pitoisuuteen. Hiilihydraattien rajoittaminen korjaa verensokeria, verenpainetta, veren lipidiprofiileja ja solujen energiametaboliaa.
Vaikka musta puhutaan valkoiseksi, aineenvaihdunnan tasolla on aivan samantekevää onko sokeri peräisin perunasta, täysjyväleivästä vai pullasta. ruoansulatuskanava hajottaa hiilihydraatittien sisältämän tärkkelyksen yksittäisiksi sokerimolekyyleiksi, jotka imeytyvät elimistöön. Verenkierrossa leivästä, pullasta, perunasta, marmeladista ja suklaasta peräisin olevat sokerimolekyylit vaikuttavat aineenvaihduntaan samalla tavoin. Toki täysjyväleivässä on enemmän ravinteita kuin pullassa ja sen sisältämät kuidut hidastavat sokereiden imeytymistä, mutta täysjyväleivässäkin on melkoisesti sokeria.
Jatkuvasti korkea verensokeri, insuliiniresistenssi, runsas eläinproteiinien ja eläinrasvojen saanti kasvattavat sydäntautien riskiä. Sairaudet ovat monitekijäisiä.
Glykaation vaikutuksista sydän- ja verisuonitauteihin ollaan korvia huumaavan hiljaa, vaikka puoli miljoonaa suomalaista sairastaa diabetesta ja diabeetikkojen sydäntautikuoleman riski ei-diabeetikkoihin verrattuna on tilastollisesti 2-4 kertaa korkeampi.
Kolesteroli on elimistön välttämättä tarvitsema biologinen komponentti. Lähes kaikki solut voivat valmistaa kolesterolia monimutkaisessa 37-osaisessa reaktioketjussa. Eniten kolesterolia valmistaa maksa. Kolesterolia on kaikkien kehon solujen solukalvoissa. Se osallistuu solujen signalointiin ja sitä tarvitaan aivojen viejähaarakkeita suojaaviin myeliinikalvoihin. Kolesteroli on myös steroidihormonien, kuten testosteronin ja estrogeenin, sekä immuunijärjestelmää ja kalsiumin homeostaasia säätävän D-vitamiinin esiaste.
Kuolleisuus lisääntyy laakean U-käyrän mukaisesti matalilla ja hyvin korkeilla kolesterolitasoilla. Matalien kolesterolitasojen riskeistä ei useinkaan puhuta, vaikka dementia ja kuolleisuus lisääntyvät asteittain, mitä matalammille kolesterolitasoille mennään.
Hapettunut LDL-kolesteroli on tunnettu ateroskleroosin riskitekijä. Sydänterveyden kannalta suurin ongelma ei ole kolesteroli itsessään, vaan korkean verensokerin aiheuttama oksidatiivinen stressi, glykaation kehittyneet lopputuotteet ja LDL-kolesterolin oksidaatio. LDL-kolesterolin hapettumista ja oksidatiivista stressiä voi hillitä verensokeria laskemalla.
Kuluneiden kolmen vuosikymmenen aikana lisääntyneestä sydän- ja verisuonitautien ilmaantuvuudesta on tullut polttava sosioekonominen prioriteetti. Tarve ehkäistä sydän- ja verisuonitauteja elämäntapamuutoksilla on tänään yhtä ajankohtainen kuin vuonna 1977, jolloin USDA määritteli tyydyttyneet rasvat ja kolesterolin kansakunnan vihollisiksi no:1 [4].
Sydän- ja verisuonitautien kehitys assosioituu epäterveellisiin elämäntapoihin [5, 6]:
- ravinto sisältää liikaa natriumia (suolaa)
- syödään liikaa prosessoituja elintarvikkeita
- syödään liikaa/lisättyä sokeria
- ravinto sisältää epäterveellisiä rasvoja ja erityisesti teollisia transrasvoja
- ravinnon vähäinen hedelmien ja vihannesten osuus
- vähäinen täysjyvätuotteiden ja kuidun osuus
- vähäinen palkokasvien osuus
- vähäinen kalan osuus
- vähäinen pähkinöiden ja siementen osuus
- runsas alkoholin käyttö
- stressi
- tupakointi
- vähäinen liikunta
Useimmat ravitsemustutkimukset tukevat edellisiä havaintoja. Rasvojen ja esimerkiksi punaisen lihan terveysvaikutuksista on kuitenkin olemassa ristiriitaista näyttöä. Viimeisimmät meta-analyysit ovat joiltain osin puhdistaneet tyydyttyneiden rasvojen mainetta. Todennäköisesti tyydyttyneet rasvat eivät yksin kasvata sydän- ja verisuonitautien riskiä.
Hiljattain runsaasti mediahuomiota saanut punaisen lihan ja paksusuolensyövän yhteyttä korostava tutkimus oli uutisankka; tai tarkemmin se oli tilastollinen silmänkääntötemppu, jossa sovellettiin taikasanoja suhteellisen riskin alenema. Tosiasiassa punainen liha lisäsi suolistosyövän riskiä 0,63 % ja ei-lihaa sisältävä ruokavalio 0,40 %. Todellinen riski jäi alle prosenttiin ja tutkimuksen virhemarginaaliin.
Terveysvaikutuksiltaan tyydyttyneet (kovat) rasvat ovat monien tutkimusten mukaan neutraaleja. Tämä on naturalistinen lähestymistapa: kädellisten evoluutio on jatkunut miljoonia vuosia. Nykyihmisten ravintoon on kuulunut tyydyttyneitä rasvoja 200 000 vuoden kehityshistorian ajan. Monityydyttymättömät teolliset siemenöljyt keksittiin hieman yli sata vuotta sitten. Tekeekö tehdas parempaa ravintoa kuin äiti? En tarkoita Saarioisten äitejä, vaan rintamaitoa, joka sisältää runsaasti kolesterolia ja tyydyttyneitä rasvoja. Naturalistina minä luotan luonnollisiin rasvoihin ja äidin maitoon enemmän kuin teollisiin rasvoihin.
Tutkimusnäyttö tukee hypoteesia, jonka mukaan elämäntapamuutokset, kuten liikunnan lisääminen ja ruokavalion muuttaminen voivat ehkäistä sydän- ja verisuonitauteja. Se, mitä tämä käytännössä tarkoittaa on monen tekijän summa. Ravinnon terveysvaikutuksista kinastellaan ja siitä Ruokasodassa on kyse.
Iäkkäiden ihmisten määrä kasvaa teollistuneissa maissa nopeasti. Trendi lisää terveydenhoitoon kohdistuvia taloudellisia ja sosiaalisia paineita. Tämän vuoksi on perusteltua selvittää aineenvaihdunnan patofysiologiset mekanismit sellaisten toimenpiteiden kehittämiseksi, jotka vähentävät elintapoihin liittyvien kardiometabolisten tautien sairastumisalttiutta, ja jotka voidaan helposti toteuttaa väestötason suosituksilla.
Yhteiskunnallisena prioriteettina tulee olla ikääntyvien ihmisten terveiden elinvuosien lisääminen ja sydäntauteihin liittyvien sosioekonomisten kustannusten vähentäminen. Tämä tavoite keventää yhteiskunnalle sydäntaudeista koituvaa sosioekonomistista painolastia ja lisää ikääntyvien ihmisten elämänlaatua. Samalla meidän on taisteltava diabetes- ja lihavuusepidemioita vastaan. Diabetes ei ole ikääntymiseen, vaan elintapoihin liittyvä sairaus.

Energian ylimäärä
On tunnettua, että lihottavat ruokavaliot lisäävät sydän- ja verisuonitautien riskiä. Energiansaannin vähentäminen 20–50%:lla hillitsee tutkimusten mukaan sairastuvuutta aineenvaihduntasairauksiin, kuten lihavuuteen ja tyypin 2 diabetekseen. Tämä pätee ainakin kokeellisissa eläinmalleissa [7].
Julkaistut kliiniset tutkimukset vahvistavat, että energiansaannin rajoittaminen laskee sydän- ja verisuonitautien riskiä. Kiinnostavaa on, että pieni koetutkimus, johon osallistui 24 koehenkilöä, osoitti, että vain 10 viikon energianrajoitus (80% normaalista energiansaannista) laski merkittävästi sekä systolista että diastolista verenpainetta [8].Korkean verenpaineen tiedetään altistavan sydän- ja verisuontitaudeille.
Lisäksi havaittiin merkittävä verensokerin lasku vastaavan 10 viikon energianrajoitusta koskevan ruokavaliointervention jälkeen [9]. Verensokerin lasku tarkoittaa sokerimetabolian parantumista. Korkea verensokeri on eräs tunnettu kardiometabolisten häiriöiden riskitekijä.
Useat tutkimukset osoittavat, että pidempiaikainen energiaa rajoittava ravintomalli laskee sydän- ja verisuonitautien riskiä parantamalla seerumin lipidiprofiilia, paasto-glykemiaa ja verenpainetasoja [10–12]. Ravinnon sisältämän energian rajoittamisen hyödyistä voit lukea täältä.
Hiljattain Comprehensive Assessment of the Long-term Effect of Reducing Intake of Energy -tutkimusohjelmassa arvioitiin pitkäkestoisen energianrajoituksen vaikutusta sydän- ja verisuoniterveyteen. Tähän satunnaistettuun tutkimukseen osallistui 218 koehenkilöä. Koehenkilöt jaettiin kahteen ryhmään, joista toinen noudatti rajoitetun energiansaannin ruokavaliota -25 % energiansaannilla 2 vuoden ajan ja toinen ryhmä noudatti tavanomaista ruokavaliota ilman energiarajoituksia 2 vuoden ajan.
Havainnot osoittivat, että jo kuuden kuukauden vähäenergisen ruokavalion aikana paino laski merkittävästi ja lipidiprofiilit sekä verenpainetasot paranivat [13]. Molemmat tekijät liittyvät kasvaneeseen kardiovaskulaariseen riskiin.
Tyydyttyneet rasvat (SFA) ja sydäntaudit
Runsas tyydyttyneen rasvan saanti yhdistetään usein kasvaneeseen sydän ja verisuonitautien riskiin erityisesti siksi, että se lisää matalatiheyksisen kolesterolin (LDL) pitoisuutta seerumissa. Tyydyttyneitä rasvoja sisältävät ravinto kasvattaa ateroskleroosin riskiä [14] ja insuliiniresistenssiä lisäämällä aterogeenisten lipoproteiinien LDL ja erittäin matalatiheyksisten lipoproteiinien ( VLDL) määrää ja vähentämällä suurtiheyksisten lipoproteiineja (HDL) [15].
Ancel Keysin seitsemän maan tutkimus oli yksi ensimmäisistä tutkimuksista, joissa arvioitiin tyydyttyneiden rasvojen saantiin liittyvää CVD-riskiä. Tutkimuksessa arvioitiin sydän- ja verisuonikuolleisuutta 11 579 miehellä, joita seurattiin 15 vuoden ajan. Tulokset osoittivat positiivisen korrelaation sydän- ja verisuonikuolemien ja tyydyttyneiden rasvojen saannin välillä [21].
Näin tapahtui kuitenkin vain, koska Ancel Keys hylkäsi 22 maan tutkimusaineistosta 15 maata, joissa positiivinen korrelaatio tyydyttyneiden rasvojen ja sydänkuolleisuuden välillä ei toteutunut. Seitsemän maan tutkimus on eräs räikeimmistä esimerkeistä tieteellisestä kirsikanpoiminnasta. Valitettavasti se on ravitsemussuositusten kiveen hakattu paradigma. Ranskalainen paradoksi näkyy selvästi Ancel Keysin alkuperäisessä datassa.
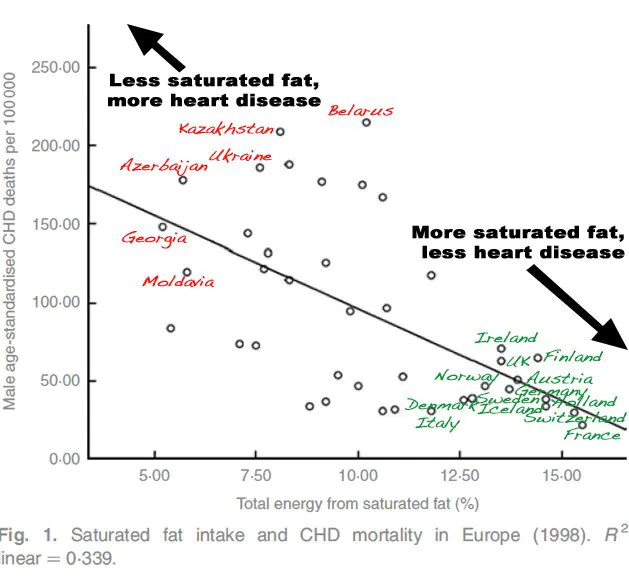
Kovat rasvat vs. pehmeät rasvat Euroopassa
Seuraavina vuosina tutkittiin Japanissa ja länsimaissa asuvia japanilaisia miehiä. Tutkimuksissa havaittiin japanilaismiesten sydän- ja verisuonikuolleisuuden lisääntyneen länsimaissa, minkä arveltiin johtuvan runsaasti tyydyttynyttä rasvaa sisältävän ruokavaliosta. Korrelaatio on olemassa, mutta kausaalisuuden osoittamisesta ei ole jälkeäkään. [14, 22].
Muistutan, että Mainen osavaltiossa margariinin kulutus liittyy avioerojen lisääntymiseen. Se on fakta, mutta ei siltä pohjalta voi voita suositella avioerojen ehkäisemiseen. Vai voiko?
Tyydyttyneiden rasvojen ja sydäntautien välisestä syy-yhteydestä ei vallitse tieteellistä yksimielisyyttä. Totesin jo tekstin alussa, että yksittäisten ravintoaineiden terveysvaikutusten osoittaminen ei ole aivan yksiselitteistä.
Tyydyttyneiden rasvojen vaaroja tukeva L. Robertsonin ja kumppaneiden tutkimus, johon tässä tutkimuskatsauksessa viitataan (14), on vuodelta 1977. Se on epidemiologinen väestötutkimus japanilaisten miesten sydänkuolleisuudesta Japanissa, Hawajilla ja Kaliforniassa.
Tutkimus osoitti, että Kaliforniassa ja Hawajilla elävät japanilaismiehet kuolivat useammin sydäntauteihin kuin samanikäiset Japanissa elävät miehet. Tämän uskottiin johtuvan runsaammasta tyydyttyneiden rasvojen saannista. Kriittisesti arvioiden: japanilaiset söivät ja syövät yhä edelleen terveellisemmin ja liikkuvat enemmän kuin amerikkalaiset. Määrällisesti amerikkalaiset kuluttavat keskimäärin lähes 1000 kilokaloria enemmän energiaa päivässä kuin japanilaiset. Yhdysvalloissa elävien japanilaismiesten elämäntapojen amerikkalaistuminen lisäsi siis tyydyttyneiden rasvojen lisäksi raffinoitujen sokereiden ja transrasvojen saantia sekä kokonaisenergian määrää, mutta vähensi kasvisten saantia ja arkiliikuntaa. Viitattu tutkimus ei todista, että Yhydsvaltoihin muuttaneet japanilaismiehet kuolivat sydäntauteihin tyydyttyneiden rasvojen vuoksi – se vain väittää niin.
Epidemiologisten tutkimusten todistusarvo on parhaimmillankin ”suuntaa antava”. Tiedetään, että vuonna 1977 USDA julkaisi tyydyttyneiden rasvojen ja kolesterolin rajoittamiseen tähtäävät ravintosuositukset, jotka perustuivat Ancel Keysin 7 maan tutkimukseen. Tässä tieteellisessä ilmapiirissä julkaistut epidemiologiset tutkimukset noudattivat tuloksiltaan yleisesti hyväksyttyä linjaa ja kallistuivat varmasti muista muuttujista riippumatta yleisesti hyväksytyn linjan kannalle. Korrelaatio on helppo osoittaa, mutta se ei osoita syy-yhteyttä.
Euroopassa eniten tyydyttyneitä rasvoja kuluttavien ranskalaisten ja sveitsiläisten sydänkuolleisuus on Euroopan alhaisinta. Vastaavasti eniten monityydyttämättömiä rasvoja syövien itäeurooppalaisten sydänkuolleisuus on Euroopan korkeinta. Tämä ilmiö tunnetaan ranskalaisena paradoksina. Se ei sovi vallitseviin ravitsemusoppeihin tyydyttyneiden rasvojen ja kolesterolin sydäntauteja lisäävästä vaikutuksesta. Tällaisista ekologisista faktoista ei kuitenkaan voi ja pitäisi vetää kovin pitkälle meneviä johtopäätöksiä, koska muuttujia on niin paljon.
P. M. Cliftonin systemaattinen kirjallisuuskatsaus (2017) kallistuu tyydyttyneiden rasvojen haittojen puolelle
P. M. Cliftonin systemaattinen kirjallisuuskatsaus analysoi tärkeimmät sydäntautien ja rasvojen suhdetta selvittävät tutkimukset. Katsaus on niin pitkä, että sivuan sitä vain lyhyesti. Se antaa hyvän kuvan siitä, kuinka vaikea yksittäisen ravintoaineen terveysvaikutuksia on selvittää.
Siri-Tarino et al. 2010
toteutti meta-analyysin tyydyttyneiden rasvojen saannin assosiaatiosta sydäntauteihin ja sydäntautikuolleisuuteen 16 kohorttitutkimuksesta. Viimeisin näistä oli vuodelta 2007. Dataa päivitettiin kuudesta kohortista.
Siri-Tarinon meta-analyysissä käytettiin mukautettua mallia, joka sisälsi kuuden kohortin mukauttamisen muihin rasvoihin ja rasvojen korvaamisen hiilihydraatteilla. Kuusi Siri-Tarinon analysoimaa kohorttitutkimusta osoitti tyydyttyneiden rasvojen ja sydäntautien välillä positiivisen yhteyden. Kymmenen analysoitua tutkimusta ei löytänyt yhteyttä sydäntautien ja tyydyttyneiden rasvojen väliltä. Siri-Tarinon johtopäätös oli, että tutkimukset antavat ristiriitaisia tuloksia, jotka eivät osoita selvää yhteyttä tyydyttyneiden rasvojen ja sydäntautien välillä ja siten tue yleistä näkemystä tyydyttyneiden rasvojen haitallisuudesta.
R. Chowdhuryn
20 tutkimuksen (283 963 henkilön) meta-analyysi vuodelta 2014 ei löytänyt näyttöä tyydyttyneiden rasvojen yhteydestä sydäntauteihin. Chowdury et al. havaitsi, että tyydyttyneet rasvahapot eivät liity CHD-tapahtumiin ja kuolemiin verrattuna hiilihydraatteihin. Sen sijaan transrasvahappojen saanti lisäsi sydäntauteja. Monityydyttymättömien rasvojen saanti ei myöskään laskenut sydäntautien ja -kuolleisuuden riskiä tilastollisesti merkittävästi.
”The evidence did not clearly support cardiovascular guidelines that encouraged high consumption of polyunsaturated fatty acids and low consumption of total saturated fats.” – Chowdhury
De Souza et al. (2015)
analysoi tyydyttyneiden rasvojen ja transrasvojen saannin vaikutuksia kardiovaskulaarisiin tapahtumiin ja sydänkuolleisuuteen 41 erillisen tutkimuksen meta-analyysissä. Yksitoista analysoitua kohorttia osoitti tyydyttyneen rasvan ja sydäntautikuolleisuuden välille yhteyden.
Johtopäätös: runsas tyydyttyneiden rasvojen saanti ei lisää sydänkuolleisuutta verrattuna hiilihydraatteihin. Runsas tyydyttyneiden rasvojen saanti hiilihydraatteihin verrattuna ei myöskään näytä lisäävän muita sydäntautitapahtumia. Transrasvojen kokonaissaanti liittyi kuitenkin kaikkien syiden kuolleisuuteen.
Zong et al. (2016)
tutki yksittäisten rasvahappojen saannin vaikutuksia sairaanhoitajien terveystutkimuksen (Nurses Health Study) ja terveydenhuollon ammattilaisten seurantatutkimuksen (Health Professionals Follow Up Study) aineiston pohjalta. Verrattaessa tyydyttyneiden rasvojen saannin korkeinta ja matalinta kvintiiliä, sepevaltimotaudin riskisuhde tyydyttyneillä rasvoilla oli korkeampi kuin monityydyttymättömillä rasvoilla tai täysjyvähiilihydraateilla. Monityydyttämättömät rasvat ja täysjyvähiilihydraatit laskivat sepelvaltimotaudin riskiä.
Sekä maitotuotteista että teollisista lähteistä peräisin olevat transrasvat nostavat selvästi LDL-kolesterolia ja alentavat HDL-kolesterolia, mutta niiden vaikutukset sydän- ja verisuonitauteihin ovat kiistanalaisia.
Bendsen et al. 2011
analysoi kuusi julkaistua ja kaksi julkaisematonta prospektiivista kohorttitutkimusta transrasvojen (TFA) kokonaissaannin ja sydäntautiriskien yhteydestä vertaamalla ääri-kvintiilejä.
Eläinperäinen transrasvojen saanti ei kasvattanut merkittävästi sydänsairauksien riskiä. Teollisten transrasvojen saanti viittasi positiiviseen yhteyteen sydäntautien ja teollisten transrasvojen välillä.
Kirjoittajat päättelivät, että teollinen TFA voi olla positiivisesti yhteydessä sydänsairauksiin, kun taas luonnollinen eläinperäinen TFA ei ole. Käytettävissä olevien tutkimusten rajallisen määrän vuoksi ei kuitenkaan voida olla varmoja, onka transrasvojen lähteellä merkitystä.
Praagman et al. 2016
analysoi EPIC-Alankomaat-kohorttia (1807 IHD*-tapahtumaa) ja havaitsi, että tyydyttyneiden rasvojen saanti liittyi pienempään sydän- ja verisuonitautien riskiin. SFA:n (tyydyttyneiden rasvojen) korvaaminen eläinproteiinilla, cis-MUFA:lla (kertatyydyttymättömällä rasvalla), PUFA:lla (monityydyttämättömällä rasvalla) tai CHO:lla (hiilihydraateilla) liittyi tutkimuksessa korkeampaan iskeemisen sydäntaudin riskiin.
Matalammat sydäntautien (IHD) riskit havaittiin maitotuotteista, kuten voista, juustosta, maidosta ja muista meijerituotteista peräisin olevien SFA-yhdisteiden suuremmilla saannoilla.
Rotterdamin tutkimuksessa Praagman et al. 2016 ei löytänyt yhteyttä tyydyttyneiden rasvojen ja sydäntautien välillä. He havaitsivat kuitenkin korkeamman sydäntautiriskin palmitiinihapon saannilla, mutta eivät tyydyttyneiden rasvojen muilla rasvahappoketjujen pituuksilla.
* IHD= Ischemic Heart Disease
EPIC-Alankomaat-tutkimuksessa tyydyttyneiden rasvojen korvaaminen eläinproteiinilla liittyi korkeampaan sydän- ja verisuonitautien riskiin. Rotterdamin tutkimuksessa tyydyttyneiden rasvojen korvaaminen eläinproteiineilla lisäsi sydäntautien riskiä, mutta muiden makroravinteiden suhteen yhteyttä ei havaittu.
Blekkenhorts et al. 2015
Australialaisessa tutkimuksessa, jossa seurattiin 1469 ikääntynyttä naista, tyydyttyneiden rasvojen saannin korkeimmalla kvartiililla kumulatiivinen ateroskleroottinen verisuonikuolleisuusriski verrattuna alimpaan kvartiilin oli noin 16 % korkeampi.
Guasch-Ferre et al. 2015
Predimed-havainnointiraportissa tyydyttyneiden rasvahappojen ja transrasvojen saannin äärimmäisten kvintiilien vertailussa eniten tyydyttyneitä rasvoja saaneilla havaittiin 81% suurempi kardiovaskulaaristen sairauksien riski (336 tapahtumaa).
Farvid et al. 2014
analysoi linolihapon (omega-6) ja sepelvaltimotautien välistä yhteyttä (kaikki sepelvaltimotaudin lopputulokset: sydäninfarkti, iskeeminen sydänsairaus, sepelvaltimon ohitusleikkaus, äkillinen sydämenpysähdys, akuutti sepelvaltimo-oireyhtymä ja sydän- ja verisuonitauteihin liittyvät kuolemat).
Tutkijat sisällyttivät meta-analyysiin 6 kohorttia dieetin ja sepelvaltimotaudin kohorttitutkimusten Pooling-projektista: ateroskleroosiriski yhteisöissä -tutkimus (ARIC), Suomen liikkuvan klinikan terveystutkimus (FMC); Israelin iskeemisen sydänsairauden tutkimus (IIHD); Iowan naisten terveystutkimus (IWHS); Västerbottenin interventio-ohjelma (VIP) ja naisten terveystutkimus (WHS). Malmön ruokavalion ja syöpäkohortin (Malmö Diet and Cancer Cohort) tutkijat toimittivat tutkimukselle dataa. NHS (Nurses Health Study) ja HPFS (Health Professionals Follow Up Study) päivitettiin: NHS:ssä 20 vuodesta 30 vuoteen ja HPFS:ssä 6 vuodesta 24 vuoteen. ATBC-tutkimuksen tiedot analysoitiin uudelleen sekoittavien muuttujien mukauttamiseksi samalla tavalla kuin muut tähän meta-analyysiin sisältyvät kohorttitutkimukset. Muita tutkimuksia olivat Monica-tutkimus Tanskassa ja Morgen-tutkimus Alankomaissa sekä MRFIT-tutkimus.
Tutkimuksen tarkoituksena oli arvioida omega-6-linolihapon (LA) yhteyttä sydän- ja verisuonitauteihin ja näiden aiheuttamiin kuolemantapauksiin.
Meta-analyysi ei sisältänyt Kuopion tai Glostrupin tietoja, jotka ovat molemmat pieniä. 13 kohorttitutkimuksessa oli yhteensä 310 602 henkilön terveystiedot ja 12 479 CHD-tapahtumaa, mukaan lukien 5882 CHD-kuolemaa.
Kymmenessä kohortissa raportoitiin kardiovaskulaaristen tapahtumien tulokset. Kahdessa tutkimuksessa ei raportoitu kardiovaskulaarikuolemia. Verrattuna korkeimpaan alimpaan luokkaan, ruokavalion linolihappo (omega-6) liittyi 15% pienempään kardiovaskulaaristen tapahtumien riskiin ja 21% pienempään sydänsairauskuolemien riskiin.
Korvaamalla 5%:n tyydyttyneiden rasvojen energiansaannista omega-6-rasvoilla laski 9% CHD-tapahtumien riskiä ja 13% pienempään CHD-kuolleisuuden riskiin. Verrannollisia arvioita saatiin, kun linolihappovan korvaavasi hiilihydraateista saatavaa energiaa.
Vastakkaisia tuloksia saatiin Chowduryn meta-analyysistä, jossa ruokavalion omega-6-rasvat eivät laskeneet sydäntautiriskiä kahdeksassa kohorttitutkimuksessa, jotka sisälsivät 206 376 henkilön terveystietoja. Kohortit olivat Morgen, MRFIT, Glostrup, Kuopio, Malmo, ATBC, NHS ja HPFS. Farvidin meta-analyysi sisälsi kuusi kohorttitutkimusta enemmän kuin Chowdhuryn meta-analyysi. Nämä 6 kohorttia olivat Pooling-projektista plus Tanskan Monica. Chowdury et al. ei tutkinut erikseen Willett-ryhmän suorittamaa makroravinteiden korvaamista ja tutki vain tyydyttyneiden ja tyydyttymättömien rasvojen saannin tertiilejä suhteessa sydämen päätepisteisiin.
Wang et al. 2016
raportoi yhdistettyjen sairaanhoitajien ja terveydenhuollon ammattilaisten seurantatutkimuksesta. Tutkimus keskittyi kokonaiskuolleisuuteen (3 439 954 henkilöä ja 33 304 kuolemaa). Runsas rasvan saanti ja pienempi hiilihydraattien saanti assosioitui 16%:n pienempään kuolleisuuteen.
Li et ai., 2015
tarkasteli samoja kahta kohorttia päivitetyssä analyysissä (84 628 naista (sairaanhoitajien terveystutkimus, 1980-2010) ja 42 908 miestä (terveydenhuollon ammattilaisten seurantatutkimus, 1986-2010) ruokavalion rasvaa suhteessa CHD-riskiin. 24–30 seurantavuoden aikana esiintyi 7667 CHD-tapausta. Suuremmat monityydyttymättömien rasvahappojen saannit liittyivät merkittävästi pienempään sydäntauti-riskiin.
Hiilihydraatit (puhdas tärkkelys / lisätty sokeri) liittyivät positiivisesti lisääntyneeseen sydänsairauden riskiin. Valkoisten viljojen ja lisätyn sokerin korvaaminen täysjyväviljoilla assosioitui pienempään sydäntautiriskiin. PUFA ei eronnut merkittävästi MUFA:sta, mutta se poikkesi täysjyvästä.
Mozaffarianin meta-analyysi, 2010
Usein viitattu Mozaffarianin meta-analyysi päätyi tulokseen, että pitkällä aikavälillä tyydyttyneiden rasvojen korvaaminen monityydyttämättömillä rasvoilla parantaa sydänterveyttä, mutta tyydyttyneiden rasvojen korvaaminen hiilihydraateilla ei Mozaffarianin meta-analyysin mukaan paranna sydänterveyttä.
Mozaffarianin tutkimuksessa on mukana kaksi tutkimusta (suomalaiset mielisairaalatutkimukset), jotka eivät täytä Mozaffarianin tutkimukselleen asettamia kriteereitä. Kun ne poistetaan, myös hatara yhteys sydäntautien ja tyydyttyneiden rasvojen välillä katoaa.

Ramsdenin löytämät unohdetut tutkimukset
Sydneyn ruokavalio-sydäntutkimus (Sydney Diet Heart Study)
Sydneyn ruokavalio-sydäntutkimus oli kontrolloitu satunnaistettu tutkimus, johon osallistui 458 miestä vuosina 1966–1973. Tutkimuksen tavoitteena oli selvittää kuinka tyydyttyneen rasvan korvaaminen safloriöljystä (ja margariinista) saatavilla monityydyttämättömillä rasvahappoilla (PUFA) vaikuttaa terveyteen. Safloriöljy sisältää vain linolihappoa (omega-6).
Interventiotutkimus jatkui 2-7 vuotta, mediaanin ollessa hieman yli 3 vuotta.Tutkimuksesta julkaistiin yksi raportti vuonna 1978, jonka jälkeen Sydney Diet Heart Study unohdettiin vuosikymmeniksi. Julkaistussa raportissa todettiin, että vaikka omega-6-rasvaa saaneen ryhmän seerumin kokonaiskolesteroli laski hieman verrattuna kontrolliryhmään, interventioryhmässä kuolleisuus kaikkiin syihin lisääntyi.
Interventioryhmän 221 miehestä 37 kuoli. Kontrolliryhmän 237 miehestä 28 kuoli. Tutkijat totesivat, että omega-6-PUFAa saavassa interventioryhän miehillä oli 70-74 % korkeampi sydän- ja verisuonitautikuolleisuuden riski.
Sydney Diet Heart Studyn päivitetty analyysi, jossa yhdistettiin kolme vastaavaa tutkimusta, vahvisti, että tyydyttyneiden rasvojen korvaaminen vain omega-6 PUFA:lla liittyi 33% suurempaan sydän- ja verisuonitautikuolleisuuden riskiin.
Sydneyn tutkimusta on kritisoitu siitä, että safloriöljyä sisältävä margariini sisälsi runsaasti haitallisia transrasvoja. Se voi selittää omega-6 rasvojen kuolleisuutta lisäävän vaikutuksen. Transrasvat kuitenkin lisäävät yleensä kolesterolia, mutta interventioryhmässä kolesteroli sen sijaan laski. Se herättää kysymyksiä.
Minnesotan sepelvaltimotutkimus (Minnesota Coronary Study)
Minnesotan sepelvaltimotutkimus on suurin tutkimus, jossa on tutkittu millaisia vaikutuksia tyydyttyneen rasvan korvaaminen n-6 PUFA:lla aiheuttaa. Se oli kaksoissokkoutettu kontrolloitu satunnaistettu tutkimus, joka toteutettiin vuosina 1968–1973. Siihen osallistui 4393 miestä ja 4664 20–97-vuotiasta naista kuudesta mielisairaalasta ja yhdestä hoitokodista. Kyse oli ensisijaisesti ennaltaehkäisevästä tutkimuksesta, koska vain 392:lla oli elektrokardiografisia todisteita aikaisemmasta sydäninfarktista.
Interventioryhmän jäsenet noudattivat ruokavaliota, jossa tyypilliset rasvalähteet (voi ja muut eläinperäiset tyydyttyneet rasvat) korvattiin maissiöljyllä ja maissiöljypohjaisella margariinilla. Koska laitosten ruokaa tarjoillaan kahvila-tyyliin, tutkijat pystyivät tekemään kaksoissokkoutetun tutkimuksen.
Vain noin neljännes koehenkilöistä oli kokeessa vähintään vuoden. Mielenkiintoinen tosiasia tässä tutkimuksessa on, että vaikka se päättyi vuonna 1973, tulokset julkaistiin akateemisessa lehdessä vasta vuonna 1989. Tuossa julkaisussa kirjoittajat eivät ilmoittaneet eroja sydän- ja verisuonitapahtumissa tai kuolleisuudessa koko tutkimuspopulaatiossa huolimatta seerumin kokonaiskolesterolitason merkittävästä 15 prosentin laskusta interventioryhmässä.
Yksityiskohtaisempi analyysi tutkimusaineistosta ja monet alaryhmätulokset, jotka eivät sisältyneet vuoden 1989 julkaisuun, sisältyivät vuonna 1981 julkaistuun diplomityöhön. Työssä esitetyt taulukkoanalyysit viittasivat lisääntyneeseen kuolleisuusriskiin ≥ 65-vuotiaiden keskuudessa interventioryhmässä. Tuloksia ei kuitenkaan koskaan julkaistu akateemisessa lehdessä.
Ramsden et al. palautti osan alkuperäisistä tiedoista, jotka oli tallennettu magneettinauhoille ja paperiasiakirjoihin, ja julkaisi vuonna 2016 kumulatiivisen kuolleisuuden taulukot koko tutkimuspopulaatiosta ja ennalta määritellyistä alaryhmistä, jotka oli julkaistu alun perin vasta opinnäytetyössä vuonna 1981.
Palautetut tiedot eivät osoittaneet tilastollisesti merkitseviä eroja interventio- ja vertailuryhmien välillä aortan ja sepelvaltimoiden ateroskleroosissa 298 päivän mediaaniseurannan jälkeen, mutta sen sijaan havaittiin, että sydäninfarktin esiintyvyys oli interventioryhmän ruumiinavausdatan perusteella 90 % korkeampi.
Näiden tulosten lisäksi kirjoittajat tekivät myös meta-analyysin, jossa he yhdistivät Minnesotan sepelvaltimotutkimuksen tulokset neljään vastaavaan, mutta huomattavasti pienempään tutkimukseen, joissa tyydyttynyt rasva oli korvattu omega-6 (PUFA)-rikkailla kasviöljyillä.
Yhdistetyt tulokset eivät osoittaneet vaikutusta sydän- ja verisuonitauteihin tai kaikkien syiden kuolleisuuteen huolimatta seerumin kokonaiskolesterolipitoisuuksien keskimääräisestä 8-14% laskusta interventioryhmissä verrattuna kontrolliryhmiin.
Tutkimuksen merkittävä rajoitus, kuten myös Ramsden on todennut, on, että vain pieni osa rekrytoiduista henkilöistä pysyi tutkimuksessa vähintään vuoden. Esimerkiksi uusin Cochrane-katsaus ei sisältänyt Minnesotan sepelvaltimotutkimusta tästä syystä. Kuten myös kirjoittajat huomauttivat, näiden analyysien tuloksia tulisi tulkita varovaisesti, koska palautettujen tietojen kohteiden lukumäärä on pieni. Kevyesti hydratun maissiöljymargariinin, tärkeimmän transrasvojen lähteen käyttö interventioryhmässä on saattanut vaikuttaa tuloksiin.
Rasvasota näyttää jatkuvan: Tyydyttyneet rasvahapot (SFA) eivät lisää sydän- ja verisuonitautien (CVD) riskiä osoitti kaksi äskettäin julkaistua satunnaistettujen kontrolloitujen tutkimusten (RCT) analyysiä. SFA:n korvaaminen linolihapolla lisäsi CVD-riskiä yhdessä tutkimuksessa. Lisäksi äskettäin tehdyssä suuressa prospektiivisessa kohorttitutkimuksessa raportoitiin pienemmästä sydän- ja verisuonitautiriskistä lisääntyneellä SFA-energian saannilla, ja kohorttitutkimusten viimeaikaisissa meta-analyyseissä todettiin, että SFA ei lisännyt sydän- ja verisuonitautien riskiä.
Tyydyttyneiden ja trans-rasvahappojen pelkistämisestä johtuviin terveyshyötyihin viittaavia vastalauseita on kuitenkin lukuisia, mukaan lukien äskettäin julkaistut RCT:t, prospektiiviset kohorttitutkimukset ja ekologiset tutkimukset. Vaikuttaakin siltä, että tieteellä ei ole selkeää vastausta tyydyttyneiden rasvojen terveysvaikutuksista huolimatta valtavasta työstä. Jos joku väittää, että on kiistattomia todisteita siitä, että tyydyttyneet rasvat lisäävät sydäntautien riskiä, hän ei tiedä mistä puhuu tai valehtelee. Tiedot ovat hajanaisia ja ristiriitaisia.
Tutkimukset eivät ole samanarvoisia. Luotettavimpia tutkimuksia ovat systemaattiset kirjallisuuskatsaukset, meta-analyysit ja satunnaistetut kontrolloidut tutkimukset (erityisesti sokkoutetut satunnaistetut kontrolloidut tutkimukset).
Epidemiologiset seurantatutkimukset antavat epäluotettavia tietoja, koska ravitsemusta käsittelevissä seuranta- ja kyselytutkimuksissa ihmiset unohtavat ja valehtelevat tietoisesti tai tietämättään.
Mihin jäinkään?
Ai niin! Tämän tutkimuskatsauksen mukaan tyydyttyneitä rasvoja sisältävät ruokavaliot johtavat matala- asteiseen tulehdustilaan (inflammaatio) ja insuliiniresistenssiin. Tästä, kuten rasvojen vaikutuksista terveyteen on myös päinvastaisia tutkimustuloksia. Avataan tätä hieman.
Insuliiniresistenssin havainnut Joseph Kraft uskoi, että lähes kaikki sydän- ja verisuonitaudit johtuvat diagnosoidusta tai diagnosoimattomasta diabeteksesta.
Insuliiniresistenssi vaikuttaa tyypin 2 diabeteksen sekä sydän- ja verenkiertoelimistön sairauksien kehittymiseen.
Insuliiniresistenssi on monien elämäntapasairauksien taustalla vaikuttava juurisyy. Lihas-, rasva- ja maksasolujen heikentynyt kyky ottaa vastaan glukoosia ylläpitää veren korkeaa glukoosipitoisuutta. Samalla puutteellisesti energiaa saavat solut surkastuvat, sairastuvat ja kuolevat.
Jatkuvasti korkea verensokeri edistää sokereiden glykatoitumista rasvojen ja proteiinien kanssa. Glykotoksiinit aiheuttavat oksidatiivista stressiä, joka puolestaan kasvattaa sydän- ja verenkiertoelimistön sairauksien riskiä. Elimistö yrittää päästä eroon ylimääräisistä sokereista lisäämällä virtsan eritystä. Diabetes, eli sokeritauti tunnettiin tämän vuoksi aiemmin makeavirtsaisuutena.
Insuliiniresistenssin riskitekijöitä on useita, kuten ylipaino, lihavuus, verenpaine, vaihteleva vuorokausirytmi, D-vitamiinin puute ja vähän liikuntaa sisältävä elämäntapa. Erilaiset geneettiset ja epigeneettiset tekijät voivat laukaista insuliiniresistenssiin johtavan aineenvaihduntahäiriön.
Ruokavaliotekijät vaikuttavat insuliiniresistenssiin, mutta kausaatiota eri ravintoaineille on vaikea määrittää ravintotutkimuksen rajoitusten vuoksi. Ruokiin, jotka liittyvät insuliiniresistenssiin, lukeutuvat runsaasti sokeria sisältävät korkean glykeemisen indeksin ruoat, runsaasti rasvaa ja fruktoosia sisältävät ruoat sekä vähän omega-3-rasvoja ja kuitua sisältävät ruoat.
Yksinkertaistaen: insuliiniresistenssiä lisäävät erityisesti herkut, kuten pikaruoat, makeiset, keksit jne. jotka sisältävät runsaasti sokereita ja huonoja rasvoja. Runsaasti rasvaa ja sokeria sisältäviä ruokia sekä sokeroituja juomia pidetään perustekijöinä metabolisen oireyhtymän taustalla.
Ruokavalio voi myös muuttaa monityydyttymättömien ja tyydyttyneiden fosfolipidien suhdetta solukalvoissa. Monityydyttymättömien rasvahappojen (PUFA) prosenttiosuus korreloi käänteisesti insuliiniresistenssin kanssa. Oletetaan, että solukalvon juoksevuuden lisääminen lisäämällä PUFA-pitoisuutta saattaa johtaa lisääntyneeseen insuliinireseptorien määrään, insuliinin lisääntyneeseen affiniteettiin sen reseptoreihin ja parempaan insuliinisensitiivisyyteen. Solukalvojen rakenteelliset muutokset voivat toisaalta altistaa inflaamaatiolle ja heikentää immuunijärjestelmän toimintaa.
D-vitamiinin puute ja monet hormonit, kuten kortisoli ja kasvuhormoni vaikuttavat insuliiniresistenssiin, Kortisoli vastustaa insuliinia. Stressihormonina tunnetun kortisolin eritys vähenee ketogeenisellä ruokavaliolla. Sokereiden rajoittamisen seurauksena autonomista hermostoa kiihdyttävästä glutamaatista syntetisoidaan hermostoa rauhoittavaa GABAa. Tällä on suotuisia terveysvaikutuksia. Edelleen tämä johtaa lisääntyneeseen maksan glukoneogeneesiin, vähentää glukoosin perifeeristä hyödyntämistä ja lisää insuliiniresistenssiä. Kortisoli tekee tämän vähentämällä glukoosikuljettajien (erityisesti GLUT4) siirtymistä solukalvoon.
Myös leptiinin aineenvaihdunnan häiriöt liittyvät insuliiniresistenssiin. Leptiini on rasvakudoksen erittämä hormoni, jonka fysiologisena tehtävänä on säädellä kylläisyyden tunnetta. Tutkimukset osoittavat, että leptiinin puute ja leptiiniresistenssi lisäävät sairaalloista lihavuutta ja liittyvät vahvasti insuliiniresistenssiin, metaboliseen oireyhtymään ja diabetekseen.
Akuutti ja krooninen tulehdus voivat aiheuttaa insuliiniresistenssia. Esimerkiksi tulehdukseen liittyvä TNF-a voi edistää insuliiniresistenssiä edistämällä lipolyysiä, häiritsemällä insuliinin signalointia ja vähentämällä GLUT4:n ilmentymistä.
Monen geneettisen lokuksen on todettu liittyvän insuliiniherkkyyteen. Tähän sisältyy vaihtelu paikoissa lähellä NAT2-, GCKR- ja IGFI-geenejä, jotka liittyvät insuliiniresistenssiin. Tutkimukset ovat vahvistaneet, että näiden geenien lähellä olevat lokit ovat yhteydessä insuliiniresistenssiin. Näiden lokusten arvioidaan kuitenkin muodostavan vain 25–44% insuliiniresistenssin geneettisestä vaikutuksesta.
Insuliiniresistenssi ylläpitää lipogeneesiä, jossa insuliini laskee veren korkeaa sokeripitoisuutta varastoimalla glukoosia rasvasoluihin. Glukoosi muutetaan rasvasoluissa triglyserideiksi. Tämä kasvattaa rasvakudosta ja heikentää rasvakudoksen leptiinisignalointia. Lihassolujen puutteellinen energiansaanti kasvavan rasvakudoksen heikentämän leptiinisignaloinnin kanssa vaikuttaa lisäksi nälkähormoni greliinin eritykseen.
Greliini informoi aivoja ravinnon tarpeesta. Häiriintyneen greliinisignaloinnin seurauksena ihmisellä voi olla jatkuva nälkä, vaikka veressä olisi riittävästi energiaa koko päiväksi ja rasvakudokseen varastoitu energia kattaisi viikkojen energiantarpeen.
Energian tallentaminen rasvakudokseen on luonnollista.Varhaisilla ihmisillä ravinnon saanti ei ollut samalla tavoin turvattua kuin nykyihmisillä. Metsästäjä-keräilijät sattoivat elää hyvin niukalla tai olemattomalla ravinnolla päivistä viikkoihin, mutta kun ravintoa oli tarjolla, sitä tankattiin myös huonompien aikojen varalle.
Energian varastoimisessa insuliinilla on keskeinen rooli. Laihduttaessa insuliinin rooli on rasvan polttamista estävä, koska se ylläpitää lipogeneesiä ja estää lipolyysin käynnistymistä. Jatkuvasti korkea insuliinipitoisuus estää rasvsasoluihin varastoidun energian purkamisen vapaiksi rasvahapoiksi, joita solut voisivat käyttää energianlähteenä. Veren insuliinipitoisuus laskee lipolyysin käynnistymisen kannalta riittävästi keskimäärin 8 tuntia syömisen jälkeen. Se tarkoittaa, että keho voi hyödyntää rasvasolujen energiaa vain yöaikaan. Tehokkaan rasvanpolton aikaikkuna jää silloin melko lyhyeksi.
Insuliiniresistenssi lihottaa koska insuliini on anabolinen hormoni, joka säätelee energiaravinteiden käyttöä ja varastoimista. Jatkuvasti korkea veren insuliinipitoisuus ja solujen heikentynyt insuliinisensitiivisyys ohjaavat ylimääräistä verensokeria rasvasoluihin. Samalla korkea insuliinipitoisuus ja solujen heikentynyt energiansaanti lisäävät nälästä kertovan greliinin eritystä ja laskevat kylläisyydestä kertovan leptiinin eritystä.
Matala-asteinen tulehdus
Tämän tutkimuskatsauksen mukaan tyydyttyneiden rasvojen saanti edistää lipopolysakkaridien imeytymistä suolistossa, mikä voi aiheuttaa tulehdusta [16, 17] sitoutumalla TLR-4:een, mikä liittyy korkeampaan CVD-riskiin. Lipopolysakkaridi on rasvahapon ja suurimolekyylisen hiilihydraatin muodostama molekyyli. Lipopolysakkaridit voivat aktivoida immuunijärjestelmän, sillä niitä on esimerkiksi monien gramnegatiivisten bakteerien ulkokalvossa. TLR-2:n aktivaatio, keramidituotanto ja lipidilauttojen muodostuminen näyttävät liittyvän myös tulehdusprosessiin tyydyttyneen rasvan vuoksi [18–20].
Matala-asteinen tulehdus on sydän- ja verisuonitautien riskitekijä. Ateroskleroosiin liittyy jatkuva tulehdusvaste. Viimeaikaiset perustutkimuksen havainnot ovat vahvistaneet matala-asteisen tulehduksen perustavan roolin ateroskleroosin kehittymisessä. Inflammaatio välittää kaikkia ateroskleroosin vaiheita taudin alusta aina tromboottisiin komplikaatioihin asti.
Tutkimuksissa on havaittu selkeitä yhteyksiä riskitekijöiden ja aterogeneesimekanismien välillä. Kliiniset tutkimukset osoittavat, että ateroskleroosiin liittyvät tulehdusmekanismit toteutuvat myös ihmisillä. Tulehduksesta kertovien markkereiden lisääntyminen kertoo kasvaneesta sydän- ja verisuonitautien riskistä. Krooninen matala-asteinen tulehdus (kohonnut C-reaktiivisen proteiinin CRP-taso) määrittelee prospektiivisesti ateroskleroottisten komplikaatioiden riskiä. Yhdessä muiden tunnettujen riskitekijöiden kanssa tulehdusmarkkerit voivat auttaa tunnistamaan korkeamman riskin henkilöitä entistä aiemmin.
Eräät sepelvaltimotaudin hoidot hillitsevät myös kroonista matala-asteista tulehdusta. Statiineihin liittyvän lipiditason alenemisen tulehdusta estävä vaikutus ei korreloi pienitiheyksisten lipoproteiinitasojen laskun kanssa. Uudet havainnot ateroskleroosiin liittyvistä tulehdustekijöistä lisäävät ymmärrystämme ateroskleroosin mekanismeista ja tarjoavat kliinisiä sovelluksia riskien kartoittamiseen ja hoitojen kohdistamiseen.
Krooninen inflammaatio on keskeinen tekijä sydän- ja verisuonitautien patogeneesissä, mutta se assosioituu vahvasti myös diabeteksen, dementian ja masennuksen kasvaneeseen alttiuteen. Matala-asteinen tulehdus lisää riskiä kuolla mihin tahansa syyhyn. Sellaisten riskitekijöiden tunnistaminen, jotka voisivat tehokkaasti vähentää kroonista tulehdusta, edistäisi tehokkaasti kroonisten sairauksien ehkäisyä.
Sokeri
Runsaasti sokeria sisältävä ruokavalio (erityisesti sokerilla makeutetut juomat voivat olla yksi subkliinisen C-reaktiivisella proteiinilla (CRP) mitattavan matala-asteisen tulehduksen aiheuttajista. Sokeria kulutetaan runsaasti länsimaisissa ruokavalioissa. 18 kehittyneen maan lisätyn sokerin kulutusta verrattaessa havaittiin, että lisätyn sokerin kokonaissaanti prosentteina energiasta vaihteli aikuisilla 13,5–24,6 % välillä.
Yhdysvalloissa valtakunnalliset elintarvikkeiden kulutuskyselyt (NHANES) ovat arvioineet, että fruktoosimaissisiirapin (HFCS) prosenttiosuus makeutusaineena kasvoi16 prosentista (1978) 42 prosenttiin (1998) ja vakiintui sille tasolle. Samanlainen suuntaus havaittiin myös fruktoosin kokonaiskulutuksessa.
Tuoreimmat tiedot osoittavat, että yleisen tietoisuuden lisääntyessä lisätyn sokerin kulutus Yhdysvalloissa on laskenut vuosina 1999–2008 keskimäärin 18,1 prosentista 14,6 prosenttiin. Sokerista saatavan energian kokonaissaanti on kuitenkin edelleen paljon suurempi kuin Yhdistyneen kuningaskunnan ravitsemuksellisen neuvoa-antavan komitean (SACN) ohjeet, joissa suositellaan, että listättyjen sokereiden enimmäismäärä on 5% päivittäisestä energiansaannista. Myös Maailman terveysjärjestön (WHO) suositus lisätylle sokerille on 5 % päivittäisestä energiasta.
Runsas sokeri edistää maksassa olevien vapaiden rasvahappojen (FFA) de novo -synteesiä, mikä lipotoksisuusteorian mukaan tuottaa FFA-metaboliitteja, jotka voivat laukaista tulehdusprosesseja. ja reaktiivisten happilajien (ROS) muodostumista.
Elimistön kaikki solut osaavat hyödyntää glukoosia. Fruktoosin aineenvaihdunta, eli fruktolyysi tapahtuu maksassa. Koska ei ole olemassa negatiivisia takaisinkytkentämekanismeja, jotka kontrolloivat ja estävät fruktoosin ylimääräisen saannin maksan mitokondrioissa, fruktoosi muuttuu itsenäisesti osittain asetyyli-CoA: ksi, joka on rakennusosa rasvahapposynteesille.
Fruktoosin metabolinen reitti tukee lipotoksisuuden teoriaa, mutta vielä ei tiedetä onko sakkaroosin sisältämä fruktoosi merkittävämpi inflammaation aiheuttaja kuin glukoosi.
Interventiotutkimuksista saatu näyttö todistaa, että fruktoosiannokset, jotka tuottavat ylimääräistä energiaa (+ 21–35% ) nostavat maksarasvoja. Tätä vaikutusta näyttää kuitenkin sekoittavan liiallinen energian saanti.
Ruokavalion fruktoosimetabolian on vahvistettu edistävän vapaiden rasvahappojen de novo -synteesiä maksassa, kun fruktoosin saanti on runsasta. Vaikka triglyseridien lisääntyminen maksassa näyttää olevan hyvänlaatuisen steatoosin oire, on alustavaa näyttöä siitä, että vapaiden rasvahappojen (FFA) metaboliitit voivat edistää alkoholista riippumattoman rasva-maksasairauden (NAFLD) etenemistä alkoholista riippumattomaksi steatohepatiitiksi (NASH) lisäämällä vapaiden happiradikaalien (ROS) määrää ja käynnistämällä tulehdusprosesseja, jotka johtavat maksasolujen apoptoosiin ja maksan arpeutumiseen eli kirroosiin.
Kudosbiopsioiden tutkimukset vahvistavat tulehduksellisten biomarkkereiden, kuten CRP, IL-6 ja IL-1RA systeemisten tasojen asteittaisen kasvun terveestä rasvakudoksesta runsaasti immuunisoluja sisältävään rasvakudokseen ja terveestä maksasta alkoholista riippumattomaan steatohepatiittiin (NASH).
On perusteltua olettaa, että erityisesti runsas fruktoosin saanti rasittaa ja vaurioittaa maksaa. Laajassa systemaattisessa kirjallisuuskatsauksessa (lue tästä) ei havaittu merkittävää eroa sillä, onko maksan metaboloima fruktoosi peräisin sakkaroosista (pöytäsokeri), fruktoosista vai fruktoosisiirapista (HFCS). Tämä vahvistaa sen, että ylimääräinen sokeri lähteestä riippumatta vaurioittaa maksaa.
Tulevissa tutkimuksissa maksan rasvoittumista ja de novo lipogeneesia pitäisi tarkastella NAFLD:n mrkkerina, samalla kun mitataan sellaisia spesifisempiä tulehdusmarkkereita, jotka ovat yhteydessä maksarasvaan, esim. fetuiini A. Se viittaa fruktoosinkulutuksen ja lisääntyneen viskeraalisen rasvakudoksen väliseen yhteyteen.
Viskeraalinen rasvakudos tuottaa tulehduksellisia sytokiineja, kuten TNF-a ja IL-6, jotka puolestaan voivat lisätä C-reaktiivisen proteiinin vapautumista maksassa. Runsas sokerin saanti lisää erityisesti viskeraalista rasvaa, joka ylläpitää matala-asteista tulehdusta erittämällä tulehdussytokiinejä.
Eläintutkimuksissa fruktoosi on aiheuttanut suoliston eräiden mikrobipopulaatioiden ylikasvua ja lisääntynyttä suoliston läpäisevyyttä. Tämän seurauksena lipopolysakkaridien endotoksiinitasot siirtyvät ja aktivoivat Tollin kaltaisen reseptorin 4 maksan Kupffer-soluissa. Aktivaatio johtaa useiden sytokiinien, kuten TNF-a:n eritykseen.
Gersch et al. raportoi, että runsaasti fruktoosia sisältävä ruokavalio lisää merkittävästi munuaisten MCP-1-ekspressiota rotilla. In vitro -tutkimus ihmisen epiteelin tubulaarisoluilla viittasi fruktoosin, mutta ei glukoosin, indusoimaan MCP-1-tuotannon aktivaatioon.
Glukoosin erityisestä roolista oksidatiivisissa tapahtumissa on todisteita
Korkean glykeemisen indeksin ravinto liittyy nopeasti syömisen jälkeen (postbrandiaalisesti) ilmeneviin lisääntyneisiin tulehdusvasteisiin vasteena hyperglykemialle. Myöhemmässä postbrandiaalisessa vaiheessa vapaiden rasvahappojen määrä lisääntyy. Molemmat tekijät lisäävät vapaiden radikaalien tuotantoa ja proinflammatoristen sytokiinien vapautumista, mikä aiheuttaa inflammaatiota ja vaihingoittaa verisuonia.
Fruktoosilla on alhainen glykeeminen indeksi (GI). Matalan glykeemisen indeksin ravinnon tiedetään hillitsevän inflammaatiota. Voi siis olla, että fruktoosi osittain hillitsee runsaasti sokeria sisältävän ravinnon aiheuttamaa tulehdusreaktiota. Näin voi tapahtua tietyillä metaboliareiteillä vasteena muihin ravinteisiin.
Koska lihominen ja runsas sokerin saanti liittyvät toisiinsa ja toisaalta lihavuus ja matala-asteinen tulehdus liittyvät toisiinsa, on mahdollista, että painonnousu on välittäjä sokerin ja matala-asteisen tulehduksen välillä.
Vertaamalla sokereiden eukalorisia ja hyperkalorisia vaikutuksia tulehdusmarkkereihin saadaan merkityksellistä tietoa sokerin matala-asteiseen tulehdukseen yhdistävistä metabolisista reiteistä. Havaintoja voidaan hyödyntää kansanterveyden parantamisessa. Vielä ei ole varmuutta johtaako liika energian saanti (rasvasta tai proteiineista) samanlaisiin negatiivisiin terveyshaittoihin kuin liika sokereista saatu energia?
Sievenpiper et al. havaitsi, että fruktoosi vaikutti painonnousuun vain hyperkalorisissa ja isokalorisissa kokeissa. Eli lihottava vaikutus ei johtunut yksin fruktoosista, vaan ylimääräisestä energiasta.
Kun huomioidaan lihavuuden ja matala-asteisen tulehduksen välinen suhde, keskustelu painon muutoksesta mukana olevissa kokeissa olisi tarkoituksenmukaista. Energiarajoitetuista ruokavalioista johtuva painonpudotus liittyi tulehdusmarkkereiden parempaan parantumiseen (fruktoosin saannin määristä riippumatta) kahdessa tutkimuksessa.
Lisätyt sokerit ja puhdistetut tärkkelykset
Joidenkin tutkimusten mukaan ylipainoiset ja lihavat ihmiset syövät normaalipainoisia enemmän sokeria ja puhdasta tärkkelystä sisältäviä elintarvikkeita.
Ylipainon ja lihavuuden riski kasvaa ~14 % jos päivittäistä sokerin saantia lisätään vain viidellä grammalla [23 ]. Ruokavaliot, joissa on paljon lisättyjä sokereita ja puhdistettua tärkkelystä liittyvät korkeampaan veren paasto-triglyseridien pitoisuuteen. Triglyseridit assosioituvat vahvasti sydäntautien riskiin. Sen sijaan tiedot tärkkelyksen ja sokerin vaikutuksista LDL-kolesteroliin ovat ristiriitaisia.
American Heart Associationin (AHA) lausunnossa suositeltiin vähentämään lisättyjen sokereiden määrää ja välttämään fruktoosilla makeutettuja elintarvikkeita. Fruktoosin tiedetään lisäävän alkoholista riippumattoman rasvamaksan riskiä [24– 27].
Ruokavaliot, joissa on paljon tärkkelystä ja lisättyjä sokereita lisäävät glukoosin de novo lipogeneesiä ja maksan rasvoittumista. Insuliiniresistenteillä ihmisillä solujen insuliiniherkkyys on heikentynyt. Solujen heikentynyt kyky ottaa glukoosia vastaan ylläpitää korkeaa verensokeria. Ylimääräinen sokeri varastoidaan ensisijaisesti maksan ja lihasten glykogeeneihin, mutta koska glykogeeneihin mahtuu vain ~250 g glukoosia, ne täyttyvät sokeripitoisella ruokavaliolla hyvin nopeasti. Jos veren korkeaa sokeripitoisuutta ei voida käyttää energiaksi tai varastoida glykogeeneihin, se varastoidaan rasvasoluihin.
Lisättyjen sokereiden ja puhdistetun tärkkelyksen muuttuminen rasvaksi tuottaa triglyseridejä, jotka liittyvät kohonneeseen CVD-riskiin. Fruktoosi on tärkein sokeri, joka liittyy de novo lipogeneesiin sen maksassa tapahtuvan aineenvaihdunnan vuoksi. Glukoosi metaboloituu pääasiassa maksan ulkopuolisissa kudoksissa, kuten lihaskudoksessa [28]. Fruktoosi liitty insuliiniresistenssiin [29].
Kirjallisuudessa on ristiriitaisia tietoja lisättyjen sokereiden vaikutuksesta verenpaineeseen, mutta viime aikoina on saatu vahvaa näyttöä siitä, että sokereita rajoittava ketogeeninen ruokavalio laskee verenpainetta ja verensokeria. Hiljatain julkaistu meta-analyysi osoitti, että lisättyjen sokereiden käytöllä isoenergeettisessä ruokavaliossa ei ole kielteisiä vaikutuksia verenpaineeseen [30]. Eli tästäkään ei vallitse selvää yksimielisyyttä. Luultavasti selitystä voidaan etsiä ruokavaliosta kokonaisuutena, eikä vain yhdestä ravintoaineesta.

Ravintokuidut
Ravinnon sisältämien kuitujen vähäinen saanti liittyy kohonneeseen sydän- ja verisuonitautien riskiin. Hedelmiä, vihanneksia ja täysjyviä sisältävissä ruokavalioissa on runsaasti kuituja. [31].
Kuitujen myönteiset vaikutukset sydän- ja verisuoniterveyteen johtuvat useista tekijöistä, kuten:
- sappihappojen erittymisen lisääntymisestä
- kolesterolitasojen alentamisesta [32]
- rasvahapposynteesin vähenemisestä maksassa fermentaation tuloksena syntyvien lyhytketjuisten rasvahappojen tuotannolla [33]
- insuliiniherkkyyden lisääntymisestä [34]
- kylläisyyden tunteen lisääntymisestä, mikä johtuu siitä, että kuitu lisää ruokamassaa, mikä johtaa ruoan saannin vähenemiseen ja edelleen pienempään energiansaantiin [35].
Kirjallisuuskatsaustiedot osoittavat ravintokuitujen saannin, CVD:n ja kokonaiskuolleisuuden välisen korrelaation. Hiljattain tehty tutkimus vahvisti, että vähän kuituja sisältävää ruokavaliota (~ 15,0 g / vrk) noudattavien ihmisten kokonaiskuolleisuus oli 23% suurempi kuin ihmisillä, jotka söivät runsaasti kuituja (∼26,9 g / vrk). Sukupuoli tai etninen tausta eivät vaikuttaneet tähän korrelaatioon [36].
Tuoreessa meta-analyysissä analysoitiin 15 kohorttitutkimusta, joissa oli 1 409 014 potilaan tiedot. Tämä tuki käsitystä ravintokuitujen ja CVD-kuolleisuuden käänteisestä korrelaatiosta [37].
Kuten aiemmin osoitettiin, kuitujen saanti ~ 29,6 g / vrk, joka on lähellä suositeltua 30 g / vrk -tasoa, liittyi CV-kuolleisuuden 23%: n laskuun verrattuna kuitujen vähäiseen saantiin ~ 14,0 g / vrk.
Hedelmät ja vihannekset
Vähäistä hedelmien ja vihannesten saantia pidetään yhtenä ennenaikaisen kuoleman tärkeimmistä syistä maailmanlaajuisesti. Liian vähäisen hedelmien ja vihannesten saannin arvioidaan johtaneen 25,5 miljoonaan ennenaikaiseen kuolemaan vuonna 2013 [38].
Hedelmien ja vihannesten hyödylliset vaikutukset johtuvat ravintokuiduista, vitamiineista, kivennäisaineista, polyfenoleista ja antioksidanteista, jotka hillitsevät matala-asteista tulehdusta ja vähentävät kroonisia sairauksia, kokonaiskuolleisuutta, sekä vaikuttavat suotuisasti suoliston mikrobiomiin [39, 40].
Lisäksi julkaistut tutkimusraportit antavat todisteita ravintokuitujen, hedelmien ja vihannesten saannin positiivisesta vaikutuksesta seerumin kolesterolitasoon, verenpainetasoon, tulehdukseen ja verihiutaleiden aggregaatioon [41].
Verrattain uusi meta-analyysi, jossa arvioitiin 95 ainutlaatuista kohorttitutkimusta, osoitti, että:
- sepelvaltimotaudin suhteellinen riski laskee 8–16% jokaisesta päivittäisestä 200 g:n hedelmien tai vihannesten sekä hedelmien ja vihannesten yhteissaantia kohden (suhteellisen riskin alenema? Se ei tarkoita mitään)
- Aivohalvauksen suhteellisen riski laski 13–18%
- CVD:n suhteellinen riski laski 8–13% [42]
- Ihmisillä, joiden ruokavalio sisältää runsaasti hedelmiä ja vihanneksia (∼500 g / päivä), sydän- ja verisuonitautien riski laskee 22% verrattuna ihmisiin, joiden saanti on vähäistä (0–40 g / päivä).
Suhteellisen riskin alenema on tilastollinen silmänkääntötemppu, jolla musta saadaan valkoiseksi ja valkoinen mustaksi. Sitä käytetään erityisesti lääkkeiden markkinoinnin välineenä. Esimerkiksi: Lipitor (statiini) laskee sydänkuolleisuutta 36 %. Huimaa, eikö totta?
Absoluuttisen riskin alenema on jotain ihan muuta. Lipitorian saaneessa ryhmässä sydänkuolleisuus oli 2 %, kun kontrolliryhmässä kuolleisuus oli 3,1 %. Absoluuttinen ero kuolleisuudessa oli 1,1 %, mikä mahtuu kaiken lisäksi virhemarginaaliin. Menisikö lääke kaupaksi väitteellä: laskee sydänkuolleisuutta ehkä 1,1 % ja voi aiheuttaa joukon vakavia sivuoireita? Kehotan suhtautumaan varauksella väitteisiin, joissa puhutaan suhteellisesta riskistä.

Keskustelua ravintokuiduista
Useat tutkimukset ovat korostaneet ravintokuidun etuja sydän- ja verisuoniterveydelle, koska kuidut parantavat lipidiprofiilia ja laskemavat verenpainetta. Ravintokuitujen vähäinen saanti liittyy suurempaan CVD-riskiin [43].
Ravintokuitujen runsas saanti liittyy pienempään kuolleisuuteen kaikista syistä [44]. Vaikka erityisiä toimintoja ja toimintamekanismeja ei ole täysin ymmärretty, ehdotetut mekanismit ovat, että ravintokuitu laskee kolesterolia, glukoosin imeytymistä ja vähentää oksidatiiviseen stressiin liittyvien sytokiinien tai suoliston mikrobiomin välittämää tulehdusreaktiota [45, 46].
Ravintokuidun suojaavaan rooliin näyttää vaikuttavan paitsi kuidun määrä myös kuidun tyyppi ja lähde [47]. Itse asiassa erityyppiset ravintokuidut tai -lähteet voivat olla vastuussa erilaisista fysiologisista vaikutuksista: liukoiset kuidut ovat vastuussa kolesterolia alentavasta vaikutuksesta, kun taas liukenemattomat kuidut vaikuttavat ruoan imeytymiseen suolistossa ja glykeemiseen vasteeseen [33, 48].
Äskettäin tehty tutkimus hypertensiivisten (hypertensio – verenpainetauti) hiirien kokeellisessa eläinmallissa osoitti, että kuidut ja asetaatti johtivat monien järjestelmien homeostaasia säätelevän transkriptiotekijän Egr1:n alasregulointiin. Egr1 moduloi useiden geenien ilmentymistä ja CVD-prosesseihin liittyviä signaalireittejä. Egr1 liittyy sydämen hypertrofiaan, munuaisfibroosiin ja inflammaatioon [49].
Lipidejä alentavan vaikutuksen osalta täysjyvät, siemenet ja pähkinät ovat sisältämänsä liukoisen kuidun vuoksi tärkeitä [50]. Monet tutkimukset ovat nostaneet esiin beeta-glukaanin (liukoinen kuitu) potentiaaliset terveyshyödyt. Beeta-glukaania saa enimmäkseen kaurasta ja ohrasta. Beeta-glukaanin kulutukseen on liittynyt ~5–10% alhaisempia triglyseridi- ja LDL-kolesterolitasoja [51–53].
Whitehead et al. korosti, että ruokavalio, joka sisälsi ~ 3 g kauran beeta-glukaania/ vrk, laski triglyseridien ja LDL-kolesterolin tasoja, mutta ilman merkittävää vaikutusta HDL-kolesteroliin. HDL ei laskenut, vaikka beeta-glukaanin saanti oli hyvin korkea (jopa 12,4 g / vrk).
Korkeampi LDL-kolesterolia alentava vaikutus havaittiin tyypin 2 diabetesta sairastavilla ja sellaisilla potilailla, joilla oli korkeampi lähtötason LDL-kolesteroli [54], mikä viittaa parempaan tehoon niillä, joiden metabolinen profiili on huonompi.
Mirman et al. teki prospektiivisen kohorttitutkimuksen 2295 terveellä koehenkilöllä, joita tutkimus seurasi 4,7 vuoden ajan. Tutkimuksen mukaan ravintokuitujen saannilla erityisesti palkokasveista, hedelmistä, vihanneksista ja pähkinöistä oli sydän- ja verisuonitaudeilta suojaava vaikutus.
Kasvikuitujen myönteiset vaikutukset CVD-riskin vähentämisessä näyttivät liittyvän triglyseridien vähenemiseen ja parantuneeseen triglyseridi-HDL-suhteeseen [55].
Toinen äskettäin tehty tutkimus korosti ravintokuitujen, suolen mikrobiomin ja sydän- ja verisuonitautien riskin pienentämisen välistä yhteyttä, mikä viittaa mikrobiomin mahdolliseen rooliin CVD-riskin moduloinnissa [56].
Monityydyttämättömät rasvahapot (PUFA): omega-3
Jatkuvasti lisääntyvä tutkimusnäyttö osoittaa, että omega-3-PUFA:lla on erilaisia kardioprotektiivisia ominaisuuksia, kuten plasman triglyseridien laskeminen, verenpaineen säätely, rytmihäiriöiden ja tulehdusten hillitseminen sekä endoteelin toimintahäiriöiden parantaminen [57].
Omega-3, erityisesti eikosapentaeenihappo (EPA) ja dokosaheksaeenihappo (DHA), ovat olleet pitkään tutkijoiden mikroskoopin alla. Havainnot ovat osoittaneet useita erilaisia mekanismeja, joilla kiertävät ja yhdistetyt omega-3-PUFA:t voivat toimia solu- ja molekyylitasoilla, mukaan lukien geneettiset ja epigeneettiset modulaatiot [58].
Esteröimättömät omega-3-rasvahapott tai niiden asyyli-CoA-tioesterit voivat sitoa ja moduloida suoraan tumareseptorien toimintaa ja transkriptiotekijöitä, jotka säätelevät geeniekspressiota useissa kudoksissa [59]. Nämä reseptorit ovat keskeisiä säätelijöitä monille CVD:hen liittyville solutoiminnoille, mukaan lukien lipidimetabolia, glukoosi-insuliinihomeostaasi ja inflammaatio [60].
On mielenkiintoista, että omega-3-PUFA:n vaikutukset näihin signalointireitteihin vaikuttavat todennäköisesti triglyseridien alenemiseen [61] ja lisääntyneeseen ”hyödyllisten adipokiinien, batokiinien” tuotantoon. Niiden tiedetään parantavan metabolista homeostaasia [62]. Lisäksi omega-3 PUFA voi vähentää tumatekijä-kappa B:n (NF-κB) translokaatiota tumaan, mikä vähentää tulehduksellisten sytokiinien tuotantoa [63].
Omega-3 PUFA:n rytmihäiriöitä hillitsevät vaikutukset näyttävät välittyvän sellaisten mekanismien kautta, joihin sisältyy ionikanavan suora ja epäsuora modulointi, solukalvon koostumus ja juoksevuus sekä tulehdusta ja fibroosia estävät vaikutukset [64].
Pitkäaikainen omega-3-PUFA-lisäravinteen saanti aiheuttaa pitkittynyttä eteisrefraktiivisuutta ja vähentää haavoittuvuutta indusoitavalle eteisvärinälle [65]. PUFA:n kulutus voi myös vaikuttaa leposykkeeseen ja sekä systoliseen että diastoliseen verenpaineeseen [66]. Lyhytaikaisissa kokeissa omega-3-PUFA:n saanti lisäsi typpioksidituotantoa, lievitti vasokonstriktiivisia reaktioita noradrenaliinille ja angiotensiini II:lle, tehosti vasodilatoivaa vastetta ja paransi valtimoiden yhteensopivuutta [67–70]. Tällaiset vaikutukset voivat vähentää systeemistä verisuoniresistenssiä ja verenpainetta.

Kertatyydyttämättömät rasvat (MUFA)
Kiistanalaisempia ovat käytettävissä olevat tiedot kertatyydyttämättömien rasvojen sydän- ja verisuonitaudeilta suojaavasta vaikutuksesta, koska julkaistujen tutkimusten määrä on pieni.
Elintarvikkeissa yleisimpiä MUFA-rasvoja ovat oleiinihappo, palmitoleiinihappo ja vakseenihappo. Esimerkiksi oliiviöljyssä on noin 70 prosenttia kertatyydyttymättömiä, 14 prosenttia monityydyttymättömiä ja 11 prosenttia tyydyttyneitä rasvahappoja. Runsas monityydyttymättömien rasvahappojen määrä pitää oliiviöljyn nestemäisenä. Oliiviöljyn tyypillinen rasvahappokoostumus:
- omega 9 -oleiinihappoa 63–83%
- palmitiinihappoa 7–17%
- palmitoleiinihappoa 0,3–3%
- omega 6 -linolihappoa 3,5–14%
- steariinihappoa 0,5–5%
- omega 3 -linoliinihappoa 0,01–1,5%
- myristiinihappoa 0–0,1%
- arakidihappoa 0–0,8%
Tokoferoleja oliiviöljyn painosta on 15–17 prosenttia. Oliiviöljyssä on runsaasti E-vitamiinia sekä esimerkiksi fenoleja, polyfenoleja, fenolihappoa, steroleja, kuten Beeta-sitosteroleja, skvaleenia, beetakaroteenia, terpeenejä, a-klorofylliä ja beetaklorofylliä.
Tuoreen meta-analyysin tulosten perusteella [71] oliiviöljyyn näyttää liittyvän pienempi CVD-riski. Itse asiassa useat muut tutkimukset osoittavat, että ekstra-neitsytoliiviöljy (EVOO) näyttää olevan merkityksellinen tekijä sydän- ja verisuonitapahtumien, kuten sydäninfarktin ja aivohalvauksen, esiintyvyyden vähentämisessä [72, 73].
Vaikka EVOO:n käyttämiä molekyylimekanismeja ei olekaan täysin ymmärretty, EVOO:n terveellistä roolia voidaan viitata sen korkeaan MUFA-tasoon ja useisiin biologisesti aktiivisiin fenoliyhdisteisiin, joilla tiedetään olevan tärkä kardioprotektiivinen rooli [74].
Antosyaanit
Antosyaanit ovat vesiliukoisia flavonoideja ja monia niistä pidetään terveyttä edistävinä. Esimerkiksi mustikassa on paljon antosyaaneja, joista monet ovat antioksidantteja. Antosyaaneita käytetään myös elintarvikkeiden väriaineina, jolloin niiden E-koodi on E 163.
- Syanidiini E-koodi E 163a, oranssinpunainen
- Delfinidiini E-koodi E 163b, violetti tai sininen
- Malvidiini E-koodi E 163c, violetti
- Pelargonidiini E-koodi E 163d, harmaansininen tai sinipunainen
- Peonidiini E-koodi E 163e, harmaansininen/sinipunainen
- Petunidiini E-koodi E 163f, tummanpunainen tai violetti
Antosyaanin varsinaista flavonoidiosaa kutsutaan antosyanidiiniksi. Antosyaani tarkoittaa tarkasti ottaen antosyanidiinin ja sokerin yhdistettä.
Antosyaanit ovat polyfenoliyhdisteitä, jotka ovat vaikuttavat kukkien, marjojen, hedelmien ja vihannesten punaiseen, violettiin ja siniseseen väriin ja joita esiintyy myös punaviinissä. Useat epidemiologiset tutkimukset tukevat sekä antosyaanien että polyfenolien sydäntaudeilta ennaltaehkäisevää vaikutusta [75, 76]. Sydäntaudeilta suojaava vaikutus johtuu antosyaanien sisältämistä fenoleista, polyfenoleista ja antioksidanttiominaisuuksista [77, 78].
Prekliinisiset tutkimukset, kokeellisiset eläinmallit ja in vitro -näyttö, tukevat antosyaanien roolia vaikutusta lipidiprofiiliin, joka on yleisesti käytetty CVD-riskin biomarkkeri. Antosyaanit voivat hidastaa tai estää lipidien ja glukoosin imeytymistä suolistossa ja estää kolesterolisynteesiä, mikä johtaa seerumin triglyseridien, kokonaiskolesterolin ja muun kuin HDL-kolesterolin laskuun ja seerumin HDL-pitoisuuden nousuun [78, 79].
Fenoliyhdisteiden biologinen hyödyntäminen on erittäin heikkoa: vain 10% imeytyy ohutsuolessa, kun taas noin 90% poistuu ulosteen mukana tai metaboloituu suoliston mikrobin kautta [80].
Antosyaanien suojaava vaikutus ei voi johtua ensisijaisesti antioksidanttiominaisuuksista, jotka ovat aktiivisia vain suoliston tasolla (missä fenoliyhdisteiden pitoisuus on korkea), mutta niiden sydäntaudeilta suojaava vaikutus voi selittyä sillä, että antosyaanit vaikuttavat sekundaarisesti solunsisäisinä välittäjinä eri signalointireiteillä.
Muut tutkimukset korostivat antosyaanien kardioprotektiivista ja anti-inflammatorista vaikutusta. Antosyaanien saanti edistää erityisesti typpioksidituotantoa, joka parantaa verenkiertoa ja toisaalta voi estää NF-kB-transkriptiota, mikä vähentää tulehdusta edistävien molekyylien tuotantoa [81].
Zhu et al. korosti antosyaanien anti-inflammatorista vaikutusta satunnaistetussa kontrolloidussa kliinisessä tutkimuksessa (RCT) [82]. Tässä tutkimuksessa yhteensä 150 hyperkolesterolemiaa sairastavaa potilasta sai puhdistettua antosyaaniseosta (320 mg / vrk) tai lumelääkettä kahdesti päivässä 24 viikon ajan.
Antosyaanien kulutus vähensi merkittävästi seerumin C-reaktiivisen proteiinin (−21,6% vs. −2,5%), liukoisen verisuonisolun adheesiomolekyylin 1 (−12,3% vs. 0,4%) ja plasman IL-1β: n (−12,8% vs. −1,3%) verrattuna lumelääkkeeseen. Tutkijat havaitsivat myös merkittävän eron LDL-kolesterolin (−10,4% vs. 0,3%) ja HDL-kolesterolin tason muutoksissa (14,0% vs. −0,9%) kahden ryhmän välillä.
Jos hivenravinteilla on tärkeä rooli CVD-riskin moduloinnissa , on myös hyvin tunnettua, että normaalipainon ylläpitäminen on sydän- ja verisuonitaudeilta suojaava tekijä. Bertoia et al. teki kolme prospektiivista kohorttitutkimusta 124 086 miehellä ja naisella arvioidakseen, liittyikö eräiden flavonoidien alaluokkien saanti painon muutoksiin ajan myötä. Useimpien flavonoidien alaluokkien, mukaan lukien antosyaanit, lisääntynyt kulutus liittyi käänteisesti painon muutokseen 4 vuoden ajanjaksolla. Suurin korrelaatio havaittiin antosyaanien, flavonoidipolymeerien ja flavonolien kohdalla [83]. Siten tässä yhteydessä korkean flavonoidin hedelmien ja vihannesten, kuten omenoiden, päärynöiden, marjojen ja paprikoiden syöminen voi auttaa painonhallinnassa ja CVD: n ehkäisyssä.
Vitamiinit
Useat tutkimukset osoittavat, että E-, C-vitamiinit ja muut antioksidantit voivat vähentää sydän- ja verisuonitautialttiutta neutraloimalla orgaanisia vapaita radikaaleja ja deaktivoimalla virittyneitä happimolekyylejä kudosvaurioiden estämiseksi [84].
Antioksidanteilla voi olla kyky hidastaa tai estää ateroskleroottisten plakkien muodostumista todennäköisesti estämällä LDL-kolesterolin hapettumista [85]. Tiedot C-vitamiinin ja E-vitamiinin roolista sydän- ja verisuonitautien ehkäisyssä ihmisillä tehdyissä tutkimuksissa ovat kuitenkin edelleen kiistanalaisia.
Yhdeksän kohortin koontitutkimuksessa yli 700 mg / vrk C-vitamiinilisän käyttö liittyi vahvasti sepelvaltimotautiriskin 25 prosentin laskuun [86]. Sesso et al. teki kontrolloidun satunnaistetun tutkimuksen 4641 yhdysvaltalaiselle keski-ikäiselle miehelle arvioidakseen, vähentääkö pitkäaikainen (8vuoden seuranta) E-vitamiinin tai C-vitamiinin käyttö merkittävien sydän- ja verisuonitapahtumin riskiä. E- tai C-vitamiinilisät eivät vähentäneet suurten kardiovaskulaaristen tapahtumien riskiä [87].
Ellulu et al. toteutti satunnaistetun kontrolloidun tutkimuksen 64 lihavalla, verenpainetautia ja / tai diabetesta sairastavalla. Tutkimus osoitti, että kahdesti päivässä otettu 500 mg C-vitamiinilisä voi hillitä matala-asteista tulehdusta. C-vitamiini vaikutti terveyteen indusoimalla CRP:n, IL-6: n ja paasto-verensokerin laskua 8 viikon hoidon jälkeen [88].
Tähän mennessä on tehty vain vähän tutkimuksia ruokavalion sisältämien vitamiinien (ei lisäravinteiden) vaikutuksista terveyteen. Suuri kiinalaistutkimus (Zhao et al.) selvitti ruokavalion karoteenin, C-vitamiinin ja E-vitamiinin yhdistelmän vaikutusta kaikista syistä johtuvan kuolleisuuden sekä syöpä- ja CVD- kuolleisuuden riskiin yli 130 000 kiinalaisella aikuisella [89]. Tulokset osoittivat karoteenin ja C-vitamiinin käänteisen yhteyden miesten kuolleisuuteen. Alimpiin kvintiileihin verrattuna vastaava riskin pieneneminen korkeimmassa kvintiilissä oli 17% sekä karoteenilla että C-vitamiinilla.
Vaikka nämä assosiaatiot olivat naisilla heikompia kuin miehillä, tulokset olivat mielenkiintoisia ja tilastollisesti merkittäviä. Toisessa tutkimuksessa arvioitiin 7 vuoden ajan antioksidanttien saantia (E-, C- ja A-vitamiinit) ravinnosta ja lisäravinteista yli 3000 postmenopausaalisella naisella, joilla ei ole sydän- ja verisuonitautia. Tutkimuksen havainnot osoittivat, että E-vitamiinin saanti ravinnosta liittyi käänteisesti kuolemaan johtavan sepelvaltimotaudin riskiin. Sen sijaan A- ja C-vitamiinien saanti ei tutkimuksessa liittynyt pienempiä sydän- ja verisuonitautikuoleman riskiin [90].
Ikä aiheuttaa muutoksia kehon koostumuksessa, aineenvaihduntatekijöissä ja hormonaalisissa tasoissa. Muutokset liittyvät erityisesti fyysisen aktiivisuuden vähenemiseen, mikä lisää kehon rasvamassaa ja vähentää lihasmassaa. Tämä vaikuttaa subkliiniseen tulehdustilaan, jota pidetään yhtenä ateroskleroosin ja CVD:n mekanismeista [1, 2]. Pitkään jatkuva epätasapaino energian saannin ja kulutuksen välillä sekä siihen liittyvä lihavuus on tunnustettu aineenvaihduntasairauksien ja sydän- ja verisuonitautien riskitekijä [91, 92]. Tämä on perinteinen muna vai kana -ongelma. On näyttöä, että ruokavalion ja suoliston mikrobiomin indusoimat hormonaaliset ja metaboliset muutokset altistavat lihomiselle. Lihavuus voi olla oire aineenvaihdunnan ja hormonitasojen häiriintymisestä, eikä niiden syy.

Vähäinen liikunta
Elämäntapa vaikuttaa kroonisten sairauksien kehittymiseen [93, 94]. Liikunta ja fyysinen aktiivisuus voivat parantaa terveyttä ja vähentää sydän- ja verisuonitautien riskiä [95].
Joissain tutkimuksissa on arvioitu päivittäisen istumiseen käytetyn ajan yhteyttä sydän- ja verisuonitautien riskiin. Tiedot perustuvat lähinnä itsearviointiin. Hiljattain julkaistu tutkimus seurasi yli 5000 iäkkään henkilön elintapoja ja osoitti, että istumiseen käytetty aika korreloi positiivisesti lisääntyneen sydän- ja verisuonitautien riskin kanssa [96].
Suuressa tutkimuksessa verrattiin149 077 henkilön fyysistä aktiivisuutta, istumiseen käytettyä aikaa ja sydäntautikuolleisuutta ~9 vvuoden seurannassa. Seurantaan osallistuneista 8689 kuoli seurannan aikana. Näistä 1644 johtui sydän- ja verisuonitaudeista. Tutkimus vahvisti tilastollisesti merkittävän yhteyden vähän liikuntaa sisältävän elämäntavan ja korkeamman sydänkuolleisuusriskin välillä [97 ].
Erilaiset ruokavaliot
Sydän- ja verisuonitautien riskitekijöiden ehkäisemiseksi ja vähentämiseksi on ehdotettu useita ruokavaliotyyppejä vähärasvaisesta ruokavaliosta runsasrasvaiseen ruokavalioon ja kaikkea siltä väliltä.
Kreikkalaisessa lääketieteessä sana dieetti tarkoitti alunperin joukkoa ohjeita, joilla ylläpidetään terveyttä ja hyvinvointia. Näihin ohjeisiin lukeutuivat ohjeet syömisestä ja liikunnasta.
MeDi (välimeren ruokavalio), DASH, vegetaristinen / vegaaninen ruokavalio, ketogeeninen ruokavalio ja japanilainen ruokavalio kuuluvat terapeuttisiin ruokavalioihin, joiden tavoitteena on terveyden ylläpitäminen ja kroonisten aineenvaihduntasairauksien ja niihin liittyvien oireiden ehkäisy [98, 99]. Ruokavaliot painottavat eri ravintoaineiden merkitystä, mutta tavoite on sama: terveys ja painonhallinta. On monta tapaa syödä oikein ja onta tapaa syödä väärin.

Välimeren ruokavalio (MeDi)
Välimeren ruokavalio on useissa vertailuissa arvioitu terveellisimmäksi ruokavalioksi. Tätä on yritetty hyödyntää Itämeren ruokavalion markkinoimisessa ihmisille. Koko idea haisee hapansilakalta.
Välimeren ruokavalion yksi keskeinen terveyttä edistävä tekijä on runsas oliiviöljyn käyttö. Oliiviöljy on luonnollinen, runsaasti hyviä ravinteita sisältävä suurimmaksi osaksi kertatyydyttämättömiä rasvoja sisältävä öljy, joka rinnalla prosessoitu rypsiöljy on traktori-öljyä. Monityydyttämättömät rasvat ovat molekyylirakenteeltaan hyvin epävakaita, minkä vuoksi ne hajoavat kuumennettaessa erilaisiksi aldehydeiksi ja polymerisoituvat herkästi. Itämeren ruokavaliossa voi on hyviäkin ideoita, mutta teollisten koneöljyjen myyminen ihmisille on maatalous- ei terveyspolitiikkaa.
MeDi-ruokavaliolle on ominaista runsas hedelmien, pähkinöiden, vihannesten, täysjyvätuotteiden, oliiviöljyn, kalan ja äyriäisten syöminen. Ravintokuitujen sisältävien täysjyvätuotteiden sekä hedelmien ja vihannesten kulutuksen on raportoitu vähentävän liikalihavuuden, tyypin 2 diabeteksen ja CVD: n riskiä.
Välimeren ruokavalioon sisältyy maltillisesti punaista lihaa ja puhdistettuja sokereita [100]. MeDi laskee sydän- ja verisuonitautialttiutta ja siihen liittyvää kuolleisuutta [101, 102]. Välimeren maissa suosittu ruokavalio on todistetusti hyödyllinen sekä sydän- ja verisuonitautien ensisijaisessa että toissijaisessa ehkäisyssä.
Yksi MeDi:n tärkeimmistä näkökohdista on ruokavalion sisältämien tyydyttymättömien rasvojen korkea pitoisuus, hyvät kuidun ja proteiinin lähteet sekä vähäinen tyydyttyneiden rasvojen saanti. Italialaiset saavat karkeasti puolet päivittäisestä energiasta hiilihydraateista, kolmanneksen kertatyydyttämättömistä rasvoista (oliiviöljy) ja 20 % proteiineista. Ranskalaiset ja sveitsiläiset puolestaan saavat lähes 15 % päivittäisestä energiasta tyydyttyneistä rasvoista (voi, kerma jne.). Koska ranskalaisten ja sveitsiläisten sydänkuolleisuus on pienintä Euroopassa tyydyttyneiden rasvojen saanti ei yksin selitä sydän- ja verisuonitautikuolleisuutta. Välimeren ruokavalioon sisältyy luonnollisia rasvoja ja puhtaita raaka-aineita, mutta ei teollisia koneöljyjä ja paljon raffinoituja elintarvikkeita. Myös Ranskassa suositaan puhtaita raaka-aineita. Se on keskeinen ero. Suomalaisten sydänongelmien taustalla ei ole tyydyttyneet rasvat, vaan teolliset siemenöljyt, jotka eivät kuulu ihmisen ruokavalioon. Ne ovat traktoreiden ravintoa.
Sekä American Heart Association / American College of Cardiology (AHA / ACC) että Euroopan kardiologisen seuran suuntaviivat tukevat voimakkaasti tyydyttyneiden rasvojen korvaamista kerta- ja monityydyttymättömillä rasvoilla [103]. AHA ja ACC ovat kuitenkin yksityisiä yhdistyksiä, jotka rahoittavat toimintansa taloudellisilla lahjoituksilla. Esimerkiksi sokeri- ja maissiteollisuus rahoittavat AHAa. Euroopan kardiologisen seuran rahoittajista en tiedä, mutta vanha viisaus kannattaa muistaa: Kenen leipää syöt, sen lauluja laulat!
MeDi:n positiivisista vaikutuksista osoittavat tiedot on johdettu RCT Lyonin sydäntutkimuksessa, joka osoitti, että CVD-tapahtumat ja kuolemaan johtavat päätetapahtumat vähenivät jopa 4 vuoden ajan niillä koehenkilöillä, jotka satunnaistettiin MeDi-ryhmään [104, 105].
Äskettäin PREvenciòn con Dieta MEDiterànnea -tutkijat osoittivat, että Välimeren ruokavaliota noudattavilla koehenkilöillä oli vähemmän monosyyttejä, tulehdusmarkkereita ja LDL-kolesterolin hapettumiseen liittyvää geeniekspressiota [106].
Oliiviöljyn, kalaöljyn ja pähkinöiden tyydyttymättömien rasvapitoisuuksien sydän- ja verisuonitauteihin liittyvien myönteisten vaikutusten taustalla oleviin mekanismeihin kuuluvat parantuneet lipidiprofiilit, vähentynyt matala-asteinen tulehdus ja alentunut verenpaine [107].
Välimeren ruokavaliolla lisääntynyt hedelmien ja vihannesten saanti on yhdistetty alempaan painoindeksiin ja reaktiivisten happilajien (ROS) tasoon. Niinpä Unesco on tunnustanut MeDin ”ihmiskunnan aineettomaksi kulttuuriperinnöksi” hyvin osoitettujen terveysvaikutusten vuoksi.
Dietary Approaches to Stop Hypertension (DASH) diet
DASH-ruokavalio kehitettiin USA:ssa verenpaineen alentamiseksi ja sydän- ja verisuonitautien ennaltaehkäisemiseksi [103]. DASH suosittelee verenpainetta kohottavan suolan vähentämistä. Ruokavaliossa korostetaan hedelmien, vihannesten, kasviproteiinien, täysjyvätuotteiden, vähärasvaisten maitotuotteiden saantia ja kehotetaan vähentämään tyydyttyneiden rasvojen ja rasvoista saatavan kokonaisenergian määrää.
DASH-ruokavalion edut on tunnustettu yhdysvaltalaisen National Heart, Lung and Blood Institute (NHLBI):n ja Yhdysvaltain maatalousministeriön (USDA) yleisissä ruokavalio-ohjeissa.
Kansainväliset diabeteksen ja kardiovaskulaaristen kliinisten käytäntöjen suuntaviivat ovat myös suosittaneet DASH-ruokavaliota kardiovaskulaaristen riskien vähentämiseksi [108]. Itse asiassa DASH-ruokavalion kontrolloidut satunnaistetut tutkimukset osoittivat LDL-kolesterolin laskevan muiden kardiometabolisten riskitekijöiden ohella. Prospektiiviset kohorttitutkimukset osoittavat, että DASH-ruokavalio laskee diabetekseen ja kardiovaskulaarisiin syihin liittyvää kuolleisuutta [109].
Kasvisruokavalio (Veg Diet)
Kasvisruokavalioille on ominaista eläinperäisen ravinnon kulutuksen minimoiminen tai eläinravinnosta luopuminen. Erilaisia vegetaristisia ruokavalioita on useita, enkä lähde niitä tässä tarkemmin yksilöimään. Osa kasvisruokavalioista sallii kananmunien ja kalan syömisen. Vegaaneja paitsi useimmat vegetaristit sallivat meijerituotteiden syömisen. Mustana hevosena voidaan mainita joustava fleksasaminen (fleksetaarinen ruokavalio), jossa osa ruokavalion lihasta korvataan kasvisvaihtoehdoilla. Se, missä arkisen sekaruokavalion ja fleksaamisen raja kulkee, taitaa olla semantinen ongelma.
Kasvisruokavalio korostaa vihannesten, hedelmien, jyvien, palkokasvien, siementen ja pähkinöiden saantia. Vaikka vegetarismi voidaan määritellä monin tavoin, kasvisruokavalio tarkoittaa yleensä lakto-ovo-kasvisruokavaliota, joka ei sisällä lihaa, siipikarjaa ja kalaa.
Kasvissyönti voi tarkoittaa selvästi rajoittavampaa tai spesifimpiä ruokavaliota, kuten vegaani-ruokavaliota, johon ei kuulu mikään eläinperäinen ravinto, puolikasvissyöjiä (vaihteleva määritelmä) ja kala-kasvissyöjiä (voi syödä kalaa, mutta ei lihaa).
Lihan kulutuksen rajoittamisen oletetaan yleensä laskevan sydän- ja verisuonitautien riskiä [110]. AHA / ACC antoi ravitsemussuosituksia, jotka korostavat runsaasti hedelmiä ja vihanneksia sisältäviä ruokavalioita, ja kehottavat välttämään punaista lihaa ja tyydyttynyttä rasvaa.
Perinteisiä kasvipohjaisia ruokavaliota noudattavilla populaatioilla (Afrikan maaseudulla ja Aasiassa) sydän- ja verisuonitautien riski on vähäinen. Myös perinteistä liha-rasva-maito-sisäelin-ruokavaliota noudattavien Masai-sotureiden sydäntautien riski on käytännössä olematon. Näitä yhdistää puhtaat, luonnolliset ja hyvin vähän jalostetut ravintoaineet, liikkuva elämäntapa ja syöminen silloin kun on nälkä. Itse asiassa eroja länsimaiseen elämäntapaan on niin paljon, että ei niitä ole mielekästä verrata toisiinsa. Esimerkiksi eräät Amazonin alkuperäiskansat eivät syö edes päivittäin, kun meitä länkkäreitä kehotetaan syömään muutaman tunnin välein runsaasti prosessoituja ja helvetisti sokeria sisältäviä ruokia.
Yhdysvalloissa ensimmäinen suuri tutkimus kasvisruokavalion noudattamisesta, tehtiin seitsemännen päivän adventistien keskuudessa, Tutkimus vahvisti annos-vastesuhteen lihan kulutuksen ja sydän- ja verisuonitautien riskin välillä [111].
EPIC-Oxfordin tutkimus osoitti, että kasvissyöjien sydän- ja verisuonitautien riski on 32% pienempi kuin ei-kasvissyöjien riski. Veg-ruokavaliossa on runsaasti fytoravinteita, kuten karotenoideja, lykopeeneja, flavonoideja, antosyaaneja jne., jotka toimivat synergistisesti ja kardioprotektiivisesti matala-asteisen tulehduksen ja oksidatiivisen stressin hillitsemisessä [112].
Veg-ruokavaliolle on tavallista kasviproteiinien sekä raudan, sinkin, jodin, D-vitamiinin ja kalsiumin alhaisempi hyötyosuus ja imeytyminen. Vegaanien kohdalla B12-vitamiinin ainoa lähde on lisäravinnepurkki.
Nämä ovat terveyden ja hyvinvoinnin ylläpitämisen kannalta tärkeitä elinmineraaleja ja vitamiineja. Kasvisruoat sisältävät runsaasti antinutritionaalisia tekijöitä, joita voi esiintyä luonnossa (esim. ruoansulatusentsyymin estäjät, tanniinit, fytaatti, glukosinolaatit ja isotiosyanaatit), jotka muodostuvat prosessoinnin aikana (esim. d-aminohapot, lysinoalaniini) tai johtuen geneettisestä muunnoksesta (esim. lektiinit).
Palkokasvit, viljat, perunat ja tomaatit sisältävät ruoansulatuskanavan proteolyyttisten entsyymien estäjiä. Soijapavut ovat keskittynein trypsiinin estäjien lähde, kun taas herneet ja jalostetut soijapaputuotteet sisältävät trypsiinin estäjiä huomattavasti alhaisempia määriä [113–115].
Ketogeeninen ruokavalio (KD)
Ketogeeninen ruokavalio kehitettiin 1920-luvulla epilepsian kohtausten hallitsemiseksi. Se sisältää runsaasti rasvaa (60–80%) ja proteiinia (10–20%) ja vain hyvin vähän hiilihydraatteja (5–10%). S
Ketogeeninen ruokavalio imitoi aineenvaihdunnan tasolla paastoa. Myönteiset vaikutukset johtuivat enimmäkseen ketonien, kuten β-hydroksibutyraatin, asetoasetaatin ja asetonin tuotannosta maksassa [116].
Ketogeenisen ruokavalion kliiniseen terapiakäyttöön kiinnitettiin enemmän huomiota 1990-luvulla. Nykyään KD on vakiintunut ei-farmakologinen hoito vaikeasti hoidettaville epilepsioille. Tämän lisäksi ketogeenistä ruokavaliota käytetään laajemmin erilaisissa neurologisissa häiriöissä, kuten Alzheimerin ja Parkinsonin tautien terapiana, sekä aineenvaihduntasairauksien, kuten metabolisen oireyhtymän ja diabeteksen hoitona.
Viime aikoina KD:tä on käytetty myös lihavuuden hoitona ja sydän- ja verisuonitautien ehkäisyyn [117]. Ketogeenisen ruokavalion ja sydän- ja verisuonitautien riskitekijöiden ehkäisyä koskevat tutkimukset ovat edelleen kiistanalaisia [118]. Sharman et al. tutkimus osoitti, että aikuisten miesten sopeutuminen tähän ruokavalioon johti merkittävään plasman paasto-triasyyliglyserolien (TAG) vähenemiseen (−33%), aterianjälkeiseen hyperlipidemian laskuun rasvapitoisen aterian jälkeen (−29%) ja paasto-insuliinipitoisuuksien vähenemiseen (−34%).
Ketogeenisellä ruokavaliolla LDL-partikkelikoko kasvoi merkittävästi ilman muutoksia oksidatiivisissa LDL-konsentraatioissa. Kiinnostavaa kyllä, kirjoittajat kuvasivat HDL-kolesterolin merkittävän nousun 3 viikon ketogeenisen ruokavalion jälkeen. Seerumin lipidien, insuliinin ja lipidien alaluokkien vasteet ketogeeniseen ruokavalioon olivat suotuisat yleisen CVD-riskiprofiilin kannalta.
Lisäksi ketogeeninen ruokavalio auttaa painon hallinnassa ja laihduttamisessa erityisesti. Eläinkokeissa on havaittu, että KD lisää eläinten energian kulutusta. Ihmiskokeissa on havaittu, että KD vähentää nälkää ja siten myös energiansaantia.
Painonpudotus johtuu todennäköisesti suuremmasta energiavajeesta, mutta ketoosin metabolisia mekanismeja ei vielä täysin tunneta. Pitkäaikaisia tutkimuksia tarvitaan painonpudotuksen selvittämiseksi ja siihen liittyvien aineenvaihduntamekanismien ymmärtämiseksi.
Maksan rasvapitoisuuden osoitettiin lisääntyneen isoenergeettisen rasvaisen vähähiilihydraattisen ruokavalion aikana. Tämä tapahtuma viittaa siihen, että runsasrasvainen ravinto voi lisätä alkoholittoman rasvamaksa (NAFLD) riskiä, vaikka muut tutkimukset, joissa käytettiin runsaasti hiilihydraatteja sisältävää (”tavanomaista”) hypoenergeettistä ruokavaliota ja hypoenergeettista vähähiilihydraattista ruokavaliota (KD), osoittivat, että maksan rasvapitoisuus väheni merkittävästi ketogeenisen ruokavalion aikana [119–121].
KD:hen liittyy maksan koon ja massan pieneneminen verrattuna tavalliseen hypokaloriseen ruokavalioon. Tämä johtuu todennäköisesti maksan glykogeenien, eli sokerivarastojen tyhjenemisestä.
Rasvamaksan kehittymiseen ketogeenisellä ruokavaliolla vaikuttaa geneettinen alttius henkilöillä, joilla on PNPLA3-geeni [122].
”Alkoholiin liittymätön rasvamaksatauti (NAFLD) lisää maksa- ja sydäntautikuolleisuutta ja on tärkein nopeasti yleistyvän maksasolusyövän syy. NAFLD on yhtä yleinen kuin metabolinen oireyhtymä, ja sitä sairastavien potilaiden joukosta tulisikin löytää ne, joiden fibroosiriski on lisääntynyt ja joilla on kirroosi tai maksasolusyöpä. Noin 40 %:lla suomalaisista on PNPLA3-geenin I148M-variantti ja 15 %:lla TM6SF2-geenin E167K-variantti. Molemmat lisäävät NASH:n ja maksasolusyövän riskiä.” – Duodecim
Tutkittavilla, joilla oli PNPLA3-muunnelmia, maksan rasvapitoisuus oli matalampi kuin verrokkeilla, kun he noudattivat ketogeenistä ruokavaliota [123]. KD:n ongelmana pidetään usein kuitujen saannin vähäisyyttä. Joskus, mutta nykyisin varsin harvoin, esiin nostetaan tyydyttyneiden rasvojen potentiaaliset riskit. Se puolestaan on taistelu tuulimyllyjä vastaan; ketogeenistä ruokavaliota noudattavien lipidiprofiilit, verenpaine, verensokeri ja sydänterveys näyttävät olevan paremmalla tasolla kuin monilla vähemmän rasvaa syövillä. Kuitujen vähäisen saannin vaikutuksista ei ole saatavilla tietoja, joten tarvitaan muita pitkittäistutkimuksia, jotta kaikki tämäntyyppiseen ravitsemustapaan liittyvät kysymykset voidaan luonnehtia pitkällä aikavälillä.
Japanilainen ruokavalio
Japanilainen ruokavalio sisältää laajan valikoiman puhtaista ja tuoreista raaka-aineista valmistettuja ruokia, kuten papuja, tofua, tuoretta kalaa, vihanneksia, japanilaisia suolakurkkua, sieniä, merilevää ja hedelmiä [124]. Vaikka ruokavalio eroaa länsimaisista ruokavalioista, japanilaisella ruokavaliolla on samanlaisia ominaisuuksia kuin Välimeren ruokavaliolla.
Aikaisemmin julkaistut tutkimukset osoittivat, että yksittäisten ruokaryhmien, kuten hedelmien, vihannesten, papujen ja kalojen, saanti liittyi käänteisesti sydän- ja verisuonitautikuolleisuuteen ja kuolleisuuteen kaikkiin syihin Japanissa [125, 126].
Japanilaiselle ruokavaliolle on ominaista runsas natriumin saanti ja matala kaliumin saanti, mikä osaltaan lisää korkeaa natrium / kalium (Na – K) -suhdetta, mikä voi olla vahva indikaattori sydän- ja verisuonitautien kuolleisuuden riskille [127].
Tutkimukset osoittavat, että Na – K-suhde assosioituu positiivisesti aivoverenvuotoon liittyvään aivohalvaukseen, mutta ei tilastollisesti merkittävästi iskeemisen aivohalvauksen riskiin.
Japanilainen ruokavalio sisältää runsaasti happamoitettuja (fermentoituja) ruokia, kuten kalaa ja juustoa, mutta vähän emäksisiä elintarvikkeita, kuten hedelmiä ja vihanneksia, jotka voivat johtaa endogeenisen hapon tuotantoon [128].
Ruokavalion korkea happokuormitus on yhdistetty kardiometabolisten riskitekijöiden, kuten insuliiniresistenssin [129], korkean verenpaineen tai verenpainetaudin [130, 131], suuren vyötärön ympärysmitan, korkeiden triglyseridien ja LDL-kolesterolin sekä tyypin 2 diabeteksen [132] riskeihin133].
Mutta vastoin odotuksia viimeaikaiset tutkimukset ovat osoittaneet, että japanilainen ruokavalio voi vähentää kuolleisuutta sekä syöpään että sydän- ja verisuonitauteihin [134, 135], mikä viittaa potentiaaliseen vaihtoehtoiseen kardiometaboliset riskit arvioivaan ravitsemukselliseen malliin.
Lopuksi
Sydän- ja verisuonitaudit ovat monitekijäisiä, epäterveellisiin elintapoihin ja huonoihin ravitsemustottumuksiin liittyvä sairaus. Monet tutkimukset viittaavat siihen, että liiallinen natriumin ja prosessoitujen elintarvikkeiden saanti, lisätyt sokerit, epäterveelliset rasvat, vähäinen hedelmien ja vihannesten, täysjyvätuotteiden, kuidun, palkokasvien, kalan ja pähkinöiden saanti, alkoholin runsas kulutus, stressi, tupakointi ja liikunnan puute lisäävät sydän- ja verisuonitautien riskiä.
Tässä katsauksessa analysoitavien erityyppisten ruokavalioiden joukossa MeDi näyttää olevan paras ravitsemuksellinen malli, koska se sisältää täysjyvätuotteita, palkokasveja, kuituja, kerta- ja monityydyttämättömiä rasvoja sulkematta kokonaan pois eläinperäisiä elintarvikkeita, kuten lihaa, kalaa, maitotuotteita, munia, ja rajoittamatta alkoholinkulutusta.
Lisäksi MeDi-elämäntavassa otetaan huomioon paitsi elintarvikkeet, myös mielialat ja fyysinen aktiivisuus, mikä tarkoittaa tiettyä elämäntapaa, joka ei rajoitu ruokaan. Useat tutkimukset osoittavat, että MeDiä noudattavilla koehenkilöillä on pienempi lihavuuden ja tyypin 2 diabeteksen riski, sekä LDL-kolesterolin hapettumiseen liittyvän geeniekspression hyödyllinen modulointi [106].
Kiinnostavista keskusteluista ja pienistä tutkimuksista huolimatta muista analysoiduista ruokavalioista ei vielä ole riittävästi tutkimustietoja ja näyttö, jotta niitä voitaisiin pitää parempina ruokavalioina kuin MeDi sydän- ja verisuonitautien ehkäisyssä.
Pahoittelen, jos tekstiin jäi kirjoitus- tai käännösvirheitä. Korjaan niitä hiljalleen. Artikkelin tavoite ei ole pahoittaa kenenkään mieltä. Toin esiin tutkimusten tukemia näkökulmia ja omia näkökulmia.
Lähteet
1. Garcia-Arellano A, Martínez-González MA, Ramallal R, Salas-Salvadó J, Hébert JR, Corella D, et al. Dietary inflammatory index and all-cause mortality in large cohorts: the SUN and PREDIMED studies. Clin Nutr. 2019;38:1221–31. [PubMed] [Google Scholar]
2. LaCroix AZ, Bellettiere J, Rillamas-Sun E, Di C, Evenson KR, Lewis CE, et al. Association of light physical activity measured by accelerometry and incidence of coronary heart disease and cardiovascular disease in older women. JAMA Netw Open. 2019;2:e190419. [PMC free article] [PubMed] [Google Scholar]
3. Vincent L, Leedy D, Masri SC, Cheng RK. Cardiovascular disease and cancer: is there increasing overlap? Curr Oncol Rep. 2019;21:47. [PubMed] [Google Scholar]
4. Doughty KN, Del Pilar NX, Audette A, Katz DL. Lifestyle medicine and the management of cardiovascular disease. Curr Cardiol Rep. 2017;19:116. [PubMed] [Google Scholar]
5. Konstantinidou V, Daimiel L, Ordovás JM. Personalized nutrition and cardiovascular disease prevention: from Framingham to PREDIMED. Adv Nutr. 2014;5:368S–71S. [PMC free article] [PubMed] [Google Scholar]
6. Lanier JB, Bury DC, Richardson SW. Diet and physical activity for cardiovascular disease prevention. Am Fam Physician. 2016;93:919–24. [PubMed] [Google Scholar]
7. Heilbronn LK, Ravussin E. Calorie restriction and aging: review of the literature and implications for studies in humans. Am J Clin Nutr. 2003;78:361–9. [PubMed] [Google Scholar]
8. Velthuis-te Wierik EJ, van den Berg H, Schaafsma G, Hendriks HF, Brouwer A. Energy restriction, a useful intervention to retard human ageing? Results of a feasibility study. Eur J Clin Nutr. 1994;48:138–48. [PubMed] [Google Scholar]
9. Loft S, Velthuis-te Wierik EJ, van den Berg H, Poulsen HE. Energy restriction and oxidative DNA damage in humans. Cancer epidemiology, biomarkers & prevention: a publication of the American Association for Cancer Research, cosponsored by the American Society of Preventive. Oncology. 1995;4:515–9. [PubMed] [Google Scholar]
10. Verdery RB, Walford RL. Changes in plasma lipids and lipoproteins in humans during a 2-year period of dietary restriction in Biosphere 2. Arch Intern Med. 1998;158:900–6. [PubMed] [Google Scholar]
11. Walford RL, Harris SB, Gunion MW. The calorically restricted low-fat nutrient-dense diet in Biosphere 2 significantly lowers blood glucose, total leukocyte count, cholesterol, and blood pressure in humans. Proc Natl Acad Sci USA. 1992;89:11533–7. [PMC free article] [PubMed] [Google Scholar]
12. Walford RL, Mock D, Verdery R, MacCallum T. Calorie restriction in biosphere 2: alterations in physiologic, hematologic, hormonal, and biochemical parameters in humans restricted for a 2-year period. J Gerontol Ser A Biol Sci Med Sci. 2002;57:B211–224. [PubMed] [Google Scholar]
13. Lefevre M, Redman LM, Heilbronn LK, Smith JV, Martin CK, Rood JC, et al. Caloric restriction alone and with exercise improves CVD risk in healthy non-obese individuals. Atherosclerosis. 2009;203:206–13. [PMC free article] [PubMed] [Google Scholar]
14. Robertson TL, Kato H, Rhoads GG, Kagan A, Marmot M, Syme SL, et al. Epidemiologic studies of coronary heart disease and stroke in Japanese men living in Japan, Hawaii and California. Incidence of myocardial infarction and death from coronary heart disease. Am J Cardiol. 1977;39:239–43. [PubMed] [Google Scholar]
15. Nuno DM, Lamping KG. Dietary fatty acid saturation modulates sphingosine-1-phosphate-mediated vascular function. J Diabetes Res. 2019;2019:1–11. [PMC free article] [PubMed] [Google Scholar]
16. Moreira APB, Texeira TFS, Ferreira A. Influence of a high-fat diet on gut microbiota, intestinal permeability and metabolic endotoxaemia. Br J Nutr. 2012;108:801–9. [PubMed] [Google Scholar]
17. Clifton PM, Keogh JB. A systematic review of the effect of dietary saturated and polyunsaturated fat on heart disease. Nutr Metab Cardiovasc Dis. 2017;27:1060–80. [PubMed] [Google Scholar]
18. Lee JY, Zhao L, Youn HS, Weatherill AR, Tapping R, Feng L, et al. Saturated fatty acid activates but polyunsaturated fatty acid inhibits toll-like receptor 2 dimerized with toll-like receptor 6 or 1. J Biol Chem. 2004;279:16971–9. [PubMed] [Google Scholar]
19. Wong SW, Kwon M, Choi AMK, Kim H, Nakahira K, Hwang DH. Fatty acids modulate toll-like receptor 4 activation through regulation of receptor dimerization and recruitment into lipid rafts in a reactive oxygen species-dependent manner. J Biol Chem. 2009;284:27384–92. [PMC free article] [PubMed] [Google Scholar]
20. Gault C, Obeid L, Hannun Y. An overview of sphingolipid metabolism: from synthesis to breakdown. Adv Exp Med Biol. 2010;688:1–23. [PMC free article] [PubMed] [Google Scholar]
21. Keys A, Menotti A, Karvonen MJ, Aravanis C, Blackburn H, Buzina R, et al. The diet and 15-year death rate in the seven countries study. Am J Epidemiol. 1986;124:903–15. [PubMed] [Google Scholar]
22. Julibert A, Bibiloni MDM, Tur JA. Dietary fat intake and metabolic syndrome in adults: a systematic review. Nutr Metab Cardiovasc Dis. 2019;29:887–905. [PubMed] [Google Scholar]
23. Skop-Lewandowska A, Zając J, Kolarzyk E. Overweight and obesity vs. simple carbohydrates consumption by elderly people suffering from diseases of the cardiovascular system. Ann Agric Environ Med. 2017;24:575–80. [PubMed] [Google Scholar]
24. Miller M, Stone N, Ballantyne C, Bittner V, Criqui M, Ginsberg H, et al. Triglycerides and cardiovascular disease: a scientific statement from the American Heart Association. Circulation. 2011;123:2292–333. [PubMed] [Google Scholar]
25. Rippe JM, Angelopoulos TJ. Added sugars and risk factors for obesity, diabetes and heart disease. Int J Obesity. 2016;40:S22–7. [PubMed] [Google Scholar]
26. Obarzanek E, Sacks F, Vollmer W, Bray G, Miller E, III, Lin P, et al. DASH Research Group. Effects on blood lipids of a blood pressure-lowering diet: the Dietary Approaches to Stop Hypertension (DASH) Trial. Am J Clin Nutr. 2001;74:80–9. [PubMed] [Google Scholar]
27. Howard B, Van Horn L, Hsia J, Manson J, Stefanick M, Wassertheil-Smoller S, et al. Low-fat dietary pattern and risk of cardiovascular disease: the Women’s Health Initiative Randomized Controlled Dietary Modification Trial. JAMA. 2006;295:655–66. [PubMed] [Google Scholar]
28. Hellerstein MK, Schwarz JM, Neese RA. Regulation of hepatic de novo lipogenesis in humans. Ann Rev Nutr. 1996;16:523–57. [PubMed] [Google Scholar]
29. Stanhope KL, Schwarz JM, Keim NL, Griffen SC, Bremer AA, Graham JL, et al. Consuming fructose-sweetened, not glucose-sweetened, beverages increases visceral adiposity and lipids and decreases insulin sensitivity in overweight/obese humans. J Clin Investig. 2009;119:1322–34. [PMC free article] [PubMed] [Google Scholar]
30. Ha V, Sievenpiper J, de Souza R, Chiavaroli L, Wang D, Cozma A, et al. Effect of fructose on blood pressure: a systematic review and meta-analysis of controlled feeding trials. Hypertension. 2012;59:787–95. [PubMed] [Google Scholar]
31. Jones JR, Lineback DM, Levine MJ. Dietary reference intakes: implications for fiber labeling and consumption: a summary of the International Life Sciences Institute North America Fiber Workshop, June 1–2, 2004, Washington, DC. Nutr Rev. 2006;64:31–8. [PubMed] [Google Scholar]
32. Lia A, Hallmans G, Sandberg AS, Sundberg B, Aman P, Andersson H. Oat beta-glucan increases bile acid excretion and a fiber-rich barley fraction increases cholesterol excretion in ileostomy subjects. Am J Clin Nutr. 1995;62:1245–51. [PubMed] [Google Scholar]
33. Brown L, Rosner B, Willett WW, Sacks FM. Cholesterol-lowering effects of dietary fiber: a meta-analysis. Am J Clin Nutr. 1999;69:30–42. [PubMed] [Google Scholar]
34. Chen JP, Chen GC, Wang XP, Qin L, Bai Y. Dietary fiber and metabolic syndrome: a meta-analysis and review of related mechanisms. Nutrients. 2018;10:24. [PMC free article] [PubMed] [Google Scholar]
35. Soliman GA. Dietary fiber, atherosclerosis, and cardiovascular disease. Nutrients. 2019;11:1155. [PMC free article] [PubMed] [Google Scholar]
36. Kim Y, Je Y. Dietary fiber intake and total mortality: a meta-analysis of prospective cohort studies. Am J Epidemiol. 2014;180:565–73. [PubMed] [Google Scholar]
37. Kim Y, Je Y. Dietary fibre intake and mortality from cardiovascular disease and all cancers: a meta-analysis of prospective cohort studies. Arch Cardiovasc Dis. 2016;109:39–54. [PubMed] [Google Scholar]
38. GBD 2013 Mortality and Causes of Death Collaborators. Global, regional, and national age-sex specific all-cause and cause-specific mortality for 240 causes of death, 1990–2013: a systematic analysis for the Global Burden of Disease Study 2013. Lancet. 2015;385:117–71. [PMC free article] [PubMed] [Google Scholar]
39. Bohn SK, Myhrstad MC, Thoresen M, Holden M, Karlsen A, Tunheim SH, et al. Blood cell gene expression associated with cellular stress defense is modulated by antioxidant-rich food in a randomised controlled clinical trial of male smokers. BMC Med. 2010;8:54. [PMC free article] [PubMed] [Google Scholar]
40. Anderson JW, Baird P, Davis RH, Jr, Ferreri S, Knudtson M, Koraym A, et al. Health benefits of dietary fibre. Nutr Rev. 2009;67:188–205. [PubMed] [Google Scholar]
41. Alissa EM, Ferns GA. Dietary fruits and vegetables and cardiovascular diseases risk. Crit Rev Food Sci Nutr. 2017;57:1950–62. [PubMed] [Google Scholar]
42. Aune D, Giovannucci E, Boffetta P, Fadnes LT, Keum N, Norat T, et al. Fruit and vegetable intake and the risk of cardiovascular disease, total cancer and all-cause mortality-a systematic review and dose-response meta-analysis of prospective studies. Int J Epidemiol. 2017;46:1029–56. [PMC free article] [PubMed] [Google Scholar]
43. Sánchez-Muniz FJ. Dietary fibre and cardiovascular health. Nutr Hosp. 2012;27:31–45. [PubMed] [Google Scholar]
44. Huang T, Xu M, Lee A, Cho S, Qi L. Consumption of whole grains and cereal fiber and total and cause-specific mortality: Prospective analysis of 367,442 individuals. BMC Med. 2015;13:59. [PMC free article] [PubMed] [Google Scholar]
45. Casas R, Castro-Barquero S, Estruch R, Sacanella E. Nutrition and Cardiovascular Health. Int J Mol Sci. 2018;19:3988. [Google Scholar]
46. Korcz E, Kerényi Z, Varga L. Dietary fibers, prebiotics, and exopolysaccharides produced by lactic acid bacteria: potential health benefits with special regard to cholesterol-lowering effects. Food Funct. 2018;9:3057–68. [PubMed] [Google Scholar]
47. McKeown NM, Meigs JB, Liu S, Saltzman E, Wilson PW, Jacques PF. Carbohydrate nutrition, insulin resistance, and the prevalence of the metabolic syndrome in the Framingham Offspring Cohort. Diabetes Care. 2004;27:538–46. [PubMed] [Google Scholar]
48. Liu S, Buring JE, Sesso HD, Rimm EB, Willett WC, Manson JE. A prospective study of dietary fiber intake and risk of cardiovascular disease among women. J Am Coll Cardiol. 2002;39:49–56. [PubMed] [Google Scholar]
49. Marques FZ, Nelson E, Chu PY, Horlock D, Fiedler A, Ziemann M, et al. High-fiber diet and acetate supplementation change the gut microbiota and prevent the development of hypertension and heart failure in hypertensive mice. Circulation. 2017;135:964–77. [PubMed] [Google Scholar]
50. Surampudi P, Enkhmaa B, Anuurad E, Berglund L. Lipid lowering with soluble dietary fiber. Curr Atheroscler Rep. 2016;18:75. [PubMed] [Google Scholar]
51. Ripsin CM, Keenan JM, Jacobs DR, Jr, Elmer PJ, Welch RR, Van Horn L, et al. Oat products and lipid lowering. A meta-analysis. JAMA. 1992;267:3317–25. [PubMed] [Google Scholar]
52. Ho HV, Sievenpiper JL, Zurbau A, Blanco Mejia S, Jovanovski E, Au-Yeung F, Jenkins AL, Vuksan V. The effect of oat β-glucan on LDL-cholesterol, non-HDL-cholesterol and apoB for CVD risk reduction: a systematic review and meta-analysis of randomised-controlled trials. Br J Nutr. 2016;116:1369–82. [PubMed] [Google Scholar]
53. Othman RA, Moghadasian MH, Jones PJ. Cholesterol-lowering effects of oat beta-glucan. Nutr Rev. 2011;69:299–309. [PubMed] [Google Scholar]
54. Whitehead A, Beck EJ, Tosh S, Wolever TM. Cholesterol lowering effects of oat beta-glucan: a meta-analysis of randomized controlled trials. Am J Clin Nutr. 2014;100:1413–21. [PMC free article] [PubMed] [Google Scholar]
55. Mirmiran P, Bahadoran Z, Khalili Moghadam S, Zadeh Vakili A, Azizi F. A prospective study of different types of dietary fiber and risk of cardiovascular disease: Tehran Lipid and Glucose Study. Nutrients. 2016;8:686. [PMC free article] [PubMed] [Google Scholar]
56. Yang T, Santisteban MM, Rodriguez V, Li E, Ahmari N, Carvajal JM, et al. Gut dysbiosis is linked to hypertension. Hypertension. 2015;65:1331–40. [PMC free article] [PubMed] [Google Scholar]
57. Mizia-Stec K, Haberka M, Mizia M, Chmiel A, Gieszczyk K, Lasota B, et al. N-3 Polyunsaturated fatty acid therapy improves endothelial function and affects adiponectin and resistin balance in the first month after myocardial infarction. Arch Med Sci. 2011;7:788–95. [PMC free article] [PubMed] [Google Scholar]
58. Tribulova N, Szeiffova Bacova B, Egan Benova T, Knezl V, Barancik M, Slezak J. Omega-3 index and anti-arrhythmic potential of omega-3 PUFAs. Nutrients. 2017;9:1191. [Google Scholar]
59. Adkins Y, Kelley DS. Mechanisms underlying the cardioprotective effects of omega-3 polyunsaturated fatty acids. J Nutr Biochem. 2010;21:781–92. [PubMed] [Google Scholar]
60. Schroeder F, Petrescu AD, Huang H. Role of fatty acid binding proteins and long chain fatty acids in modulating nuclear receptors and gene transcription. Lipids. 2008;43:1–17. [PubMed] [Google Scholar]
61. Sheena V, Hertz R, Nousbeck J, Berman I, Magenheim J, Bar-Tana J. Transcriptional regulation of human microsomal triglyceride transfer protein by hepatocyte nuclear factor-4alpha. J Lipid Res. 2005;46:328–41. [PubMed] [Google Scholar]
62. Lee MW, Lee M, Oh KJ. Adipose tissue-derived signatures for obesity and type 2 diabetes: adipokines, batokines and microRNAs. J Clin Med. 2019;8:854. [PMC free article] [PubMed] [Google Scholar]
63. Li H, Ruan XZ, Powis SH. EPA and DHA reduce LPSinduced inflammation responses in HK-2 cells: evidence for a PPAR-gamma-dependent mechanism. Kidney Int. 2005;67:867–74. [PubMed] [Google Scholar]
64. Nodari S, Triggiani M, Campia U, Dei Cas L. Omega-3 polyunsaturated fatty acid supplementation: mechanism and current evidence in atrial fibrillation. J. Atr. Fibrillation. 2012;5:718. [PMC free article] [PubMed] [Google Scholar]
65. Den Ruijter HM, Verkerk AO, Coronel R. Incorporated fish oil fatty acids prevent action potential shortening induced by circulating fish oil fatty acids. Front. Physiol. 2010;1:1–5. [PMC free article] [PubMed] [Google Scholar]
66. Mozaffarian D, Wu JH. Omega-3 fatty acids and cardiovascular disease: effects on risk factors, molecular pathways, and clinical events. J Am Coll Cardiol. 2011;58:2047–67. [PubMed] [Google Scholar]
67. Dangardt F, Osika W, Chen Y. Omega-3 fatty acid supplementation improves vascular function and reduces inflammation in obese adolescents. Atherosclerosis. 2010;212:580–5. [PubMed] [Google Scholar]
68. Rizza S, Tesauro M, Cardillo C. Fish oil supplementation improves endothelial function in normoglycemic offspring of patients with type 2 diabetes. Atherosclerosis. 2009;206:569–74. [PMC free article] [PubMed] [Google Scholar]
69. Goodfellow J, Bellamy MF, Ramsey MW, Jones CJ, Lewis MJ. Dietary supplementation with marine omega-3 fatty acids improve systemic large artery endothelial function in subjects with hypercholesterolemia. J Am Coll Cardiol. 2000;35:265–70. [PubMed] [Google Scholar]
70. Mori TA, Watts GF, Burke V, Hilme E, Puddey IB, Beilin LJ. Differential effects of eicosapentaenoic acid and docosahexaenoic acid on vascular reactivity of the forearm microcirculation in hyperlipidemic, overweight men. Circulation. 2000;102:1264–9. [PubMed] [Google Scholar]
71. Schwingshackl L, Hoffmann G. Monounsaturated fatty acids, olive oil and health status: a systematic review and meta-analysis of cohort studies. Lipids Health Dis. 2014;13:154. [PMC free article] [PubMed] [Google Scholar]
72. Guasch-Ferré M, Hu FB, Martínez-González MA, Fitó M, Bulló M, Estruch R. Olive oil intake and risk of cardiovascular disease and mortality in the PREDIMED study. BMC Med. 2014;12:78. [PMC free article] [PubMed] [Google Scholar]
73. Violi F, Loffredo L, Pignatelli P, Angelico F, Bartimoccia S, Nocella C, et al. Extra virgin olive oil use is associated with improved post-prandial blood glucose and LDL cholesterol in healthy subjects. Nutr Diabetes. 2015;5:e172. [PMC free article] [PubMed] [Google Scholar]
74. Tripoli E, Giammanco M, Tabacchi G, Di Majo D, Giammanco S, Laguardia M. The phenolic compounds of olive oil: structure, biological activity and beneficial effects on human health. Nutr Res Rev. 2005;18:98–112. [PubMed] [Google Scholar]
75. Jennings A, Welch AA, Fairweather-Tait SJ, Kay C, Minihane A-M. Higher anthocyanin intake is associated with lower arterial stiffness and central blood pressure in women. Am J Clin Nutr. 2012;96:781–8. [PubMed] [Google Scholar]
76. Du G, Sun L, Zhao R, Du L, Song J, He G, et al. Polyphenols: potential source of drugs for the treatment of ischaemic heart disease. Pharmacol Ther. 2016;162:23–34. [PubMed] [Google Scholar]
77. Qin Y, Xia M, Ma J, Hao Y, Liu J. Anthocyanin supplementation improves serum LDL-and HDL-cholesterol concentrations associated with the inhibition of cholesteryl ester transfer protein in dyslipidemic subjects. Am J Clin Nutr. 2009;90:485–92. [PubMed] [Google Scholar]
78. Wallace T, Slavin M, Frankenfeld C. Systematic review of anthocyanins and markers of cardiovascular disease. Nutrients. 2016;8:32. [PMC free article] [PubMed] [Google Scholar]
79. Rizzi F, Conti C, Dogliotti E, Terranegra A, Salvi E, Braga D, et al. Interaction between polyphenols intake and PON1 gene variants on markers of cardiovascular disease: a nutrigenetic observational study. J Transl Med. 2016;14:186. [PMC free article] [PubMed] [Google Scholar]
80. Kawabata K, Yoshioka Y, Terao J. Role of intestinal microbiota in the bioavailability and physiological functions of dietary polyphenols. Molecules. 2019;24:370. [PMC free article] [PubMed] [Google Scholar]
81. Kruger M, Davies N, Myburgh K, Lecour S. Proanthocyanidins, anthocyanins and cardiovascular diseases. Food Res Int. 2014;59:42–52. [Google Scholar]
82. Zhu Y, Ling W, Guo H, Song F, Ye Q, Zou T, et al. Anti-inflammatory effect of purified dietary anthocyanin in adults with hypercholesterolemia: a randomized controlled trial. Nutr Metab Cardiovasc Dis. 2013;23:843–9. [PubMed] [Google Scholar]
83. Bertoia ML, Rimm EB, Mukamal KJ, Hu FB, Willett WC, Cassidy A. Dietary flavonoid intake and weight maintenance: three prospective cohorts of 124086 US men and women followed for up to 24 years. BMJ. 2016;352:i17. [PMC free article] [PubMed] [Google Scholar]
84. Packer L. Protective role of vitamin E in biological systems. Am J Clin Nutr. 1991;53(4 Suppl):1050S–1055S. [PubMed] [Google Scholar]
85. Steinberg D. Lewis A. Conner Memorial Lecture. Oxidative modification of LDL and atherogenesis. Circulation. 1997;95:1062–71. [PubMed] [Google Scholar]
86. Knekt P, Ritz J, Pereira MA, O’Reilly EJ, Augustsson K, Fraser GE, et al. Antioxidant vitamins and coronary heart disease risk: a pooled analysis of 9 cohorts. Am J Clin Nutr. 2004;80:1508–20. [PubMed] [Google Scholar]
87. Sesso HD, Buring JE, Christen WG, Kurth T, Belanger C, MacFadyen J, et al. Vitamins E and C in the prevention of cardiovascular disease in men: the Physicians’ Health Study II randomized controlled trial. JAMA. 2008;300:2123–33. [PMC free article] [PubMed] [Google Scholar]
88. Ellulu MS, Rahmat A, Patimah I, Khaza’ai H, Abed Y. Effect of vitamin C on inflammation and metabolic markers in hypertensive and/or diabetic obese adults: a randomized controlled trial. Drug Des Dev Ther. 2015;9:3405–12. [PMC free article] [PubMed] [Google Scholar]
89. Long-Gang Zhao, Xiao-Ou Shu, Hong-Lan Li, Wei Zhang, Jing Gao, Sun JW, et al. Dietary antioxidant vitamins intake and mortality: a report from two cohort studies of Chinese adults in Shanghai. J Epidemiol. 2017;27:89–97. [PMC free article] [PubMed] [Google Scholar]
90. Kushi LH, Folsom AR, Prineas RJ, Mink PJ, Wu Y, Bostick RM. Dietary antioxidant vitamins and death from coronary heart disease in postmenopausal women. N Engl J Med. 1996;334:1156–62. [PubMed] [Google Scholar]
91. Bray GA, Heisel WE, Afshin A, Jensen MD, Dietz WH, Long M, et al. The science of obesity management: an Endocrine Society Scientific Statement. Endocr Rev. 2018;39:79–132. [PMC free article] [PubMed] [Google Scholar]
92. KK Ryan, Woods SC, Seeley RJ. Central nervous system mechanisms linking the consumption of palatable high-fat diets to the defense of greater adiposity. Cell Metab. 2012;15:137–49. [PMC free article] [PubMed] [Google Scholar]
93. Nystoriak MA, Bhatnagar A. Cardiovascular effects and benefits of exercise. Front Cardiovasc Med. 2018;5:135. [PMC free article] [PubMed] [Google Scholar]
94. Schmitt A, Maurus I, Rossner MJ, Röh A, Lembeck M, von Wilmsdorff M, et al. Effects of aerobic exercise on metabolic syndrome, cardiorespiratory fitness, and symptoms in schizophrenia include decreased mortality. Front Psychiatry. 2018;9:690. [PMC free article] [PubMed] [Google Scholar]
95. Adams V, Linke A. Impact of exercise training on cardiovascular disease and risk. Biochim Biophys Acta Mol Basis Dis. 2019;1865:728–34. [PubMed] [Google Scholar]
96. Bellettiere J, LaMonte MJ, Evenson KR, Rillamas-Sun E, Kerr J, Lee IM, et al. Sedentary behavior and cardiovascular disease in older women: the Objective Physical Activity and Cardiovascular Health (OPACH) Study. Circulation. 2019;139:1036–46. [PMC free article] [PubMed] [Google Scholar]
97. Stamatakis E, Gale J, Bauman A, Ekelund U, Hamer M, Ding D. Sitting time, physical activity, and risk of mortality in adults. J Am Coll Cardiol. 2019;73:2062–72. [PubMed] [Google Scholar]
98. US department of Health and Human services. Dietary Guidliness for Americans, Washington, DC; US Government Printing Office; 2005.
99. Trichopoulou A, Costacou T, Bamia C, Trichopoulos D. Adherence to a mediterranean diet and survival in a Greek Population. N Eng J Med. 2003;348:2599–608. [PubMed] [Google Scholar]
100. Åkesson A. Go nuts and go extra virgin olive oil! Mediterranean diets reduce blood pressure. Hypertension. 2014;64:26–7. [PubMed] [Google Scholar]
101. Mozaffarian D, Appel LJ, Van Horn L. Components of a cardioprotective diet: New insights. Circulation. 2011;123:2870–91. [PMC free article] [PubMed] [Google Scholar]
102. Sacks FM, Campos H. Dietary therapy in hypertension. N Engl J Med. 2010;362:2102–12. [PubMed] [Google Scholar]
103. Lichtenstein AH, Appel LJ, Brands M, Carnethon M, Daniels S, Franch HA, et al. American Heart Association Nutrition Committee. Diet and lifestyle recommendations revision 2006: a scientific statement from the American Heart Association Nutrition Committee. Circulation. 2006;114:82–96. [PubMed] [Google Scholar]
104. Graham I, Atar D, Borch-Johnsen K, Boysen G, Burell G, Cifkova R, et al. European Society of Cardiology (ESC) Committee for Practice Guidelines (CPG). European guidelines on cardiovascular disease prevention in clinical practice: executive summary: Fourth Joint Task Force of the European Society of Cardiology and Other Societies on Cardiovascular Disease Prevention in Clinical Practice (Constituted by representatives of nine societies and by invited experts) Eur Heart J. 2007;28:2375–414. [PubMed] [Google Scholar]
105. Estruch R, Ros E, Salas-Salvadó J, Covas MI, Corella D, Arós F, et al. Primary prevention of cardiovascular disease with a Mediterranean diet. N Engl J Med. 2013;368:1279–90. [PubMed] [Google Scholar]
106. Salas-Salvadó J, Bulló M, Babio N, Martínez-González MÁ, Ibarrola-Jurado N, Basora J, et al. PREDIMED Study Investigators. Reduction in the incidence of type 2 diabetes with the Mediterranean diet: results of the PREDIMED-Reus nutrition intervention randomized trial. Diabetes Care. 2011;34:14–9. [PMC free article] [PubMed] [Google Scholar]
107. Razquin C, Martinez-Gonzalez MA. A traditional mediterranean diet effectively reduces inflammation and improves cardiovascular health. Nutrients. 2019;11:1842. [PMC free article] [PubMed] [Google Scholar]
108. Siervo M, Lara J, Chowdhury S, Ashor A, Oggioni C, Mathers JC. Effects of the Dietary Approach to Stop Hypertension (DASH) diet on cardiovascular risk factors: a systematic review and meta-analysis. Br J Nutr. 2015;113:1–15. [PubMed] [Google Scholar]
109. Schwingshackl L, Hoffmann G. Diet quality as assessed by the Healthy Eating Index, the Alternate Healthy Eating Index, the Dietary Approaches to Stop Hypertension score, and health outcomes: a systematic review and meta-analysis of cohort studies. J Acad Nutr Diet. 2015;115:780–800. [PubMed] [Google Scholar]
110. Anderson TJ, Gregoire J, Pearson GJ, Barry AR, Couture P, Dawes M, et al. Canadian cardiovascular society guidelines for the management of dyslipidemia for the prevention of cardiovascular disease in the adult. Can J Cardiol. 2016;32:1263–82. [PubMed] [Google Scholar]
111. Larsson SC, Orsini N. Red meat and processed meat consumption and all-cause mortality: a meta-analysis. Am J Epidemiol. 2014;179:282–9. [PubMed] [Google Scholar]
112. Kwok CS, Umar S, Myint PK, Mamas MA, Loke YK. Vegetarian diet, seventh day Adventists and risk of cardiovascular mortality: a systematic review and meta-analysis. Int J Cardiol. 2014;176:680–6. [PubMed] [Google Scholar]
113. Crowe FL, Appleby PN, Travis RC, Key TJ. Risk of hospitalization or death from ischemic heart disease among British vegetarians and nonvegetarians: results from the EPIC-Oxford cohort study. Am J Clin Nutr. 2013;97:597–603. [PubMed] [Google Scholar]
114. Liu RH. Dietary bioactive compounds and their health implications. J Food Sci. 2013;78:A18–A25. [PubMed] [Google Scholar]
115. Gilani GS, Wu XC, Cockell KA. Impact of antinutritional factors in food proteins on the digestibility of protein and the bioavailability of amino acids and on protein quality. Br J Nutr. 2012;108:S315e32. [PubMed] [Google Scholar]
116. Friedman M, Brandon DL. Nutritional and health benefits of soy proteins. J Agric Food Chem. 2001;49:1069e86. [PubMed] [Google Scholar]
117. Freeman JM, Kossoff EH. Ketosis and the ketogenic diet, 2010: advances in treating epilepsy and other disorders. Adv Pediatr. 2010;57:315–29. [PubMed] [Google Scholar]
118. Caprio M, Infante M, Moriconi E, Armani A, Fabbri A, Mantovani G, et al. On behalf of the Cardiovascular Endocrinology Club of the Italian Society of Endocrinology. Very-low-calorie ketogenic diet (VLCKD) in the management of metabolic diseases: systematic review and consensus statement from the Italian Society of Endocrinology (SIE). J Endocrinol Investig. 2019. 10.1007/s40618-019-01061-2. [PubMed]
119. Stafstrom CE, Rho JM. The ketogenic diet as a treatment paradigm for diverse neurological disorders. Front Pharmacol. 2012;3:59. [PMC free article] [PubMed] [Google Scholar]
120. Matthew JS, William JK, Dawn ML, Neva GA, Ana LG, Timothy PS, Jeff SV. A ketogenic diet favorably affects serum biomarkers for cardiovascular disease in normal-weight men. J Nutr. 2002;132:1879–85. [PubMed] [Google Scholar]
121. Kirk E, Reeds DN, Finck BN, Mayurranjan SM, Mayurranjan MS, Patterson BW, et al. Dietary fat and carbohydrates differentially alter insulin sensitivity during caloric restriction. Gastroenterology. 2009;136:1552–60. [PMC free article] [PubMed] [Google Scholar]
122. Browning JD, Baker JA, Rogers T, Davis J, Satapati S, Burgess SC. Short-term weight loss and hepatic triglyceride reduction: Evidence of a metabolic advantage with dietary carbohydrate restriction. Am J Clin Nutr. 2011;93:1048–52. [PMC free article] [PubMed] [Google Scholar]
123. Sevastianova K, Kotronen A, Gastaldelli A, Perttilä J, Hakkarainen A, Lundbom J, et al. Genetic variation in PNPLA3 (adiponutrin) confers sensitivity to weight loss-induced decrease in liver fat in humans. Am J Clin Nutr. 2011;94:104–11. [PubMed] [Google Scholar]
124. Shen J, Wong GL-H, Chan HL-Y, Chan RS-M, Chan H-Y, Chu WC-W, et al. PNPLA3 gene polymorphism and response to lifestyle modification in patients with nonalcoholic fatty liver disease. J Gastroenterol Hepatol. 2015;30:139–46. [PubMed] [Google Scholar]
125. Katanoda K, Kim HS, Matsumura Y. New Quantitative Index for Dietary Diversity (QUANTIDD) and its annual changes in the Japanese. Nutrition. 2006;22:283–7. [PubMed] [Google Scholar]
126. Iso H, Kobayashi M, Ishihara J. Intake of fish and n3 fatty acids and risk of coronary heart disease among Japanese: the Japan Public Health Center-Based (JPHC) Study Cohort I. Circulation. 2006;113:195–202. [PubMed] [Google Scholar]
127. Takachi R, Inoue M, Ishihara J. Fruit and vegetable intake and risk of total cancer and cardiovascular disease: Japan Public Health Center-Based Prospective Study. Am J Epidemiol. 2006;167:59–70. [PubMed] [Google Scholar]
128. Adeva MM, Souto G. Diet-induced metabolic acidosis. Clin Nutr. 2011;30:416–21. [PubMed] [Google Scholar]
129. Akter S, Eguchi M, Kuwahara K, Kochi T, Ito R, Kurotani K, et al. High dietary acid load is associated with insulin resistance: the Furukawa Nutrition and Health Study. Clin Nutr. 2016;35:453–9. [PubMed] [Google Scholar]
130. Moghadam SK, Bahadoran Z, Mirmiran P, Tohidi M, Azizi F. Association between dietary acid load and insulin resistance: Tehran Lipid and Glucose Study. Prev Nutr Food Sci. 2016;21:104–9. [PMC free article] [PubMed] [Google Scholar]
131. Haghighatdoost F, Najafabadi MM, Bellissimo N, Azadbakht L. Association of dietary acid load with cardiovascular disease risk factors in patients with diabetic nephropathy. Nutrition. 2015;31:697–702. [PubMed] [Google Scholar]
132. Zhang L, Curhan GC, Forman JP. Diet-dependent net acid load and risk of incident hypertension in United States women. Hypertension. 2009;54:751–5. [PMC free article] [PubMed] [Google Scholar]
133. Kiefte-de Jong JC, Li Y, Chen M, Curhan GC, Mattei J, Malik VS, et al. Diet-dependent acid load and type 2 diabetes: pooled results from three prospective cohort studies. Diabetologia. 2017;60:270–9. [PMC free article] [PubMed] [Google Scholar]
134. Tada N, Maruyama C, Koba S, Tanaka H, Birou S, Teramoto T, Sasaki J. Japanese dietary lifestyle and cardiovascular disease. J Atheroscler Thromb. 2011;18:723–34. [PubMed] [Google Scholar]
135. Okada E, Nakamura K, Ukawa S, Wakai K, Date C, Iso H, Tamakoshi A. The Japanese food score and risk of all-cause, CVD and cancer mortality: the Japan Collaborative Cohort Study. Br J Nutr. 2018;120:464–71. [PubMed] [Google Scholar]
Articles from International Journal of Obesity Supplements are provided here courtesy of Nature Publishing Group