Mitä on kolesteroli?
Kehotan tarkkaavaisuuteen ja avoimeen mieleen, koska tämä voi järkyttää herkempiä lukijoita. LDL ei ole kolesterolia! Paha kolesteroli on sellainen kummitusjuttu?
Pahamainen LDL on lipoproteiini (Low Density Lipoprotein), eli kuljetusmolekyyli, jota elimistö tarvitsee triglyseridien, kolesterolin ja rasvaliukoisten vitamiinien kuljettamiseen verenkierrossa.
LDL on kuin pizzataksi, joka kuljettaa ravintoa nälkäisille soluille.
Elimistö saa kolesterolia ravinnosta ja syntetisoi sitä itse soluissa tapahtuvasssa kolesterolisynteesissä. Kolesterolisynteesin lopputuotteita ovat mm. ruoansulatusneste, steroidihormonit, kuten testosteroni ja estrogeeni sekä kalsiumin homeostaasia ja immuunijärjestelmää säätelevä D-vitamiini. Elimistö tarvitsee välttämättä kaikkia näitä.
Koska kolesteroli on elämälle välttämätön steroli, elimistö pyrkii pitämään kolesterolin määrän tasaisena. Ravinnosta saatu kolesteroli vähentää soluissa tapahtuvaa kolesterolisynteesiä.
Ei liene sattumaa, että samalla kun miesten kolesteroli laskee, yhä useampi mies huomaa kärsivänsä testosteronin vajauksesta. Mieskunto laskee samaa tahtia kolesterolin kanssa. Voiko se olla sattumaa? Ehkä, mutta epäilen vahvasti?
Nykyisen lääketieteellisen paradigman karikatyyri on seuraava: laske kolesterolia statiineilla, nosta testoja lääkkeillä, sairastu metaboliseen oireyhtymään ja diabetekseen, korjaa korkea verensokeri metformiinilla tai insuliinilla, syö ohjeiden mukaan riittävästi sokeria ja vedä helvetisti verenpaine-, verensokeri- ja muita lääkkeitä. Syö lääkkeitä lääkkeiden aiheuttamiin sivuoireisiin, äläkä missään nimessä hairahdu ketogeeniseen ruokavalioon, koska siitä voit sairastua! Tuo voisi olla tinfoil-tuesdayn big pharma-hupailu, mutta surullista kyllä se on hyvin lähellä arkista totuutta.
Multippeliskleroottisesti suuntautuneena onnen kerjäläisenä pääsin osaksi institutionalisoitua medikalisaatiota. Etenevään multippeliskleroosiin ei tunneta oireita hidastavaa, tai parantavaa hoitoa, mutta minulla oli reseptillä parhaimmillaan kymmenkunta erilaista droppia ja nappia. Ja voi pojat, että rouskin uskollisesti erilaisia pillereitä ja palleroita, kunnes havahduin siihen, että jokainen syömäni lääke loi tarpeen uudelle lääkkeelle: lepovapinaa korjaavat lääkkeet edellyttivät vastapainoksi lihasrelaksantteja jne.
Oloni oli saamaton, tyhjämielinen, ahdistunut ja fyysisesti heikko. Älkää ymmärtäkö väärin: osa lääkkeistä on potilaille elintärkeitä ja välttämättömiä, mutta kaikki lääkkeet eivät ole kaikille välttämättömiä ja elintärkeitä. Siinä on merkittävä ero. Suunta on aivan väärä, jos meidät medikalisoidaan parhaassa iässä.
Syö, juo, liho, liiku, laihdu, mies, nainen!
Jokainen kolmekymppinen tarvitsee pian oman dosetin. Päivittäinen ääkecocktail on uskonnollinen rituaali, joka pitää kehon kasassa ja maailman radallaan. Mutta ei helvetti! Minun mielestäni ei ole tervettä tai normaalia, että jo kolme- ja nelikymppiset syövät päivittäin 5-10 reseptilääkettä statiineista masennuslääkkeisiin ja närästyslääkkeistä verenohennuslääkkeisiin. Jossain on nyt menty pahasti metsään. Ilmiö on globaali.
Suomessa on puoli miljoonaa diabeetikkoa ja saman verran verenpainelääkkeitä syöviä. Masennuslääkkeitä määrätään yhä nuoremmille ja yhä lievemmillä perusteilla. Joka toinen lapsi sairastaa ADHD:tä ja joka toinen ADD:tä. Terveitä lapsia mahtuu kourallinen tiuhun. Lähes kaikki suomalaiset kärsivät närästyksestä, ummetuksta, turvotuksesta, vitutuksesta ja muista ruoansulatus- ja suolistovaivoista.
Pahaa kolesterolia ei oikeastaan ole olemassa sen enempää kuin yksisarvisia, vampyyrejä tai ihmissusia. On olemassa vain kolesterolia ja erilaisia kolesterolia kuljettavia molekyylejä.
Jos muutat kolesterolimolekyylissä yhdenkin atomin paikan, se ei enää ole kolesterolia. LDL ja HDL ovat kuljetusmolekyylejä, jotka sisältävät samaa kolesterolia, mutta toinen on pahaa kolesterolia ja toinen hyvää kolesterolia.
Mitä se kolesteroli on?
Dave Feldman on käyttänyt vuosikymmenen vastatakseen tähän kysymykseen ja selvittääkseen, mitä kolesteroli oikeasti on. Tutustutaan Feldmanin havaintoihin.
Jos noudatat vähähiilihydraattista ja runsaasti rasvaa sisältävää ketogeenistä ruokavaliota, sinun on hyvä ymmärtää muutama asia kolesterolista ja siitä, kuinka kolesteroli liittyy valitsemaasi elämäntapaan.
Kolesterolista liikkuu paljon kummallisia ja kauhistuttavia juttuja. Osa niistä on totta. Hapettuneet lipoproteiinit ovat todellakin terveydelle haitallisia ja voivat ennustaa sydän- ja verisuonitauteja. Kolesterolia voi kumuloitua verisuonten seinämiin, mutta kysymys kuuluu: onko kolesterolin kumuloituminen verisuonten endoteeleihin syy vai seuraus. Tästä, kuten kaikista asioista, on vähintään kaksi keskenään kinastelevaa näkemystä.
Tässä jutussa käsitellään kolesterolia ensiksi hyvin yksinkertaisella ja yleisellä tavalla. Tämä ei ole täydellinen selvitys kolesterolista. Tätä on yksinkertaistettu tarkoituksella, jotta se olisi helpompi lukea ja ymmärtää. Kirjoituksen toisessa osassa siirrytään vaikeammin sulaviin rasva- ja kolesterolijuttuihin ja lopuksi luodaan katsaus todisteisiin, jotka kyseenalaistavat lipidihypoteesin.
Ennen kuin tutustutaan kolesteroliin, hiljennytään rasvaisten juttujen ja rasvasta saadun energian äärelle. Mitä ruoka ylipäätään on? Mitä rasva on? Mieti sitä hetki. Onko ruoka makaroonilaatikkoa, katkarapusalaattia vai sisäfilepihvi pippurikastikkeella? Ehkä maksalaatikkoa ja puolukkahilloa?
Ihan sama, mitä suuhusi lapioit. Ruoka on elimistölle ensisijaisesti energiaa ja rakennusaineita.
Kaikki elävät organismit muodostuvat ahneista soluista, jotka himoitsevat sokeria, rasvaa ja välttämättömiä ravinteita. Sydän koostuu soluista. Aivot koostuvat soluista. Jokainen solu sisältää kolesterolia ja rasvaa. Puolet aivojen kuivapainosta on rasvaa. Neljännes kehon kolesterolista on aivoissa. Äidin rintamaito sisältää runsaasti myrkyllistä tyydyttynyttä rasvaa ja kolesterolia. Yrittääkö luonto myrkyttää imeväiset?
Hyvä Jumala! Miksei äidinmaito voisi olla kuin kolesterolitonta, laktoositonta, ja rasvatonta monityydyttämätöntä sokeripitoista teollista mönjää?
Biljoonien solujen solupilvet muodostavat jalat, kädet, sormet, varpaat jne. Me ihmiset olemme eräänlaisia mutualistisesti toimivia soluparvia, jotka sekoilevat erilaisten mikrobien kanssa. Kaikki kehon solut ja kehon ulkopuoliset mikrobit janoavat energiaa ja rakennusaineita, jotta ne voivat jakautua.
Solut jakautuvat mitoosissa. Ex nihilo nihil fit – mitään ei synny tyhjästä. Solut tarvitsevat erilaisia aineita uusiutuakseen. Yksi solujen uusiutumisen tarvitsema aine on kolesteroli.
Ja joka Jumalan siunaama päivä noin 200 grammaa soluja uusiutuu sinussakin. Se edellyttää rakennuspalikoita (proteiineja, rasvoja ja suojaravinteita, kuten vitamiineja ja mineraaleja) sekä energiaa (hiilihydraatteja ja rasvaa). Solujen jakautumiseen tarvitaan myös kolesterolia.
Entä kuinka ravinnon sisältämä energia pääsee lautaselta elimistön kaikkiin soluihin ja sinne pikkuvarpaan päähän asti?
Valtaosa soluista ottaa energiaa vereen imeytyneistä ravinteista. Solujen yleisin energialähde on hiilihydraattien sisältämä glukoosi (sokeri). Hiilihydraatit pilkotaan ruoansulatuskanavassa yksittäisiksi sokerimolekyyleiksi, jotka imeytyvät ohutsuolesta verenkiertoon. Verenkierrossa glukoosi pääsee kaikkialle kehoon, sinne pikkuvarpaan päähän asti, jolloin nälkäiset solut voivat napata verenkierrosta joitain ravinteita itselleen.
Solujen ruokailu tapahtuu insuliinin avulla. Insuliini ja glukagoni orkestroivat energia-aineenvaihduntaa energiantuotannosta energian varastointiin. Ilman insuliinia solut eivät pysty tehokkaasti ottamaan verenkierrosta ravintoa, mutta jos insuliinia on liikaa, solut kyllästyvät, eivätkä enää reagoi insuliiniin halutulla tavalla.
Elimistö haluaa pitää sokeriaineenvaihdunnan tasapainossa. Nykyinen elämäntapa ei tue sokeri- ja insuliiniaineenvaihdunnan tasapainoa. Jatkuvasti korkea verensokeri ja insuliini vaurioittavat verisuonia ja elimiä altistaen insuliiniresistenssille, metaboliselle oireyhtymälle (mikä itse asiassa on vain toinen nimitys insuliiniresistenssille), diabetekselle, lihomiselle, Alzheimerin taudille ja sydän- ja verisuonitaudeille.
Glukoosin ohella rasva on myös tärkeä energialähde soluille. Esimerkiksi sydänlihaksen solut hapettavat pitkäketjuisia rasvahappoja betaoksidaatiossa.
Solut saavat rasvahappoja verenkierrosta, mutta hieman eri tavalla kuin glukoosia. Glukoosi voi antautua verenkierron vietäväksi, mutta rasvahapot eivät voi. Rasvahapot tarvitsevat kyydin!
Rasvahapot ja veri ovat kuin öljy ja vesi: ne eivät sekoitu keskenään. Rasvahapot ovat siis hydrofobisia
Rasvahappojen kuljetuksesta vastaa lipoproteiinit. Ensiksikin elimistö pakkaa kolme rasvahappoa yhdistelmämolekyyleiksi, joita kutsutaan triglyserideiksi. Triglyseridit ovat nisäkkäiden tärkein rasva. Ne muodostuvat kolmesta rasvahaposta ja glyseroliosasta (tri-glyseridi).
Seuraavaksi keho valmistaa rasvahapoille kuljetusvälineen. Tämä rasvahappoja kuljettava taksi on lipoproteiini. Perinteisissä tulkinnoissa LDL-lipoproteiineja kutsutaan pahaksi kolesteroliksi. Lipoproteiineja on useita erilaisia. Kullakin on oma tarkoituksensa ja oma reittinsä.
Itse asiassa sellainen lipoproteiini, joka toimittaa kaikkia rasvahappoja, tunnetaan hyvin pienitiheyksisenä lipoproteiinina – tai VLDL:nä (Very Low Density Lipoprotein). Pakettien toimittamisen jälkeen se muuttuu matalatiheyksiseksi lipoproteiiniksi – mutta luultavasti tunnet sen jo lyhenteellä LDL (Low Density Lipoprotein) tai vain pahana kolesterolina.
Kolesteroli on steroideihin kuuluva tyydyttymätön, rengasrakenteinen, veteen liukenematon kiteinen alkoholi, joka ei triglyseridiserkkujensa tapaan sekoitu vereen. Kolesteroli hylkii vettä.
Lääketieteellisessä maailmassa triglyseridi- ja kolesterolimolekyylejä kutsutaan yleisesti lipideiksi. Lipidit hylkivät vettä, joten niitä sanotaan hydrofobisiksi (hydro = vesi, fobinen = hylkivä).
Elimistöllä voi olla syitä kolesterolin saatavuudelle myös verenkierrossa, mutta palataan siihen tuonnempana. On vielä muutama muu vesikammoinen paketti, jotka keho haluaa toimittaa soluihin kyydillä: nimittäin rasvaliukoiset A-, E-, D- ja K-vitamiinit.
Pitäisikö kehon valmistaa erillinen lipoproteiinitaksi kullekin näistä molekyyleistä?
Elimistö pakkaa kaikki munat tehokkaasti samaan koriin: lipoproteiiniin. Ihmiskeho on hämmästyttävän älykkäästi kehittynyt ja joustava. Elämä on kehittänyt eräänlaisen FedEx-kuljetuspalvelun kaikille solujen tarvitsemille vesikammoisille elementeille. Se ei ole ihmisen suuri saavutus, sillä kolesteroli on välttämätöntä kaikelle elämälle.
Suurin osa kolesterolista, jota ei käytetä solujen uusiutumiseen, kierrätetään muihin käyttötarkoituksiin, kuten steroidihormonien tai sappinesteen tuotantoon.
Olet ehkä kuullut sanottavan, että triglyseridit lisääntyvät vähähiilihydraattisella ruokavaliolla. Se ei täsmälleen ottaen ole totta.
Itse asiassa rasvassa rietastelevien LCHF-ketohörhöjen verikokeissa triglyseridipitoisuudet ovat alhaisempia, kuin teveellistä 40-60 prosenttista sokeridieettiä noudattavilla ravitsemusneuvottelukunnan ohjeiden mukaista ruokavaliota suosivilla verrokki-ihmisillä.
Hiljattain ystäväni mittautti veriarvot. Vuoden ketogeenisen ruokavalion jälkeen triglyt olivat optimaaliset, trigly-HDL-suhde optimaalinen, HDL erinomainen ja LDL:n määrässä ei ollut tapahtunut muutosta suhteessa esiketoilevaan aikaan. Sen sijaan hän oli pudottanut painoa 19 kiloa, päässyt verenpainelääkkeistä ja laskenut verensokerin esidiabeettiselta tasolta optimaaliseksi. Lääkäri oli aiheellisen huolestunut,..
Analogia: Verenkierto on kuin liikenneväylä. Tehtaat, eli solut, tarvitsevat ravinteita ja energiaa. Välillä liikenne ruuhkautuu. Erityisesti niin tapahtuu ruokailun jälkeen, jolloin veressä on runsaasti erilaisia ravinteita matkalla soluihin. Verikoe kertoo miten aktiivista työmatkaliikenne on. Se kertoo kuinka paljon glukoosia tai rasvaa on matkalla soluihin. Se ei kuitenkaan suoraan kerro, kuinka paljon ja kuinka tehokkaasti solut käyttävät ko. ravintoaineita.
Tyypin 2 diabeteksen yleinen oire on, että veressä on erittäin paljon glukoosia myös silloin kuin työmatkaliikenne ei ole aktiivista. Tämä kertoo siitä, että glukoosin pääsy soluihin on heikentynyt. Aikuistyypin diabeetikot ovat insuliiniresistenttejä. Insuliiniresistentit solut ovat ikään kuin lakossa. Ne eivät reagoi insuliiniin toivotulla tavalla. Insuliiniresistentit solut päästävät vain vähän ravinteita soluun. Seurauksena on, että solulaitteet ja solut surkastuvat ja kuolevat energianpuutteeseen.
Samalla verenkierron työmatkaliikenne uhkaa kirjaimellisesti puuroutua, sillä glukoosi aiheuttaa veressä glykaatiota, joka tekee verestä siirappia. Se kohottaa verenpainetta, ja on muutenkin rinnastettavissa kymmenen auton ketjukolariin Länsi- tai Itäväylällä.
Diabetesta sairastavat voivat syödä saman määrän ruokaa kuin terveet, mutta diabeetikon verensokeri nousee korkeammaksi ja laskee hitaammin insuliinin heikentyneen vaikutuksen vuoksi.
Insuliiniresistenssit solut eivät saa energiaa yhtä tehokkaasti kuin terveet solut. Se voi lisätä nälkää säätelevien hormonien, kuten greliinin eritystä, jolloin olo on nälkäinen pian syömisen jälkeen.
Veren glukoosista on päästävä eroon, koska muuten se tukkii suonet glykatoitumalla muiden ravinteiden kanssa.
Osa glukoosista säilötään rasvasoluihin, joiden insuliinisensitiivisyys säilyy lihassoluja kauemmin. Osan elimistö yrittää pissata pois. Siksi diabetesta sairastavien virtsaneritys lisääntyy.
Hyvin yleinen uniapnea johtuu erään hypoteesin mukaan myös korkeasta verensokerista, joka kuluttaa B1-vitamiinia; tiamiini on välttämätön vitamiini aivojen hengityskeskuksen autonomisen toiminnan säätelyssä. Tiamiinin puute aiheuttaa beriberiä ja SIDS-oireyhtymää (kätkytkuolema). Yksinkertaisin ja halvin tapa helpottaa uniapneaa on laskea verensokeria ja varmistaa B1-vitamiinin riittävä saanti.
Jos olet vähentänyt hiilihydraatteja ja saat energiasi pääasiassa rasvasta, solusi ottavat rasvaa tehokkaasti verenkierrosta. Vaikka ruokavalio sisältäisi enemmän rasvaa ja kolesterolia, niiden määrä verenkierrossa laskee, koska solut ottavat verenkierrosta glukoosin puutteessa rasvaa ja kolesterolia tehokkaammin.
Toinen yleinen oletus ketogeenisestä ruokavaliosta on, että suurin osa energiasta saadaan ketoneista, koska ketogeeninen ruokavalio johtaa ketoosiin. Maksa valmistaa ketogeenisellä ruokavaliolla energiasubstraateiksi kelpaavia ketoaineita vapaista rasvahapoista, mutta vaikka ketoaineiden tuotanto ja käyttö lisääntyy, ne ovat toissijainen energianlähde. Ensisijainen energianlähde ovat vapaat rasvahapot,joita hapetetaan energiaksi betaoksidaatiossa. Toisaalta aivojen soluille ketoaineet, kuten beta-hydroksibutyraatti, ovat optimaalista ravintoa.
Entä kuinka vapaat rasvahapot pääsevät soluihin, jossa niitä hapetetaan energiaksi? Vapaat rasvahapot kuljetetaan soluihin LDL-kuljetusmolekyylien kuljettamina. Siis se paha kolesteroli vie ruokaa soluille. Aika paha, vai mitä luulet?
Hiilihydraatteja rajoittavalla ruokavaliolla elimistön on korvattava glukoosin puute ja liikuteltava enemmän triglyseridejä solujen polttoaineeksi, koska suurin osa energiasta otetaan rasvasta. Ruokavalion vaikutuksesta veren triglyseriditasot laskevat, koska solut ottavat rasvaa vastaan ja hapettavat siitä energiaa.
Veren rasva- ja kolesteroliarvot korjaantuvat jo kolmessa kuukaudessa. Samalla verenpaine ja paino laskevat. Lue tästä!
- Solut tarvitsevat energiaa
- Rasvaisella ruokavaliolla solujen ensisijainen energialähde on triglyseridit
- Triglyseridit kuljetetaan soluihin hyvin pienitiheyksisissä lipoproteiineissa (VLDL), jotka lopulta muuttuvat pienitiheyksisiksi lipoproteiineiksi (LDL)
- Kaikki hyvin pienitiheyksiset lipoproteiinit (VLDL) sisältävät sekä triglyseridejä että kolesterolia (mutta enimmäkseen triglyseridejä)
Meidät on ehdollistettu uskomaan, että kolesteroli on tosi paha asia. Niin yksinkertaista se ei suinkaan ole. Kolesteroli voi tietyissä tilanteissa kasvattaa sairastumisen riskiä, mutta laajasti ottaen elimistömme ja itse asiassa elämä itsessään on täysin riippuvainen kolesterolista.
Lipoproteiini on hieman kuin postin pakettiauto. Se kuljettaa triglyserdien lisäksi kolesterolia ja rasvaliukoisia vitamiineja. Kolesterolin osuus lipoproteiinin lastista on hyvin niukka.
Kolesteroli kierrätetään enimmäkseen takaisin maksassa. Kolesterolin olemassaolo itsessään ei ole riski. Riski syntyy lipoproteiinien oksidoituessa ja tulehdustilanteissa.
Tämä on kolesterolista käytävän tulehduskeskustelun ydin. Vahingoittaako kolesteroli verisuonia? Vai onko kolesteroli laastari, joka paikkaa verisuoniin syntyneitä vaurioita? Perinteinen muna-kana-kysymys siis!
Monet arvovaltaiset tutkijat, lääkärit ja laitokset ovat kallistuneet jälkimmäisen hypoteesin kannattajiksi. Kolesterolikeskustelua tärkeämpää olisi varoittaa korkean verensokerin, hyperinsulinemian, insuliiniresistenssin ja diabeteksen aiheuttamista sydän- ja verisuonitautiriskeistä. Ne nimittäin ovat hyvin todellisia riskejä yli puolelle miljoonalle suomalaiselle diabeetikolle.
2. osa: Mitä se kolesteroli siis on?
Tämä on astetta laajempi ja teknisempi selitys kolesterolista. Kolesteroli (tulee antiikin Kreikan sanoista chole– (sappi) ja stereos (kiinteä), jota seuraa alkoholin kemiallinen loppuliite -ol) on orgaaninen molekyyli.
Se on steroli (tai modifioitu steroidi), siis eräänlainen lipidi. Kolesterolia biosyntetisoituu kaikissa eläinsoluissa, ja se on olennainen eläinsolukalvojen rakenteellinen komponentti. Kolesteroli toimii myös esiasteena steroidihormonien, sappihapon ja D-vitamiinin biosynteesissä.
Kolesteroli on tärkein kaikkien eläinten syntetisoima steroli. Selkärankaisilla maksan solut tuottavat tyypillisesti suurimman osan kolesterolista. Sitä ei ole prokaryooteilla (bakteereilla ja arkeilla), vaikka on olemassa joitain poikkeuksia, kuten Mycoplasma, jotka edellyttää kasvua varten kolesterolia.
François Poulletier de la Salle tunnisti kolesterolin kiinteässä muodossa sappikivissä ensimmäisen kerran vuonna 1769. Vasta vuonna 1815 kemisti Michel Eugène Chevreul nimitti yhdisteen ”kolesteriiniksi”.
Kolesteroli on välttämätöntä elämälle, ja jokainen solu kykenee syntetisoimaan sen monimutkaisen 37-vaiheisen prosessin avulla. Tämä alkaa mevalonaatti- tai HMG-CoA-reduktaasireitillä, joka on statiinilääkkeiden kohde, joka käsittää ensimmäiset 18 vaihetta. Tätä seuraa 19 lisävaihetta saadun lanosterolin muuttamiseksi kolesteroliksi.
Mies, joka painaa 68 kg, syntetisoi normaalisti noin 1 gramman (1000 mg) kolesterolia päivässä, ja hänen kehossaan on noin 35 g kolesterolia (lähinnä solukalvoissa). Tyypillinen päivittäinen kolesterolin saanti ravinnosta Yhdysvalloissa on 307 mg.
Suurin osa nautitusta kolesterolista on esteröitynyttä, minkä vuoksi se imeytyy suolesta elimistöön hyvin huonosti. Elimistö kompensoi myös nautittavan kolesterolin meytymistä vähentämällä omaa kolesterolisynteesiään. Näistä syistä ravinnon sisältämällä kolesterolilla on seitsemän – kymmenen tuntia nauttimisen jälkeen vain vähän tai ei lainkaan vaikutusta veren kolesterolipitoisuuksiin.
Mutta kolesterolin saanti ravinnosta nostaa kolesterolipitoisuutta seitsemän ensimmäisen tunnin aikana ruokailun jälkeen. Tämä johtuu siitä, että lipoproteiinit (jotka kuljettavat kaikkia elimistöön imeytyneitä lipidejä solujen ulkopuolella) jakautuvat kehon ympäri solunulkoiseen veteen, Tämän vuoksi pitoisuudet kasvavat.
Kasvit eivät tuota kolesterolia, mutta ne tuottavat fytosteroleja, jotka ovat kemiallisesti samanlaisia aineita. Samankaltaisuutensa vuoksi ne voivat kilpailla kolesterolin kanssa suoliston takaisinimeytymisestä ja siten vähentää kolesterolin reabsorptiota.
Kun suoliston vuoraussolut imevät fytosteroleja kolesterolin sijasta, ne erittävät tavallisesti fytosterolimolekyylit takaisin ruoansulatuskanavaan, mikä on tärkeä suojamekanismi. Luonnossa esiintyvien kasvisterolien ja stanolien sisältämien fytosterolien saanti vaihtelee välillä ~ 200–300 mg päivässä syömistottumuksista riippuen. Kasvisruokavalioissa fytosterolien saanti voi kasvaa 700 mg:n vuorokausisaantiin.
Kolesteroli muodostaa noin 30% kaikista eläinsolujen kalvoista eli membraaneista. Sitä tarvitaan solukalvojen rakentamiseksi ja ylläpitämiseksi. Kolesteroli moduloi kalvojen juoksevuutta fysiologisten lämpötilojen alueella. Kunkin kolesterolimolekyylin hydroksyyliryhmä on vuorovaikutuksessa kalvoa ympäröivien vesimolekyylien kanssa, samoin kuin kalvon fosfolipidien ja sfingolipidien napapäät, kun taas iso steroidi- ja hiilivetyketju on upotettu kalvoon, polaarisen rasvahappoketjun rinnalla.
Muut lipidit
Kolesteroli lisää kalvopakkauksia vuorovaikutuksessa fosfolipidirasvahappoketjujen kanssa, mikä muuttaa kalvon juoksevuutta ja ylläpitää kalvon eheyttä siten, että solujen ei tarvitse rakentaa erillisiä soluseiniä (kuten kasvien ja useimpien bakteerien). Kalvo pysyy vakaana ja kestävänä olematta jäykkä, jolloin solut voivat muuttaa muotoa ja soluelimet liikkua.
Kolesterolin tetrasyklisen renkaan rakenne edistää solukalvon juoksevuutta, koska molekyyli on trans-konformaatiossa, joka tekee kolesterolin sivuketjun paitsi jäykäksi, myös tasomaiseksi. Tässä rakenteellisessa roolissa kolesteroli vähentää neutraalien liuenneiden aineiden, sekä vety- ja tatriumionien plasmakalvon läpäisevyyttä.
Kolesteroli vaikuttaa solunsisäisessä kuljetuksessa, solujen signaloinnissa ja hermoissa kulkevien signaalien johtamisessa. Kolesteroli on välttämätön invasiivisten caveolae- ja klatrriinipäällysteisten kuoppien rakenteelle ja toiminnalle, mukaan lukien caveolasta riippuvainen ja klathriinista riippuvainen endosytoosi.
Kolesterolin roolia tämän tyyppisessä endosytoosissa voidaan tutkia käyttämällä metyylibeta-syklodekstriiniä (MβCD) kolesterolin poistamiseksi plasmamembraanista. Kolesteroli säätelee substraatin esittelyn biologista prosessia ja entsyymejä, jotka käyttävät substraatin esittelyä aktivoitumismekanismina. (PLD2) on hyvin määritelty esimerkki entsyymistä, joka aktivoituu substraatin esittämisen avulla. Entsyymi palmitoyloidaan*, jolloin entsyymi kulkeutuu kolesterolista riippuvaisiin lipididomeeneihin, joita kutsutaan joskus ”lipidilautoiksi”.
| *Palmitoylaatio tapahtuu, kun rasvahappoihin sitoutuu kovalenttisesti kalvoproteiini, kuten palmitiinihappo, johon on sitoutunut kysteiini ( S -palmitoylation) ja harvemmin seriini tai treoniini. Palmitoylaation tarkka toiminta riippuu tarkasteltavasta proteiinista. Palmitoylaatio lisää proteiinien hydrofobisuutta ja myötävaikuttaa niiden kalvoyhdistelmään. Palmitoylaatiolla näyttää myös olevan merkittävä rooli proteiinien solunsisäisessä liikenteessä membraaniosastojen välillä sekä proteiini-proteiini-vuorovaikutuksen moduloinnissa . Toisin kuin prenylaatio ja myristoylaatio, palmitoylaatio on yleensä palautuva,k koska palmitiinihapon ja proteiinin välinen sidos on usein tioesterisidos. Käänteisen reaktion nisäkkään soluissa katalysoivat asyyli-proteiini tioesteraasit (APT) solujen sytosolissa ja palmitoyyli-proteiinin tioesteraasit lysosomeissa. Koska palmitoylaatio on dynaaminen, translaation jälkeinen prosessi, solun uskotaan käyttävän sitä muuttavan proteiinin solunsisäistä sijaintia, proteiini-proteiini-vuorovaikutusta tai sitoutumiskapasiteettia. Esimerkki palmitoylaation läpikäyvästä proteiinista on hemagglutiniini , membraaniglykoproteiini, jota influenssa-virus käyttää isäntäsolureseptoreihin kiinnittymiseen. Lukuisten entsyymien palmitoylaatiojaksot on tunnistettu viime vuosina, mukaan lukien: H-Ras , Gsα , β2-adrenerginen reseptori ja endoteelin typpioksidisyntaasi (eNOS). Signaalitransduktiossa G-proteiinin kautta a-alayksikön palmitoylaatio, y-alayksikön prenylaatio ja myristoylaatio osallistuvat G-proteiinin sitomiseen plasmakalvon sisäpintaan niin, että G-proteiini voi olla vuorovaikutuksessa reseptorinsa kanssa. S-palmitoylaation tekevät yleensä proteiinit, joilla on DHHC-domeeni . Ei-entsymaattisissa reaktioissa on poikkeuksia. Asyyliproteiinitioesteraasi (APT) katalysoi käänteisen reaktion. Myös muut asyyliryhmät, kuten stearaatti tai oleaatti, hyväksytään usein kasvien ja virusten proteiineissa, mikä tekee S-asyloinnista käyttökelpoisemman nimen. Noin 40% synaptisista proteiineista löydettiin palmitoylomeista. Palmitoylaatio välittää proteiinin affiniteetin lipidilauttoihin ja helpottaa proteiinien klusteroitumista. Klusterointi voi lisätä kahden molekyylin läheisyyttä. Vaihtoehtoisesti klusterointi voi sitoa proteiinin pois substraatista. Esimerkiksi fosfolipaasi D:n (PLD) palmitoylaatio erottaa entsyymin pois substraatistaan fosfatidyylikoliinista. Kun kolesterolitasot laskevat tai PIP2-tasot lisäävät palmitaatin välittämää lokalisoitumista , entsyymi siirtyy PIP2:een, jossa se kohtaa substraatinsa ja on aktiivinen substraatin esittämisen kautta . Tärkein proteiinin klustereiden välittäjä synapsissa on postsynaptisen tiheyden ( 95 kD) proteiini PSD-95 . Kun tämä proteiini palmitoyloidaan, se rajoittuu kalvoon. Tämän kalvoon kohdistuvan rajoituksen avulla se voi sitoutua postsynaptiseen kalvoon ja klusteroida sen . Presynaptisessa hermosolussa SNAP-25:n palmitoylaatio ohjaa sen jakautumaan solukalvoon ja antaa SNARE- kompleksin hajota vesikkelifuusion aikana. Tämä tarjoaa palmitoylaatiolle roolin välittäjäaineiden vapautumisen säätelyssä . Delta-kateniinin palmitoylaatio näyttää koordinoivan aktiivisuudesta riippuvia muutoksia muistinmuodostukseen osallistuvissa synaptisissa adheesiomolekyyleissä, synapsiorakenteessa ja reseptoripaikannuksissa. Gefyriinin palmitoylaation on raportoitu vaikuttavan GABAergisiin synapseihin. Palmitoylaatio – https://fi.qaz.wiki/wiki/Palmitoylation |
Fosfolipaasi D:n substraatti on fosfatidyylikoliini (PC), joka on tyydyttymätön ja jota on vähän lipidilautoissa. PC lokalisoituu solun häiriintyneelle alueelle yhdessä monityydyttymättömän lipidifosfatidyyli- inositoli 4,5-bisfosfaatin (PIP2) kanssa. PLD2:lla on PIP2:ta sitova domeeni.
Kun PIP2-pitoisuus membraanissa kasvaa, PLD2 poistuu kolesterolista riippuvaisista domeeneista ja sitoutuu PIP2:een, missä se sitten saa pääsyn substraatti-PC:hen ja aloittaa katalyytin substraatin esityksen perusteella.
Solujen signallointi
Kolesteroli on osallisena myös solujen signalointiprosesseissa, mikä auttaa lipidilautojen muodostumista plasmamembraanissa. Prosessi tuo korkean toisioviestimolekyylikonsentraation reseptoriproteiinit esiin. Kolesteroli ja fosfolipidit (sähköeristimet), voivat monella tavalla helpottaa sähköimpulssien siirtonopeutta hermokudosta pitkin.
Monissa hermokuiduissa runsaasti kolesterolia sisältävä myeliinivaippa (joka on peräisin tiivistetyistä Schwannin solukalvokerroksista) tarjoaa eristeen sähköisten impulssien tehokkaammalle johtamiselle. Myeliinivaipan vaurioituminen esimerkiksi multippeliskleroosissa hidastaa tai katkaisee hermostossa kulkevia sähköisiä impulsseja, jolloin aivojen lähettämät toimintakäskyt eivät aina saavuta lihaksia.
Demyelinaation (Schwann-solujen surkastuminen) uskotaan olevan osa multippeliskleroosin patogeneesiä. Multippelisklerootikkona minulla on siis oma lehmä ojassa. Minä tunnen kolesterolin hieman eri merkityksessä, kuin monet muut. Minä näen kolesterolin hermovälittäjiä suojaavien myeliinivaippojen välttämättömänä rakennusaineena.
Kolesteroli sitoutuu ja vaikuttaa useiden ionikanavien, kuten nikotiiniasetyylikoliinireseptorin, GABA A-reseptorin ja sisäänpäin suuntautuvan kaliumkanavan välityksellä. Kolesteroli aktivoi myös estrogeeniin liittyvän alfa-reseptorin (ERRα) ja se voi olla reseptorin endogeeninen ligandi.
Reseptorin rakenteeltaan aktiivinen luonne voidaan selittää sillä, että kolesterolia on kaikkialla kehossa. ERRα-signaloinnin estäminen kolesterolin tuotannon vähentämisellä on tunnistettu keskeiseksi välittäjäksi statiinien ja bisfosfonaattien vaikutuksissa luuhun, lihakseen ja makrofageihin. Näiden havaintojen perusteella on ehdotettu, että ERRα tulisi luokitella kolesterolin reseptoriksi.
Kolesteroli on mm. steroidihormonien lähtöaine
Kolesteroli on useiden solunsisäisten biokemiallisten reittien edeltäjämolekyyli. Se on lähtöaine D-vitamiinin synteesissä, kalsiumin aineenvaihdunnassa ja kaikkien steroidihormoneien synteesissä, mukaan lukien lisämunuaishormonit kortisoli ja aldosteroni, sekä sukupuolihormonit progesteroni, estrogeenit, testosteroni ja niiden johdannaiset. Elimistö ei syntetisoi kolesterolia turhaan. Sitä tarvitaan lukemattomiin aineenvaihduntatapahtumiin, solukalvoihin, solusignalointiin ja hermoratoja suojaavien myeliinivaippojen rakenteisiin.
Kolesteroli kierrätetään elimistössä. Maksa erittää kolesterolia sappinesteisiin, jotka sitten varastoidaan sappirakoon, joka edelleen erittää kolesterolin esteröimättömässä muodossa (sapen kautta) ruoansulatuskanavaan. Tyypillisesti noin 50% erittyvästä kolesterolista imeytyy ohutsuolessa takaisin verenkiertoon.
Kaikki eläinsolut tuottavat kolesterolia sekä kalvorakenteeseen että muuhun käyttöön, suhteelliset tuotantonopeudet vaihtelevat solutyypin ja elimen toiminnan mukaan. Noin 80% päivittäisestä kolesterolituotannosta tapahtuu maksassa ja suolistossa; muita korkeampia synteesinopeuspaikkoja ovat aivot, lisämunuaiset ja lisääntymiselimet. Kolesterolin biosynteesiä säätelevät suoraan olemassa olevat kolesterolitasot, vaikka mukana olevat homeostaattiset mekanismit ymmärretään vain osittain. Suurempi ravinnon kolesterolipitoisuus johtaa endogeenisen tuotannon nettovähennykseen, kun taas pienemmällä kolesterolin saannilla on päinvastainen vaikutus.
Tärkein säätelymekanismi on solunsisäisen kolesterolin havaitseminen endoplasman verkkokalvossa SREBP-proteiinin (sterolia säätelevää elementtiä sitova proteiini 1 ja 2) avulla.
Kolesterolin läsnä ollessa SREBP sitoutuu kahteen muuhun proteiiniin: SCAP:iin (SREBP:n pilkkoutumista aktivoivaan proteiiniin) ja INSIG-1:een. Kun kolesterolitaso laskee, INSIG-1 irtoaa SREBP-SCAP-kompleksista, mikä antaa kompleksin siirtyä Golgin laitteisiin. Tässä SREBP katkaistaan S1P: llä ja S2P: llä (site-1-proteaasi ja site-2-proteaasi), kahdella entsyymillä, jotka aktivoituvat SCAP:lla, kun kolesterolitasot ovat alhaiset. Pilkottu SREBP siirtyy sitten solun tumaan ja toimii transkriptiotekijänä sitoutuakseen sterolin säätelyelementtiin (SRE), joka stimuloi monien geenien transkriptiota. Näitä ovat pienitiheyksinen lipoproteiinireseptori (LDL) ja HMG-CoA-reduktaasi. LDL-reseptori imee verenkierrossa kiertävää LDL:ää, kun taas HMG-CoA-reduktaasi johtaa kolesterolin endogeenisen tuotannon lisääntymiseen.
Suuren osan tästä signalointireitistä selvittivät tohtori Michael S. Brown ja tohtori Joseph L. Goldstein 1970-luvulla. Vuonna 1985 he saivat Nobel-palkinnon fysiologisesta ja lääketieteestä työstään. Heidän myöhempi työ osoittaa, kuinka SREBP-reitti säätelee monia lipidien metaboliaa ja muodostumista sekä energiasubstraattien allokointia kontrolloivien geenien ilmentymistä.
Kolesterolisynteesi voidaan myös kytkeä pois päältä, kun kolesterolitaso on korkea. HMG-CoA-reduktaasi sisältää sekä sytosolidomeenin (vastuussa sen katalyyttisestä toiminnasta) että kalvodomeenin. Kalvodomeeni tunnistaa signaalit sen hajoamisesta. Kolesterolin (ja muiden sterolien) lisääntyvät pitoisuudet aiheuttavat muutoksen tämän domeenin oligomerisaatiotilassa, mikä tekee siitä alttiimman proteosomin tuhoamiselle. Tämän entsyymin aktiivisuutta voidaan vähentää myös fosforyloimalla AMP-aktivoidulla proteiinikinaasilla. Koska tämä kinaasi aktivoituu AMP:llä, joka syntyy, kun ATP hydrolysoidaan, seuraa, että kolesterolisynteesi pysähtyy, kun ATP-tasot ovat alhaiset.
Eristettynä molekyylinä kolesteroli liukenee huonosti veteen (se on heikosti hydrofiilinen). Tämän vuoksi kolesterolia liukenee vereen erittäin pieninä pitoisuuksina.
Lipoproteiinit
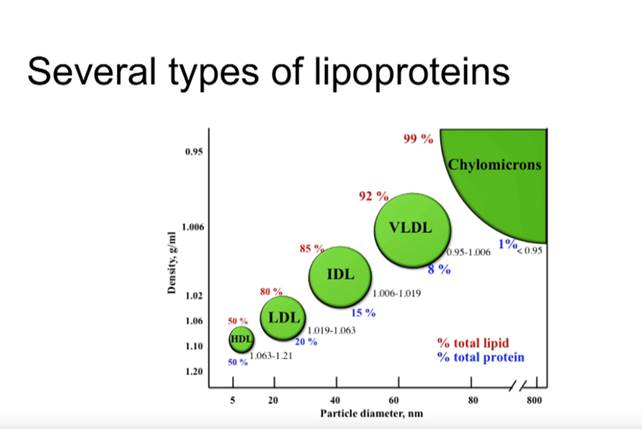
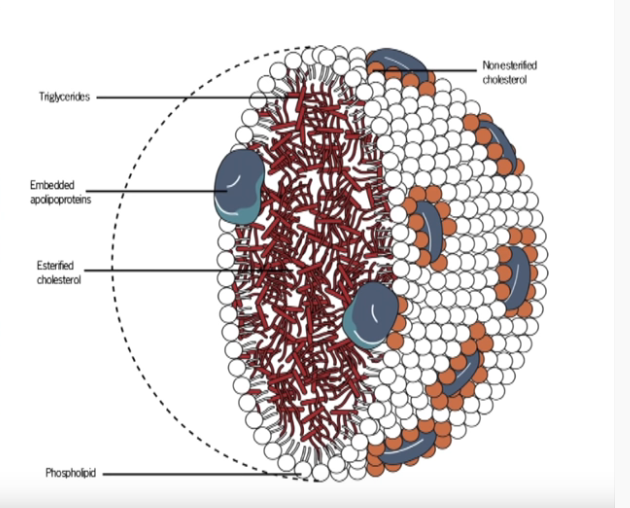
Tehokkaasta kolesterolin kuljetuksesta vastaavat lipoproteiinit, joihin kolesteroli pakataan. Lipoproteiinit ovat monimutkaisia diskoidisia molekyylejä, joissa on ulkopuolisia amfifiilisiä proteiineja ja lipidejä, joiden ulospäin suuntautuvat pinnat ovat vesiliukoisia ja sisäänpäin osoittavat pinnat rasvaliukoisia.
Rakenteensa ansiosta lipoproteiini voi kulkea veren läpi emulgoinnin avulla. Sitoutumaton kolesteroli, joka on amfipaattinen, kulkeutuu lipoproteiinimolekyylin yksikerroksisella pinnalla fosfolipidien ja proteiinien mukana. Rasvahappoon sitoutuneet kolesteroliesterit kulkeutuvat toisaalta lipoproteiinin rasva-hydrofiilisen ytimen sisällä yhdessä triglyseridin kanssa.
Veressä on useita lipoproteiinityyppejä. Suuren tiheyden järjestyksessä ne ovat kylomikronit, hyvin matalatiheyksinen lipoproteiini (VLDL), keskitiheyksinen lipoproteiini (IDL), matalatiheyksinen lipoproteiini (LDL) ja suuritiheyksinen lipoproteiini (HDL).
Eri lipoproteiinien kuljettma kolesteroli on kemiallisesti on identtistä, vaikka jotkut kolesterolimolekyylit kulkeutuvatkin kolesterolin natiivina ”vapaana” alkoholimuotona (kolesteroli-OH-ryhmä), kun taas toisissa molekyyleissä kolesteroli on rasva-asyyliestereinä, jotka tunnetaan myös kolesteroliesterinä.
Lipoproteiinimolekyylit organisoidaan monimutkaisilla apolipoproteiineilla, tyypillisesti 80-100 erilaista proteiinia partikkelia kohden, jotka voidaan tunnistaa ja sitoa solukalvojen spesifisillä reseptoreilla, ohjaamalla niiden lipidien hyötykuorma spesifisiin soluihin ja kudoksiin, jotka ovat herkistyneitä näille rasvansiirtomolekyyleille.
Nämä pintareseptorit toimivat ainutlaatuisina molekyylirekistereinä, jotka auttavat rasvan jakautumisen koko kehoon. Kylomikronit, eli vähiten tiheät kolesterolia kuljettavat molekyylit, sisältävät kuorissaan apolipoproteiini B-48:n, apolipoproteiini C:n ja apolipoproteiini E:n (tärkein kolesterolin kuljettaja aivoissa). Kylomikronit kuljettavat rasvoja suolesta lihaksiin ja muihin kudoksiin, jotka tarvitsevat rasvahappoja energiaksi tai rasvan tuottamiseksi.
Maksa tuottaa VLDL-molekyylejä triglyserideistä ja kolesterolista, jota ei käytetty sappihappojen synteesissä. Nämä molekyylit sisältävät kuorissaan apolipoproteiini B100:n ja apolipoproteiini E:n, ja valtimon seinämän lipoproteiinilipaasi voi hajottaa ne IDL:ksi. Tämä valtimon seinämän pilkkominen sallii triglyseridin imeytymisen ja lisää kiertävän kolesterolin pitoisuutta. IDL-molekyylejä kulutetaan sitten kahdessa prosessissa: puolet metaboloituu HTGL:n kautta ja LDL-reseptori vie ne maksan solupinnoille, kun taas toinen puoli menettää edelleen triglyseridejä verenkierrossa, kunnes niistä tulee kolesterolipitoisia LDL-molekyylejä.
LDL-molekyylit ovat tärkeimmät veren kolesterolinkuljettajat. Jokainen niistä sisältää noin 1500 kolesteroliesterimolekyyliä. LDL-molekyylikuoret sisältävät vain yhden molekyylin apolipoproteiini B100:n, jonka perifeeristen kudosten LDL-reseptorit tunnistavat. Apolipoproteiini B100:n sitoutuessa monet LDL-reseptorit keskittyvät klatriinilla päällystettyihin kuoppiin. Sekä LDL että sen reseptori muodostavat rakkuloita solussa endosytoosin kautta. Nämä rakkulat sulautuvat sitten lysosomiin, jossa lysosomaalihappo-lipaasientsyymi hydrolysoi kolesteroliesterit.
Kolesterolia voidaan sitten käyttää membraanin biosynteesiin tai esteröidä ja varastoida soluun, jotta se ei häiritse solukalvoja. LDL-reseptorit kuluvat kolesterolin imeytymisen aikana, ja sen synteesiä säätelee SREBP, sama proteiini, joka kontrolloi kolesterolin synteesiä de novo, sen mukaan, onko se solussa. Solun, jossa on runsaasti kolesterolia, LDL-reseptorisynteesi estetään, jotta estetään uuden kolesterolin lisääntyminen LDL-molekyyleissä. Päinvastoin, LDL-reseptorisynteesi etenee, kun solussa on kolesterolipuutetta.
Paha kolesteroli
Kun tämä prosessi muuttuu sääntelemättömäksi, veressä alkaa näkyä LDL-molekyylejä, joissa ei ole reseptoreita. Nämä LDL-molekyylit hapetetaan ja ne imeytyvät makrofageihin, jotka tukkeutuvat ja muodostavat vaahtosoluja. Nämä vaahtosolut jäävät usein kiinni verisuonten seinämiin ja edistävät ateroskleroottisten plakkien muodostumista. Tämä on se paha kolesteroli.
Kolesterolihomeostaasin häiriöt vaikuttavat varhaisen ateroskleroosin (kaulavaltimon intima-väliaineen paksuus) kehittymiseen. Näiden plakkien yhteys sydänkohtauksiin, aivohalvauksiin ja muihin vakaviin lääketieteellisiin ongelmiin on syy, minkä vuoksi kolesterolia kauhistellaan.
HDL-molekyylien uskotaan kuljettavan kolesterolia takaisin maksaan joko erittymiseen tai muihin hormoneja syntetisoiviin kudoksiin prosessissa, joka tunnetaan käänteisenä kolesterolikuljetuksena (RCT). Suuri määrä HDL-molekyylejä korreloi parempaan terveyteen
Kolesteroli on altis hapettumiselle ja muodostaa helposti hapetettuja johdannaisia, joita kutsutaan oksysteroleiksi. Kolme erilaista mekanismia voi muodostaa tällaisia: autoksidaatio, sekundaarinen hapettuminen lipidiperoksidaatioksi ja kolesterolia metaboloiva entsyymihapetus.
Suuri kiinnostus oksysteroleihin syntyi, kun niiden osoitettiin vaikuttavan estävästi kolesterolin biosynteesiin. Tämä havainto tunnettiin nimellä ”oksysterolihypoteesi”. Oksysterolien lisärooleja ihmisen fysiologiassa ovat niiden osallistuminen sappihappojen biosynteesiin, toiminta kolesterolin kuljetuksessa ja geenitranskription säätely.
Kolesteroli hapetetaan maksassa erilaisiksi sappihapoiksi. Nämä puolestaan ovat konjugoituja glysiinin, tauriinin, glukuronihapon tai sulfaatin kanssa. Konjugoitujen ja konjugoimattomien sappihappojen seos yhdessä kolesterolin kanssa erittyy maksasta sappeen. Noin 95% sappihapoista imeytyy takaisin suolistosta ja loput häviävät ulosteiden mukana. Sappihappojen erittyminen ja imeytyminen muodostavat enterohepaattisen verenkierron perustan, mikä on välttämätöntä ravintorasvojen sulatukselle ja imeytymiselle. Tietyissä olosuhteissa kolesteroli voi kiteytyä sappirakossa ja vaikuttaa sappikivien muodostumiseen (myös lesitiinistä ja bilirubiinista muodostuvia sappikiviä esiintyy, mutta harvemmin).
Joka päivä paksusuoleen pääsee jopa 1 g kolesterolia. Tämä kolesteroli on peräisin ruokavaliosta, sapesta ja suolen poistetuista suolistosoluista, ja paksusuolibakteerit voivat metaboloida sen. Kolesteroli muuttuu pääasiassa koprostanoliksi, imeytymättömäksi steroliksi, joka erittyy ulosteisiin.
Vaikka kolesteroli on steroidi, joka yleensä liittyy nisäkkäisiin, ihmisen patogeeni Mycobacterium tuberculosis pystyy hajottamaan tämän molekyylin täysin ja sisältää suuren määrän geenejä, joita sen läsnäolo säätelee.
Monet näistä kolesterolilla säädellyistä geeneistä ovat rasvahappojen β-hapetusgeenien homologeja, mutta ne ovat kehittyneet sitomaan suuria steroidisubstraatteja, kuten kolesterolia. Eläinrasvat ovat monimutkaisia triglyseridiseoksia, joissa on vähäisempiä määriä sekä fosfolipidejä että kolesterolimolekyylejä, joista kaikki eläin- (ja ihmisen) solukalvot rakennetaan.
Koska kaikki eläinsolut tuottavat kolesterolia, kaikki eläinperäiset elintarvikkeet sisältävät kolesterolia vaihtelevissa määrissä. Suurimpia ruokavalion kolesterolilähteitä ovat punainen liha, munankeltuainen ja kokonaiset munat, maksa, munuaiset, pikkulohet, kalaöljy ja voi. Ihmisen äidinmaito sisältää myös merkittäviä määriä kolesterolia. Kasvisolut syntetisoivat kolesterolia muiden yhdisteiden, kuten fytosterolien ja steroidisten glykoalkaloidien, esiasteena, ja kolesterolia on kasviruoissa vain vähän tai ei ollenkaan. Jotkut kasviruoat, kuten avokado, pellavansiemenet ja maapähkinät, sisältävät fytosteroleja, jotka kilpailevat kolesterolin kanssa imeytymisestä suolistossa, vähentävät sekä ruokavalion että sappikolesterolin imeytymistä. Tyypillinen ruokavalio myötävaikuttaa noin 0,2 gramman fytosteroleihin, mikä ei riitä vaikuttamaan merkittävästi kolesterolin imeytymisen estoon.
Fytosterolien saantia voidaan täydentää käyttämällä fytosterolia sisältäviä funktionaalisia elintarvikkeita tai ravintolisiä, joiden tiedetään olevan potentiaalisia alentamaan LDL-kolesterolitasoja. Vuonna 2016 Yhdysvaltain maatalousministeriön ruokavalion ohjeiden neuvoa-antava komitea suositteli amerikkalaisia syömään mahdollisimman vähän kolesterolia. Useimmissa kolesterolipitoisissa elintarvikkeissa on myös runsaasti tyydyttyneitä rasvoja, mikä voi siten lisätä sydän- ja verisuonitautien riskiä. [57] Joissakin täydentävissä ohjeissa suositellaan fytosterolien annoksia 1,6–3,0 grammaa päivässä (Health Canada, EFSA, ATP III, FDA).
Äskettäinen meta-analyysi osoittaa LDL-kolesterolin laskevan 12%:lla fytosterolien 2,1 gramman päiväsaannilla. Fytosteroleilla täydennetyn ruokavalion edut on kuitenkin kyseenalaistettu.
Perinteisen ja institutionalisoidun lipidihypoteesin mukaan kohonnut kolesterolitaso veressä aiheuttaa ateroskleroosia, mikä voi lisätä sydänkohtauksen, aivohalvauksen ja perifeerisen valtimosairauden riskiä. Koska veren korkeammat LDL-pitoisuudet ja pienempi LDL-partikkelikoko – vaikuttavat tähän prosessiin enemmän kuin HDL-hiukkasten kolesterolipitoisuus, LDL-partikkeleita kutsutaan usein ”pahaksi kolesteroliksi”.
Suuret toiminnallisen HDL:n pitoisuudet, jotka voivat poistaa kolesterolin soluista ja ateroomista, tarjoavat suojan ja niitä kutsutaan yleisesti ”hyväksi kolesteroliksi”. Nämä tasapainot määritetään enimmäkseen geneettisesti, mutta niitä voidaan muuttaa kehon koostumuksen, lääkkeiden, ruokavalion ja muiden tekijöiden perusteella. Vuoden 2007 tutkimus osoitti, että veren kokonaiskolesterolitasoilla on eksponentiaalinen vaikutus sydän- ja verisuonitauteihin ja kokonaiskuolleisuuteen, ja yhteys on selvempi nuoremmilla koehenkilöillä.
Koska sydän- ja verisuonitaudit ovat suhteellisen harvinaisia nuoremmalla väestöllä, korkean kolesterolin vaikutus terveyteen on suurempi iäkkäillä ihmisillä. Kohonnut lipoproteiinifraktioiden, LDL-, IDL- ja VLDL-tasojen, sijaan kokonaiskolesterolitaso, korreloivat ateroskleroosin laajuuden ja etenemisen kanssa.
Päinvastoin, kokonaiskolesteroli voi olla normaaleissa rajoissa, mutta se koostuu pääasiassa pienistä LDL- ja pienistä HDL-hiukkasista, joissa aterooman kasvunopeus on korkea. IDEALin ja EPIC:n prospektiivisten tutkimusten post hoc -analyysi havaitsi yhteyden korkeaan HDL-kolesterolitasoon (mukautettu apolipoproteiini AI ja apolipoproteiini B) ja lisääntyneeseen sydän- ja verisuonitautien riskiin, mikä epäili ”hyvän kolesterolin” kardioprotektiivista roolia.
Yhdellä 250 aikuisesta voi olla geneettinen mutaatio LDL-kolesterolireseptorille, mikä aiheuttaa heille familiaalisen hyperkolestrolemian. Peritty korkea kolesteroli voi myös sisältää geneettisiä mutaatioita PCSK9-geenissä ja apolipoproteiini B -geenissä.
Kohonnutta kolesterolitasoa hoidetaan tiukalla ruokavaliolla, joka koostuu vähärasvaisista ruoista, transrasvattomista sejö vähän kolesterolia sisältävistä elintarvikkeista. Usein (lähes poikkeuksetta) kolesterolin laskua tehostetaan hypolipideemisillä aineilla, kuten statiineilla, fibraateilla, kolesterolin imeytymisen estäjillä, nikotiinisillä happojohdannaisilla tai sappihappoa sitovilla lääkkeillä.
Hyperkolesterolemian hoidossa on useita kansainvälisiä ohjeita. Ihmiskokeet, joissa käytettiin HMG-CoA-reduktaasin estäjiä, jotka tunnetaan nimellä statiinit, ovat toistuvasti vahvistaneet, että lipoproteiinien kuljetusmallien muuttaminen epäterveellisistä terveellisempiin kuvioihin alentaa merkittävästi sydän- ja verisuonitautitapahtumien määrää myös ihmisillä, joiden kolesteroliarvot katsotaan tällä hetkellä alhaisiksi aikuisille.
Tutkimukset ovat osoittaneet, että LDL-kolesterolitasojen alentaminen noin 38,7 mg / dl statiinien avulla voi vähentää sydän- ja verisuonitauteja ja aivohalvausriskiä noin 21%. Tutkimukset ovat myös havainneet, että statiinit vähentävät aterooman etenemistä. Tämän seurauksena ihmiset, joilla on ollut sydän- ja verisuonitauteja, voivat hyötyä statiineista riippumatta heidän kolesterolipitoisuudestaan (kokonaiskolesteroli alle 5,0 mmol / L [193 mg / dl]), ja miehillä, joilla ei ole sydän- ja verisuonitauteja, on hyötyä poikkeuksellisen korkean kolesterolitason alentamisesta (”ensisijainen ennaltaehkäisy”).
Ensisijaista ennaltaehkäisyä naisilla harjoitettiin alun perin vain laajentamalla miehillä tehtyjen tutkimusten tuloksia, koska naisilla yksikään ennen vuotta 2007 toteutetuista suurista statiinitutkimuksista ei osoittanut merkittävää kokonaiskuolleisuuden tai kardiovaskulaaristen päätetapahtumien vähenemistä.
Meta-analyysit ovat osoittaneet merkittävän vähenemisen kaikista syistä ja kardiovaskulaarisesta kuolleisuudesta ilman merkittävää heterogeenisyyttä sukupuolen mukaan. Kansallisen kolesterolikoulutusohjelman vuonna 1987 julkaisema raportti, Aikuisten hoitopaneelit, ehdottaa, että veren kokonaiskolesterolitason tulisi olla: <200 mg / dl normaalia veren kolesterolia, 200–239 mg / dl raja-korkea,> 240 mg / dl korkea kolesteroli.
American Heart Association (AHA) tarjoaa samanlaiset ohjeet veren (paasto) kokonaiskolesterolipitoisuuksista ja sydänsairauksien riskistä: Statiinit alentavat tehokkaasti LDL-kolesterolia ja niitä käytetään laajalti ensisijaiseen ennaltaehkäisyyn ihmisillä, joilla on suuri sydän- ja verisuonitautiriski samoin kuin toissijaisessa ennaltaehkäisyssä niille, joille on kehittynyt sydän- ja verisuonitauti. Nykyisemmät testausmenetelmät määrittävät LDL (”huono”) ja HDL (”hyvä”) kolesterolin erikseen, jolloin kolesterolianalyysi on vivahteikkaampi. Halutun LDL-tason katsotaan olevan alle 130 mg / dl (2,6 mmol / L), vaikka uudempaa ylärajaa 70 mg / dl (1,8 mmol / L) voidaan harkita korkeamman riskin omaavilla henkilöillä joitakin edellä mainituista kokeista. Kokonaiskolesterolin suhde HDL: ään – toinen hyödyllinen mitta – on paljon alle 5: 1.
Keskustelu kolesterolista ja erityisesti pahasta LDL-kolesterolista käy kiivaana. Kaikki eivät suhtaudu luottavaisesti lipidihypoteesin paradigmaan. Epidemiologiset tutkimukset, joita kolesterolihypoteesin tukemiseksi laaditaan, ovat todistusvoimaltaan kovin heppoisia. Virallinen lääke- ja ravitsemustieteellinen linja on selvä: vähemmän kolesterolia ja tyydyttyneitä rasvoja sekä enemmän statiineja. Mitä nuorempana aloitat statiinit, sitä parempi (lääkeyhtiöille). On nimittäin kiusallista tutkimusnäyttöä, jonka mukaan kolesterolin laskeminen lisää sydänkuolleisuutta (Minnesota Heart Study, Framingham Heart Study ja Sydney Heart Study, jotka olivat kontrolloituja satunnaistettuja tutkimuksia).
Palataan rasvateoriaan
Kolesteroliteoria on hallinnut vuosikymmeniä lääkäreiden ja maallikoiden käsityksiä sydän- ja verisuonitautien syistä, mutta on tullut aika hylätä tämä käsitys, kirjoittavat ruotsalaiset tiedemiehet, sisätautiopin professori Lars Werkö, kirurgian professori Tore Schrestén ja elinsiirtokirurgian dosentti Ralf SundBerg.
Sydänkohtaukseen sairastuneiden ja kuolleiden ihmisten kolesterolilukemat ovat usein muita pienempiä. Matala seerumin kolesteroli liittyy suurentuneeseen kuoleman riskiin.
Kiista kolesterolin merkityksestä vauhdittui 1990-luvulla, jolloin monet tutkijat (mm. Ruotsissa sisätautiopin dosentti Uffe Ravnskov) kyseenalaistivat syy-yhteyden korkeiden kolesteroliarvojen ja sydäntautien välillä.
Tämä perustui suureksi osaksi 30 vuotta jatkuneeseen Framinghamin tutkimukseen. Se näet osoitti, ettei kohonnut kolesteroli ole sydäntaudin riskitekijä yli 47-vuotiailla ihmisillä. Asia oli pikemminkin niin päin, että kolesterolin aleneminen lisäsi kuolleisuutta verrattuna niihin, joiden kolesterolipitoisuus suureni.
Sachdevan työryhmä julkaisi tammikuussa 2009 jättitutkimuksen Amerikan Sydänliiton aloitteesta, jossa mitattiin veren kolesteroliarvot lähes 137 000 sydänkohtauksen vuoksi sairaalahoitoa saaneelta potilaalta. Kaikki kolesteroliarvot olivat oletettuja pienempiä, jopa huomattavasti alle amerikkalaisten keskiarvon.
Emeriusprofessorit Matti Järvilehto Oulusta ja Pentti Tuohimaa Tampereelta kritisoivat Medical Hypotheses-lehden artikkelissaan kolesterolihoitoja. Medialle lähettämässään tiedotteessa he esittävät näkemyksensä, joka tukee täysin Erkki Antilan, Pentti Raasteen ja Matti Tolosen vuosia esittämiä näkemyksiä: ravinnon rasvat ja kolesteroli eivät ole valtimotautien syy ja kolesterolin alentaminen lääkkein on enimmäkseen turhaa ja jopa terveydelle haitallista.
Statiinien käyttäjillä D-vitamiinin vajauksen yhteydessä lähes kaikilla esiintyy lihas- ja sidekudoskipuja. Statiinit saattavat lisäksi heikentää D-vitamiinin vaikutusta syrjäyttämällä hoitopitoisuuksilla D-vitamiinin reseptoristaan.
Etusivun uutiseksi päätynyt Oxfordin yliopiston professori Rory Collins myöntää salanneensa tutkimuksissaan statiinien sivuvaikutuksia. Statiineista voi olla vakavaa haittaa sydänlihakselle kirjoittavat japanilaiset sydänlääkärit yhdessä amerikkalaisen kardiologin Peter Langsjoenin kanssa julkaisemassaan artikkelissa.
Vääristeltyjen tutkimusten perusteella miljoonat britit syövät statiineja turhaan. Collins johtaa vuonna 1994 perustettua Cholesterol Treatment Trialists (CTT) Collaborationia, jonka tutkimuksiin mm. Suomen Sydänliiton ylilääkäri Mikko Syvänne on vedonnut statiineja puolustaessaan.
Yli 20 tutkimusta osoittaa, että pisimpään elävät ne ihmiset, joiden veressä on riittävästi kolesterolia. Siis enemmän kuin 5 mmol/l, jota lääkärit pitävät lääkehoidon rajana.
Päivi Tirkkalan väitöskirjassa (2011)osoitettiin, että matalat kolesteroliarvot ovat yhteydessä kuolleisuuteen. Sen sijaan korkeat kolesterolitasot yli 74-vuotiailla eivät lisänneet sairastumisen tai kuoleman riskiä. Lisäksi kolesterolit ovat yhteydessä kognitiivisiin kykyihin. Matalat kolesterolitasot heikentävät muistia ja voivat aiheuttaa dementiaa.
Norjan HUNT2-tutkimuksessa seurattiin yli 50 000 20-74 vuotiasta henkilöä. 1,0 mmol/l kokonaiskolesterolin nousu naisilla vähensi kuolleisuutta 6 %, kun alle 5 mmol/l tasot lisäsivät kuoleman riskiä. Miehillä kuolleisuus oli pienintä, kun kolesteroli oli 5,0-5,9 mmol/l. Naisten kuoleman riski on 28 % pienempi, kun kokonaiskolesteroli on yli 7,0 mmol/l verrattuna arvoon alle 4,9 mmol/l.
Myös Pietarissa ja Honolulussa tehdyissä tutkimuksissa toistuu sama ilmiö: matala kolesteroli korreloi suurentuneen kuolemanriskin kanssa (Shestov ym. 1993, Schatz ym 2001). Kelan autoklinikkatutkimus tukee näitä tutkimuksia: sen mukaan miesten optimaalinen kolesterolitaso on 5-7 mmol/l ja naisilla vastaava suositus on 6-9 mmol/l.
Statiinit nostavat verensokeria ja lisäävät aikuistyypin diabeteksen riskiä keskimäärin 9-13 %, mutta naisilla riski kasvaa lähes 50 %. Suomalaiseen tutkimukseen osallistui 10 149 henkilöä, joilla oli suurentunut diabeteksen riski.
Amit Sachdeva ym. havaitsivat 136 905 potilaan tutkimusaineisossa, että akuutin sydänkohtauksen saaneiden potilaiden kolesteroli oli merkittävästi matalampi kuin samanikäisten terveiden verrokkien (American Heart Journal 2009).
Al-Mallah ym. totesivat, että ”pahan” LDL-kolesterolin pioisuudet olivat tavallista pienempiä ja kuolleisuus kaksin verroin yleisempää matalien LDL-lukemien potilailla (Cardiology Journal 2009). Nämä tutkimukset osoittavat, että seerumin kohonneen kolesterolipitoisuuden ja sydänkuoleman välillä ei vallitse kausaalisuhdetta.
Pohjoismaiden tunnetuin ja vaikutuvaltaisin ravitsemustieteilijä, tanskalainen professori Arne Astrup on muuttanut täysin mielipiteensä rasvoista ja kolesteroliteoriasta. Aikaisemmin hyvin kriittisesti tyydyttyneisiin rasvoihin suhtautunut Astrup kirjoitti vastattain maailman johtavan ravitsemuslääketieteen lehden pääkirjoituksessa, ettei tyydyttyneillä rasvoilla ole syy-yhteyttä sydän- ja verisuonitauteihin.
Astrupin kanssa samoilla linjoilla on myös professori Heikki Karppanen, joka sai melkoisesti kuraa niskaansa puhuessaan kolesteroliteoriaa vastaan.
Arne Astrup oli vannoutunut tyydyttyneiden rasvojen vastustaja ja hiilihydraattien puolestapuhuja. Vuonna 2013 Astrup siirtyi näkemykissään lähelle vähähiilihydraattisen ruokavalion periaatteita.
Hän myönsi julkisesti, ettei rasva ole vaarallista, kuten vuosikymmeniä on opetettu. Samaa sanoi myös professori Jussi Huttunen Suomessa. Nykyisin tiedetään, että elintasosairauksien taustalla ei ole välttämätön rasva, vaan hiilihydraattien liiallinen painottaminen ruokavaliossa.
Ryhmä tutkijoita Oaklandin lasten sairaalasta Kaliforniassa ja Harvardin kansanterveyslaitoksen ravitsemus- ja epidemiologian osastolta Bostonissa, Massachusettsissa, tekivät meta-analyysin prospektiivisista epidemiologisista tutkimuksista tyydyttyneiden rasvahappojen saannin ja sepelvaltimotauti-, aivohalvaus- tai sydän- ja verisuonitauti-riskin assosiaatiosta yleensä.
Prospektiivisissä epidemiologisissa tutkimuksissa seurataan ajan mittaan ryhmää alun perin terveitä ihmisiä, kohorttia, ja koetetaan selvittää, liittyykö taudin esiintyminen tiettyjen tunnistettavien tekijöiden toteutumiseen esim. ruokavalio- ja muut elämäntapatekijät. Meta-analyysissä kerätään ja analysoidaan yhdessä tiettyä aihetta koskevien eri tutkimusten tuloksia yleisen johtopäätöksen tekemiseksi kertyneen tieteellisen tiedon perusteella.
Kaksikymmentäyksi tutkimusta vastasi nykyisen meta-analyysin sisällyttämisperusteita. Yhdessä nämä käsittivät 347 747 henkilöä, joista noin 11 000 sairastui sydän- ja verisuonitauteihin.
Analyysin tulokset eivät osoittaneet merkittävää yhteyttä tyydyttyneiden rasvahappojen suuren saannin ja sepelvaltimotaudin, aivohalvauksen tai sydän- ja verisuonitautien lisääntyneen riskin välillä. Ikä, sukupuoli ja tutkimuksen laatu olivat tekijöitä, jotka otettiin huomioon analyysissä, mutta ne eivät vaikuttaneet tulokseen. Linkki
Prospektiivisten kohorttitutkimusten ja satunnaistettujen kontrolloitujen tutkimusten meta-analyysi tutki rasvahappojen ja sepelvaltimotaudin välistä yhteyttä. Tähän analyysiin tunnistettiin yhteensä 32 prospektiivista kohorttitutkimusta, jotka sisälsivät tietoja ruokavalion rasvahappojen saannista.
Analyysissä tutkittiin 530 525 osallistujaa. Tutkimus käsitti 15 907 sepelvaltimotautitapausta. Tutkimusten kesto oli 5–23 vuotta. Kirjoittajat tutkivat myös 17 havainnointitutkimusta, joissa oli tietoja kiertävästä rasvahappokoostumuksesta (ts. Rasvahapot veressä). Näihin tutkimuksiin osallistui 25721 osallistujaa, joista 5 519 johti sepelvaltimotautiin. Näissä tutkimuksissa seuranta oli 1,3-30,7 vuotta.
Tyydyttyneiden rasvahappojen kokonaissaantiin ei liittynyt sepelvaltimotaudin riskiä (yhdistetty suhteellinen riski 1,02, 95%:n luottamusväli: 0,97-1,07).
Kiertävien tyydyttyneiden rasvahappojen kokonaismäärään ei liittynyt sepelvaltimotaudin riskiä (yhdistetty suhteellinen riski 1,06, 95%: n luottamusväli: 0,86-1,30)
Yksittäisiin kiertäviin rasvahappoihin, kuten palmitiini- ja steariinihappoihin, ei myöskään liittynyt sepelvaltimotaudin riskiä.
Margariinihappoon (maitotuotteissa esiintyvä tyydyttynyt rasvahappo) liittyi merkittävästi pienempi sepelvaltimotaudin riski
Kirjoittajat päättelivät, että olemassaolevat todisteet eivät tue selvästi sydän- ja verisuonitautien suuntaviivoja, jotka suosivat tyydyttyneiden rasvojen korvaamista monityydyttämättömillä rasvoilla.
Toinen 26 kohorttitutkimuksen ameta-analyysi rvioi runsaasti tyydyttyneitä rasvoja sisältävien elintarvikkeiden ja kuolleisuuden riskin välistä yhteyttä. Runsas maidon, juuston, jogurtin ja voin saanti ei lisännyt sydän- ja verisuonitautiekuolleisuuden tai kaikkien syiden aiheuttaman kuolleisuuden riskiä matalaan saantiin verrattuna.
Runsaan maitotuotteiden, maidon ja juuston kokonaissaanti ei liittynyt sydän- ja verisuonikuolleisuuteen.
Vuoden 2010 meta-analyysi kohorttitutkimuksista, joka seurasivat 347747 ihmistä 5-23 vuoden aikana, toimitti seuraavat todisteet tyydyttyneen rasvan ja sepelvaltimotaudin, aivohalvauksen ja sydän- ja verisuonitautien välisestä yhteydestä:
Tyydyttyneiden rasvojen saanti ei liittynyt sepelvaltimotaudin, aivohalvauksen tai sydän- ja verisuonitautien lisääntyneeseen riskiin
Yhdistetyt suhteelliset riskit olivat 1,07 (95%: n luottamusväli: 0,96–1,19, p = 0,22) sepelvaltimotaudissa, 0,81 (95%: n luottamusväli: 0,62–1,05, p = 0,11) aivohalvauksessa ja 1,00 (95%: n luottamusväli: 0,89- 1,11, p = 0,95) sydän- ja verisuonitaudeissa.
Kovarianttien, kuten ikä, sukupuoli ja tutkimuksen laatu, mukauttamisen jälkeen tulokset eivät muuttuneet eikä merkittävää yhteyttä tyydyttyneiden rasvojen ja sydän- ja verisuonitautitapahtumien välillä havaittu.
Ruokavalion tyydyttyneiden rasvojen ja sairauksien esiintyvyyden välillä ei havaittu yhteyttä muiden ravintoaineiden ja kokonaisenergian mukauttamisen jälkeen.
Vuoden 2009 järjestelmällisessä katsauksessa toimitettiin seuraava yhteenveto mahdollisista kohorttitutkimuksista ja satunnaistetuista kontrolloiduista tutkimuksista:
Tyydyttyneiden rasvojen ja sepelvaltimotaudin kohorttitutkimusten meta-analyysin perusteella tyydyttyneiden rasvahappojen saanti ei liittynyt merkittävästi sepelvaltimotauditapahtumiin.
Suhteelliset riskit korkeimmalle verrattuna pienimpään tyydyttyneiden rasvojen saantiluokkaan olivat sepelvaltimotautikuolleisuuden osalta 1,14 (95%: n luottamusväli: 0,82–1,60, p = 0,431) ja 0,93 (95%: n luottamusväli: 0,83–1,05, p = 0,269). sepelvaltimotautitapahtumiin.
Tyydyttyneiden rasvojen ja kuoleman tai sydän- ja verisuonitautitapahtumien välillä ei ollut merkittävää yhteyttä tyydyttyneiden rasvahappojen saannin 5 prosentin kokonaisenergian lisäyksellä.
Ruokavalion rasvan ja sepelvaltimotaudin satunnaistettujen kontrolloitujen tutkimusten meta-analyysin perusteella kuolemaan johtavan sepelvaltimotaudin suhteellista riskiä ei vähennetty rasvamodifioiduilla ruokavalioilla.
Ruotsissa julkaistu väestötutkimus käsitti lähes kaksi miljoonaa miestä ja kaksi miljoonaa naista. Vuosina 1998–2002 määrätyt statiinit eivät olleet yhtään vähentäneet sydänkohtauksia eikä sydänkuolemia.
Tulos on yhdenmukainen Ray et. al. meta-analyysin kanssa (2010): Statiinien käyttö ei lisännyt elinikää satunnaistetuissa primaaripreventiotutkimuksissa, joihin oli osallistunut 65 229 ”suuren riskin” henkilöä. Analyysi käsitti 244 000 henkilövuotta ja 2793 kuolemantapausta.
Kelan ja Tilastokeskuksen tilastot kertovat samaa Suomesta: Statiinien jyrkästi lisääntynyt käyttö ei ole vähentänyt sydänkuolemia.
Amerikkalaiset lääkärit Hayward ja Krumholz kritisoivat LDL-kolesterolin saamaa liaallista huomiota hoidossa. Heidän mielestään pitäisi hoitaa todellisia risikitekijöitä, ei LDL:ää. ”On aika jättää hyvästit tälle vanhalle, perusteettomalle ja harhaanjohtavalle rasvateorialle”, kirjoittivat ruotsalaislääkärit.
Mitään kovin kummoista konsensusta kolesterolin ja tyydyttyneiden rasvojen yhteydestä sydän- ja verisuonitauteihin ei ole. Nykyisestä käytännöstä hyötyvät lääketeollisuus ja siihen sijoittaneet enemmän kuin kolesterolilääkkeitä ahmivat statinistit. Oma kantani on, että ihminen tarvitsee välttämättä kolesterolia ja sen laskeminen johtaa terveyden heikkenemiseen. Uskon, että sydän- ja verisuonitautien todellinen syypää on hyperglykemia ja hyperinsulinemia. Jokainen tehköön omat johtopäätöksensä.
Täydentävää materiaalia
https://cholesterolcode.com/a-simple-guide-to-cholesterol-on-low-carb-part-i/https://cholesterolcode.com/a-simple-guide-to-cholesterol-on-low-carb-part-ii/
https://ruokasota.fi/2020/11/20/ketogeeninen-ruokavalio-ja-epilepsia/
https://ruokasota.fi/2020/11/03/insuliini-ja-terveys-neljas-luku/
https://ruokasota.fi/2020/10/27/insuliini-ja-terveys-kolmas-luku/
https://ruokasota.fi/2020/10/20/insuliini-ja-terveys-hiilihydraatti-insuliinimalli/
https://ruokasota.fi/2020/09/01/ruokasotaa-ja-anarkiaa-osa-3/
https://ruokasota.fi/2020/08/23/mozaffarianin-meta-analyysin-kritiikki/
https://ruokasota.fi/2020/08/12/hammentavia-ruokajuttuja-osa-1/
https://ruokasota.fi/2020/10/11/insuliini-ja-terveys-johdanto/





