Ketogeeninen ruokavalio, sydän- ja verisuonitaudit 4: endoteeli, verenpaine ja paino
Endoteeli on ohut, yksinkertainen solukerros, joka verhoaa verisuonten sisäpintoja. Endoteeli säätelee veren virtausta, ravinteiden ja aineenvaihduntatuotteiden vaihtoa verenkierron ja ympäröivien kudosten välillä. Se ei kuitenkaan ole vain passiivinen este. Tulehdusreaktion aikana endoteelisoluista tulee aktiivisia, ja ne osallistuvat aktiivisesti immuunivasteen koordinointiin.
Endoteelisolut ovat verisuonten ja imusuonten sisäpintaa verhoavia soluja. Ne toimivat aktiivisina säätelijöinä ja välittäjinä verisuoniston, immuunijärjestelmän ja kudosten välillä. Endoteelisolut ovat tärkeitä sydän- ja verisuonijärjestelmän ja laajemmin koko kehon toiminnan ylläpitämisessä. Ne säätelevät verisuonten joustavuutta muun muassa tuottamalla typpioksidia, endoteliinia ja prostaglandiineja.
Endoteelisolut tuottavat erilaisia sytokiinejä ja adheesiomolekyylejä. Ne ovat keskeisiä immunoreaktiivisia soluja, ja niiden toimintahäiriö johtaa moniin patologisiin muutoksiin. Lisäksi niillä on erittäin tärkeä rooli monissa muissa prosesseissa [176,177].
|
Sytokiinit ovat pieniä proteiineja, jotka toimivat solujen välisinä viestinviejinä. Ne ovat kuin immuunijärjestelmän puhelinverkko, jolla solut viestivät keskenään. Esimerkiksi immuunisolut vapauttavat sytokiineja tulehdusalueelle ohjatakseen muita immuunisoluja paikalle. Tulehdusta edistäviä sytokiineja ovat esimerkiksi interleukiini-1 (IL-1), interleukiini-6 (IL-6) ja tuumorinekroositekijä alfa (TNF-α). Adheesiomolekyylit ovat proteiineja, jotka sijaitsevat solujen pinnoilla ja auttavat soluja kiinnittymään toisiinsa tai solunulkoiseen aineeseen. Tulehdusreaktion aikana endoteelisolut aktivoituvat sytokiinien vaikutuksesta ja alkavat ilmentää pinnallaan adheesiomolekyylejä, kuten selektiinejä ja integriinejä. Nämä molekyylit toimivat ”tarra-aineena”, jonka avulla verenkierrossa olevat immuunisolut, kuten neutrofiilit, pystyvät tarttumaan verisuonten seinämiin ja pääsemään tulehdusalueelle. Ilman adheesiomolekyylejä immuunisoluja ei pystyttäisi ohjaamaan tehokkaasti paikalle, missä niitä tarvitaan. |
Yhdessä endoteelisolut, sytokiinit ja adheesiomolekyylit mahdollistavat tulehdusreaktion oikeanlaisen käynnistymisen ja etenemisen. Endoteeli toimii alustana, sytokiinit antavat viestin, ja adheesiomolekyylit toteuttavat solujen liikkumisen sinne, missä tulehdus on.
Ketogeeninen ruokavalio vaikuttaa ketoaineiden kautta myös endoteelisoluihin
Nämä solut ovat läheisesti mukana ketoaineiden kuljetuksessa. Endoteelisolut pystyvät ottamaan ketoaineita vastaan ja käyttämään niitä ATP:n tuottamiseen, koska ne ilmentävät sukkinyyli-CoA:3-oksohappo-CoA-transferaasia (SCOT, joka on ketoaineita hapettava entsyymi).
Tämä havaittiin vuoden 2022 tutkimuksessa, joka vahvisti, että sydämen endoteelisolut kykenevät hapettamaan ketoaineita, mikä lisää proliferaatiota, solujen migraatiota ja verisuonten kasvua. Lisäksi sydämen hypertrofian hiirimallissa ketogeeninen ruokavalio esti vasodilataatiota. Tämän perusteella ketogeenisellä ruokavaliolla voi olla hyödyllinen rooli sydänsairauksissa [178].
Nasserin ym. tutkimus lisää näyttöä ketoaineiden suojaavasta vaikutuksesta. Ketoaineiden (pääasiassa BHB) alhaisina pitoisuuksina (saavutettavissa ketogeenisellä ruokavaliolla) on osoitettu parantavan endoteelin ja verisuonten toimintaa aineenvaihduntasairauksissa.
Diabeettisesta ketoasidoosista johtuvien liiallisten ketoaineiden on todettu vaikuttavan diabeettiseen vaskulopatiaan ja diabeteksen verisuonikomplikaatioihin.
Diabeettisen ketoasidoosin tiedetään kuitenkin esiintyvän samanaikaisesti ketoaineiden ja glukoosin liiallisten pitoisuuksien kanssa, eikä tällaisia korkeita ketoainepitoisuuksia yleensä saavuteta ketogeenisellä ruokavaliolla. Ketoasidoosia sairastavilla diabeetikoilla on riski paitsi verisuonikomplikaatioille, myös niiden seurauksena aiheutuvalle kuolemalle [179,180,181].
Endoteelisolujen merkitys:
Vasodilataatio ja vasokonstriktio:
Endoteelisolut tuottavat typpioksidia (NO), prostasykliiniä ja endoteeliiniä, jotka säätelevät verisuonten laajenemista ja supistumista. Typpioksidi on tärkeä verenpaineen laskijana ja verisuonten joustavuuden ylläpitäjänä. Endoteeli estää normaalisti verihiutaleiden tarttumista ja hyytymien muodostumista.
Vaurioituessaan endoteeli altistaa trombien (verihyytymien) synnylle. Se erittää sekä hyytymistä estäviä (esim. hepariini, prostasykliini) että hyytymistä edistäviä tekijöitä tarpeen mukaan.
Tulehdus ja immuunivaste
Endoteelisolut säätelevät valkosolujen kiinnittymistä ja kulkua verisuoniseinämän läpi kudoksiin (adheesiomolekyylit, kuten ICAM-1, VCAM-1). Ne vapauttavat sytokiineja ja kemokiineja, jotka ohjaavat immuunivastetta.
Aineiden vaihto
- Endoteeli toimii puoliläpäisevänä suodattimena verisuoniston ja kudosten välillä.
- Sen kautta kulkee ravinteita, hormoneja ja kaasuja (happi, hiilidioksidi).
- Endoteelin läpäisevyyttä säädellään tarkasti, mutta esimerkiksi tulehduksessa se lisääntyy (turvotus).
Angiogeneesi (uusien verisuonten kasvu)
Endoteelisolut jakaantuvat ja muodostavat uusia kapillaareja esimerkiksi haavan paranemisessa ja kudosten hapenpuutteen yhteydessä. Tämä prosessi on tärkeä myös kasvainten kasvulle.
Elimistön homeostaasi ja aineenvaihdunta
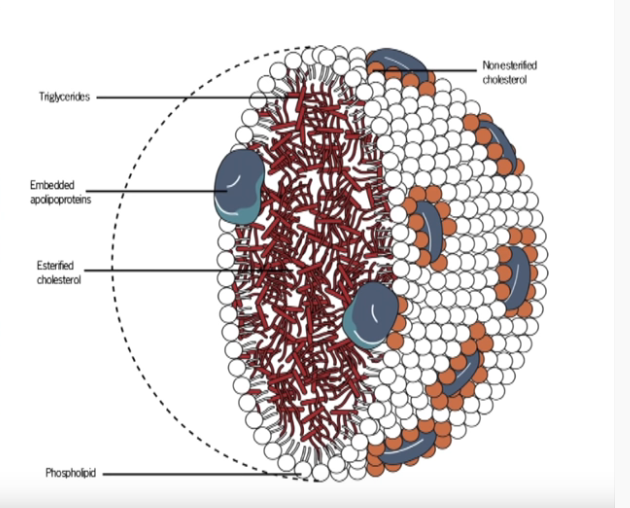
Endoteeli osallistuu mm. lipoproteiinien käsittelyyn ja verenkierron hormonien hajottamiseen. Sillä on rooli insuliiniherkkyydessä ja energiatasapainossa.
Endoteelivaurio on keskeinen tekijä valtimonkovettumataudissa (ateroskleroosissa). Endoteelin toimintahäiriö (endoteliaalinen dysfunktio) liittyy verenpainetautiin, diabetekseen, sydäninfarktiin ja aivohalvaukseen. Myös COVID-19 on osittain vaurioituneen endoteelin sairaus, koska virus ja tulehdus kohdistuvat verisuonistoon.
Ketogeeninen ruokavalio ja verisuonten endoteeli
Ravitsemuksellisen ketoosin pitoisuuksilla ketoaineet vaikuttavat suoraan verisuonten endoteelimodulaatioon, ja niillä on muun muassa tulehdusta estäviä vaikutuksia endoteelissa [97].
Gormsen ym. osoittivat, että Na-3-hydroksibutyraatti-infuusion tuottama hyperketonemia lisäsi sydänlihaksen verenvirtausta jopa 75 % ja sykettä noin 25 %. Tutkijat päättelivät, että ketoaineet vähentävät sydänlihaksen glukoosinottoa ja lisäävät sydänlihaksen verenvirtausta. He päättelivät, että ketoaineet ovat tärkeitä vasodilataattoreita ja tärkeä polttoaine sydämelle. Tämä vaikuttaa ketoaineiden terapeuttiseen potentiaaliin sydän- ja verisuonisairauksissa [155].
Toinen satunnaistettu kontrolloitu tutkimus osoitti, että 3-hydroksibutyraatti-infuusio lisäsi sydämen minuuttitilavuutta 2 l/min (40 %) ja vasemman kammion ejektiofraktio parani absoluuttisesti (8 %). Tutkimuksessa havaittiin vaikutus vasodilataatioon. Tähän liittyi vakaa systeeminen ja keuhkopaine [167].
Eläintutkimuksessa havaittiin ketogeenisen ruokavalion vaikutuksesta lisääntynyttä endoteelin typpioksidisyntaasin (eNOS) proteiinin ilmentymistä. Tutkimuksen tekijät päättelivät, että KD voi muiden tekijöiden ohella parantaa aivoverisuonten toimintaa parantaen aineenvaihduntaprofiilia, lisäämällä suotuisaa suoliston mikroflooraa ja vähentämällä Alzheimerin taudin riskiä [182].
McCarthyn ym. tutkimus osoitti, että BHB stimuloi endoteelista peräisin olevien tekijöiden tuotantoa. Itse asiassa 1,3-butaanidiolin (BHB:n esiasteen) infuusio lisäsi typpioksidisyntaasin aktiivisuutta. Kirjoittajat arvelivat, että pienet BHB-pitoisuudet voivat tarjota uuden hoidon verenpainetaudista johtuvaan verisuonten ikääntymiseen lisäämällä typpioksidin synteesiä [183].
On myös olemassa näyttöä ketoaineiden suojaavista vaikutuksista verisuonten ikääntymisen aiheuttamilta vaurioilta. BHB:n on osoitettu vähentävän ikääntymiseen ja verisuonisolujen vanhenemiseen liittyvää sekretorista fenotyyppiä nisäkkäillä [184].
Hanin ym. tutkimuksen tulokset huomioivat, että BHB edistää verisuonisolujen lepotilaa ja että tämä estää merkittävästi stressin aiheuttamaa ennenaikaista ikääntymistä ja replikatiivista ikääntymistä p53-riippumattomien mekanismien kautta. Muiden vaikutusten ohella tämä lisäsi Oct4:n ja B1-lamiinin ilmentymistä sekä verisuonten sileissä lihaksissa että endoteelisoluissa hiirillä. Kirjoittajat päättelivät, että BHB:llä oli ikääntymistä estäviä vaikutuksia verisuonisoluissa hnRNP A1:n indusoiman B1-lamiinireitin lisääntyneen ilmentymisen kautta, jota Oct4 välittää [185].
Meronin ym. työn tulokset viittaavat siihen, että ketogeeninen ruokavalio, jota välittää kohtalaisen oksidatiivisen stressin indusointi, aktivoi transkriptiotekijä Nrf2:n. Tämä tekijä puolestaan indusoi solujen antioksidanttipuolustusjärjestelmään osallistuvien kohdegeenien transkriptiota [186]. Myös glukoosi- ja HbA1c-tasot laskevat ketogeenisessä ruokavaliossa. Verisuonten endoteelisolujen krooninen altistuminen korkeille glukoosipitoisuuksille johtaa useiden tulehdusta edistävien ja ateroskleroottisten geenien ilmentymisen lisääntymiseen [187].
Glukoosia alentava mekanismi on toinen tekijä, joka suosii verisuonten endoteelin toimintaa. On kuitenkin myös raportteja, jotka viittaavat endoteelin toiminnan heikkenemiseen KD:llä. Coppola ym. osoittivat lisääntynyttä valtimoiden jäykkyyttä KD:llä hoidetuilla epilepsiaa sairastavilla lapsilla [188].
Toinen tutkimus osoitti, että sydän- ja verisuonitautien riski voi olla lisääntynyt, mutta vain erittäin vähähiilihydraattisen ruokavalion ensimmäisten päivien aikana [189].
Suurin osa tutkimuksesta keskittyy edelleen eksogeenisten ketonien vaikutukseen, ei ketogeeniseen ruokavalioon. Valtaosa tutkimusnäytöstä viittaa ketogeenisen ruokavalion ja sen kautta indusoitujen ketoaineiden hyödyllisiin vaikutuksiin verisuonten endoteelin toiminnassa. Ketogeenisen ruokavalion vaikutukset verisuonten endoteeliin on esitetty kuvassa 2.
Kuva 2.
Ketogeenisen ruokavalion vaikutus verenpaineeseen
Entä miten ketogeeninen ruokavalio vaikuttaa verenpaineeseen? On olemassa useita mekanismeja, joilla KD pystyy vaikuttamaan tähän parametriin. Tiedetään, että ketogeeninen ruokavalio laskee insuliinipitoisuuksia, koska se sisältää vähän hiilihydraatteja [82].
Insuliini vastaa natriumin pidättymisestä elimistöön stimuloimalla sen takaisinimeytymistä. Tämä liittyy myös nesteen pidättymiseen elimistössä.
Insuliinipitoisuuden laskiessa veden ja natriumin poistuminen elimistöstä lisääntyy. Tämä johtaa muiden elektrolyyttien, kuten kaliumin, poistumiseen virtsan mukana. Myös magnesiumin ja kalsiumin määrä voi vähentyä. Elektrolyyttihäviötä tapahtuu vain ketogeenisen ruokavalion ensimmäisen jakson aikana (ensimmäinen viikko) ja se johtuu luonnollisesta sopeutumisesta ketoosiin. Tiedetään, että riittävät elektrolyyttitasot ovat olennainen tekijä normaalin verenpaineen ylläpitämisessä [190, 191, 192, 193, 194, 195, 196].
Verisuonten endoteelilla on tärkeä vaikutus verenpaineeseen, johon ketogeeninen ruokavalio voi vaikuttaa. Lisäksi ketogeeninen ruokavalio voi vaikuttaa suotuisasti hypotalamus-aivolisäke-lisämunuais (HPA) -akseliin ja sympaattiseen hermostoon (SNS) [197, 198, 199,200].
Toinen mahdollinen verenpainevaikutuksen mekanismi voi olla ketogeenisen ruokavalion vaikutus reniini-angiotensiini-aldosteroni (RAA) -järjestelmään, kuten kahdessa vuoden 2023 julkaisussa on havaittu [201,202].
Painonpudotus on tärkeä mekanismi, joka liittyy ketogeenisen ruokavalion verenpainevaikutukseen. Ketogeenisen ruokavalion kanssa samanaikaisesti toteutuva kalorivaje ja itse painonpudotus (ja kehon koostumuksen paraneminen) voivat epäsuorasti parantaa verenpaineparametreja [203,204,205].
Vuonna 2021 julkaistun tutkimuksen kirjoittajat osoittavat, että ketogeeninen ruokavalio voi alentaa verenpainetta, mutta se ei aiheuta merkittäviä muutoksia verrattuna ei-ketogeenisiin ruokavalioihin. Tutkijat osoittavat, että tämä johtuu suurelta osin painon- ja rasvanpoltosta sekä sydän- ja verisuonitautien riskiparametrien paranemisesta [203,204,205].
Vuonna 2023 julkaistussa tutkimuksessa, jossa tutkittiin erittäin vähäkalorisen ketogeenisen ruokavalion (VLCKD) vaikutusta lihaviin ja korkean verenpaineen omaaviin naisiin, havaittiin, että tällä ruokavaliolla sekä systolinen että diastolinen verenpaine paranivat merkittävästi (−12,89 % ja −10,77 %; p < 0,001).
|
Ennen ruokavaliointerventiota keskimääräinen systolinen verenpaine oli 140,88 ± 8,99 mmHg ja diastolinen verenpaine 88,90 ± 6,71 mmHg. 45 päivän ketogeenisen ruokavalion jälkeen systolinen verenpaine laski keskimäärin 122,56 ± 10,08 mmHg:iin ja diastolinen verenpaine keskimäärin 78,94 ± 6,68 mmHg:iin. |
Kirjoittajat päättelivät, että erittäin vähäkalorinen ketogeeninen ruokavalio alensi turvallisesti verenpainetta lihavilla verenpainetautia (hypertensio) sairastavilla naisilla [206]. Merkittävää on, että verenpaineen lasku johtui pääasiassa kalorien puutteesta, painonpudotuksesta ja vyötärön ympärysmitasta, eikä niinkään itse ruokavaliosta. On todennäköistä, että vastaava vaikutus voitaisiin saavuttaa käyttämällä samaa kalorialijäämää tasapainoisessa tavanomaisessa ruokavaliossa.
Toinen 2023 tehty tutkimus osoitti, että VLCKD alensi tehokkaasti verenpainetta alkoholista riippumatonta rasvamaksaa (NAFLD) sairastavilla potilailla 8 viikon aikana. Keskimääräinen systolinen verenpaine laski arvosta 133,51 ± 12,86 mmHg arvoon 123,27 ± 10,51 mmHg ja diastolinen verenpaine arvosta 81,73 ± 8,09 mmHg arvoon 75,27 ± 7,84 mmHg [207].
2022 toteutetussa satunnaistetussa kontrolloidussa tutkimuksessa ketogeeninen ruokavalio yhdessä jatkuvan positiivisen hengitystiepaineen (CPAP) kanssa alensi systolista ja diastolista verenpainetta enemmän (142,8 ± 13,3 mmHg:stä 133 ± 11,9 mmHg:iin ja 85,4 ± 8,38 mmHg:stä 78,7 ± 6,43 mmHg:iin) kuin pelkkä CPAP-hoito (134,2 ± 10,4 mmHg:stä 130 ± 9,7 mmHg:iin ja 87 ± 11,6 mmHg:stä 82 ± 9,5 mmHg:iin) potilailla, joilla oli vaikea obstruktiivinen uniapneaoireyhtymä.
Toisessa satunnaistetussa kontrolloidussa tutkimuksessa verrattiin eri ketogeenisten ruokavalioiden vaikutuksia lihavuudesta ja insuliiniresistenssistä kärsivien potilaiden parametrien perusteella. Siinä havaittiin, että verenpaine laski merkittävästi jokaisessa ketogeenisessä ruokavalioryhmässä.
|
Systolinen verenpaine muuttui keskimäärin WPG-ryhmässä 132 ± 10 mmHg:stä 124 ± 13 mmHg:iin, VPG-ryhmässä 131 ± 8 mmHg:stä 121 ± 10 mmHg:iin ja APG-ryhmässä 129 ± 9 mmHg:stä 121 ± 16 mmHg:iin. Diastolinen paine laski WPG-ryhmässä keskimäärin 78 ± 11 mmHg:stä 70 ± 9 mmHg:iin, VPG-ryhmässä 78 ± 10 mmHg:stä 72 ± 10 mmHg:iin ja APG-ryhmässä 78 ± 10 mmHg:stä 71 ± 9 mmHg:iin. |
Satunnaistetussa tutkimuksessa Saslow ym. tutkivat kohtalaisen tai hyvin vähähiilihydraattisen ruokavalion vaikutusta ylipainoisiin aikuisiin, joilla on tyypin 2 diabetes tai esidiabetes. He havaitsivat kuitenkin, ettei ryhmien välillä ollut selviä eroja: Taulukko 2.
Toinen satunnaistettu kontrolloitu tutkimus osoitti, että ketogeenisen ruokavalion ja hypokalorisen ruokavalion vaikutukset verenpaineeseen eivät eronneet merkittävästi.
|
Ketogeenistä ruokavaliota noudattavien keskimääräinen systolinen verenpaine laski 110 ± 13 mmHg:stä 108 ± 13 mmHg:iin, kun taas diastolinen verenpaine nousi keskimäärin 66 ± 10 mmHg:stä 68 ± 8 mmHg:iin. Hypokalorista ruokavaliota noudattaneilla havaittiin systolisen verenpaineen ei-merkitsevä lasku 107 ± 9 mmHg:stä 106 ± 11 mmHg:iin ja diastolisen verenpaineen keskimäärin 65 ± 10 mmHg:stä 62 ± 11 mmHg:iin. |
Yancy ym. vertasivat myöhemmässä satunnaistetussa kontrolloidussa tutkimuksessa ketogeenisen ruokavalion, vähärasvaisen ruokavalion ja orlistaattihoidon (tuolloin lihaville potilaille käytetty lääke) yhdistelmän vaikutuksia eri parametreihin, kuten painoon, verenpaineeseen, seerumin lipiditasoihin paastoarvoissa ja glykeemisiin parametreihin. Osoitettiin, että ketogeenistä ruokavaliota noudattaneilla oli parempia tuloksia, mukaan lukien verenpaine.
48 viikon aikana keskimääräinen systolinen verenpaine laski −5,94 mmHg (−1,5 mmHg LFD + O -ryhmässä) ja diastolinen verenpaine laski −4,53 mmHg (−0,43 mmHg LFD + O -ryhmässä) [208].
Vähähiilihydraattisten ja vähärasvaisten ruokavalioiden vertailututkimuksissa on aiheellista viitata Fosterin ym. suorittamaan satunnaistettuun kontrolloituun tutkimukseen.
Tutkimus osoitti, että vähähiilihydraattinen ruokavalio alensi verenpainetta tehokkaammin kuin vähärasvainen ruokavalio. Havaittiin, että jokaisessa vaiheessa (3, 6, 12 ja 24 kuukautta) diastolinen verenpaine laski enemmän (2–3 mmHg) vähähiilihydraattista ruokavaliota noudattaneessa ryhmässä. Systolisen verenpaineen laskussa ei ollut suuria eroja ryhmien välillä, vaikka 3, 6, 12 ja 24 kuukauden kuluttua lasku oli edelleen suurempi vähähiilihydraattisessa ryhmässä [209].
Toinen satunnaistettu kontrolloitu tutkimus osoitti, että ketogeenisellä ruokavaliolla (enintään 30 g hiilihydraatteja päivässä) ilman kalorirajoitusta oli sama ei-merkitsevä vaikutus verenpaineen alenemiseen kuin ruokavaliolla, jossa oli kalorivaje ja rasvan saanti jopa 30 % energiasta [210]. Tämä tutkimus osoitti myös, että kalorivaje itsessään ei ollut tärkein verenpaineparametreihin vaikuttava tekijä.
Pilottikokeessa Tzenios ym. osoittivat, että 140 päivän aikana ketogeeninen ruokavalio alensi systolista verenpainetta 5,3 % lähtötasosta. Kirjoittajat raportoivat myös merkittävästä diastolisen verenpaineen noususta päivänä 28; merkittäviä muutoksia ei kuitenkaan havaittu päivinä 56, 70, 84, 112 ja 140 [211].
Voimme myös huomioida Castellanin ym. meta-analyysin tulokset, joissa kirjoittajat osoittivat, että VLCKD liittyi systolisen verenpaineen keskimääräiseen 9 mmHg:n ja diastolisen verenpaineen laskuun 7 mmHg:n verran, ja lisäksi sillä oli merkittäviä vaikutuksia painoindeksin (BMI) (−5,3 kg/m2), vyötärön ympärysmitan (−12,6 cm), HbA1c:n (−0,7 %), kokonaiskolesterolin (−28 mg/dl), triglyseridien (−30 mg/dl) ja maksaentsyymien laskuun.
Toisessa meta-analyysissä kirjoittajat vertasivat KD:n vaikutusta vähärasvaiseen ruokavalioon muun muassa verenpaineen muutosten osalta. He havaitsivat, että ketogeeninen ruokavalio alensi diastolista verenpainetta tehokkaammin (WMD — 1–43 (95 %:n luottamusväli — 2–49, 0–37) mmHg), kun taas systolisessa verenpaineessa eroja havaittiin vähemmän (WMD VLCKD:n eduksi — 1–47 (95 %:n luottamusväli — 3–44, 0–50) mmHg) [212]. Kaikki kuvatut tutkimukset on esitetty julkaisussa: Taulukko 2.
Taulukko 2.
Ketogeenisen ruokavalion vaikutus verenpaineeseen.
Nykyisten tutkimusten tulokset huomioon ottaen voidaan epäilemättä päätellä, että ketogeenisellä ruokavaliolla on hyödyllinen vaikutus verenpainearvoihin. Sen lisäksi, että ketogeenisellä ruokavaliolla on samanlainen tehokas verenpainetta alentava vaikutus kuin muillakin painonpudotustoimenpiteillä, sillä näyttää olevan jonkin verran etua tässä suhteessa, eikä se johdu pelkästään painonpudotuksesta.
in this regard.
7. Ketogeeninen ruokavalio; painonpudotus sydän- ja verisuonitautien ehkäisyssä ja hoidossa
Ketogeenistä kalorivajeruokavaliota käytetään usein painon pudottamiseen. Luonteensa vuoksi se on monille ihmisille tehokkaampi painonpudotusstrategia kuin tavanomaiset kalorirajoitteiset ruokavaliot.
Kun otetaan huomioon, että lihavuus on yksi sydän- ja verisuonitautien ensisijaisista riskitekijöistä, painonpudotus itsessään vähentää merkittävästi sydän- ja verisuonitautien riskiä.
Lihavuus on siis samanaikaisesti muiden riskitekijöiden, kuten huonon ruokavalion ja fyysisen passiivisuuden, vaikutusta, mutta samalla se on keskeinen riskitekijä itsessään [1,6,59,213,214].
Lihavuus vaikuttaa muihin riskitekijöihin, kuten esimerkiksi dyslipidemiaan, verenpainetautiin, tyypin 2 diabetekseen ja unihäiriöihin. Myös lisääntynyttä vyötärön ympärysmittaa voidaan pitää itsenäisenä sydän- ja verisuonitautien riskitekijänä, joka ei riipu painoindeksistä.
Viskeraalinen lihavuus on sydän- ja verisuonitautien yksi indikaattori ja se on yhdistetty haitallisiin sydän- ja verisuonitautitapahtumiin. Painon pudottaminen parantaa sydämen ja verisuonten toimintaa, mikä johtaa sydän- ja verisuonitautien riskin vähenemiseen [215].
Ketogeeninen ruokavalio parantaa sydän- ja verisuonitautien riskitekijöitä ja laskee painoa (usein tärkein syy ketogeenisen ruokavalion noudattamiseen). Siten se vähentää lihavuuden/ylipainon riskitekijöitä ja samalla mitätöi muita ylipainosta johtuvia riskitekijöitä.
Bueno et al.:n meta-analyysi osoitti, että ketogeeninen ruokavalio voi olla tehokkaampi vaihtoehto pitkäaikaiseen painonpudotukseen (ja joidenkin sydän- ja verisuonitautien riskitekijöiden parantamiseen) verrattuna vähärasvaisiin ruokavalioihin [212].
Ketogeenisten ruokavalioiden paremmuus vähärasvaisiin ruokavalioihin verrattuna osoitettiin myös Choi et al.:n meta-analyysissä. Vähärasvaisiin ruokavalioihin verrattuna ketogeeninen ruokavalio oli tehokkaampi parantamaan aineenvaihduntaparametreja, jotka liittyvät muun muassa painoon, lipidiprofiiliin ja glykeemiseen hallintaan ylipainoisilla potilailla (ylipainoa tai lihavuutta), erityisesti diabeetikoilla [125].
Näyttää siltä, että ketogeeninen ruokavalio ei ole ainoastaan tehokas painonpudotuksessa, vaan myös turvallinen noudattaa.
Tämän vahvistavat toisen meta-analyysin tulokset. Tämän huomioon ottaen painonpudotus on toinen tekijä, jonka ansiosta ketogeenisellä ruokavaliolla voi olla ennaltaehkäisevää ja terapeuttista potentiaalia sydän- ja verisuonisairauksissa.
8. Ketogeenisen ruokavalion vaikutus terveillä ja sydän- ja verisuonitautipotilailla
Joissakin tutkimuksissa ketogeenisen ruokavalion hyödyt sydän- ja verisuonitautipotilailla ovat merkittävämpiä kuin terveillä ja fyysisesti aktiivisilla ihmisillä.
Erot voivat johtua tietyistä mekanismeista. Ensinnäkin monet sydän- ja verisuonitautia sairastavat ovat ylipainoisia tai lihavia (mikä on paljon harvinaisempaa terveillä ihmisillä), joten sydän- ja verisuonitautia sairastavilla havaitaan suurempi painonpudotusvaikutus. Painonpudotus parantaa merkittävästi sydän- ja verisuonitautiriskiin liittyviä parametreja [215]. Tämä on osoitettu monissa tutkimuksissa, kuten Li ym., Schiavo ym. ja Michalczyk ym. julkaisuissa, joissa ketogeenistä ruokavaliota noudattaneet ihmiset laihtuivat merkittävästi enemmän kuin kontrolliryhmä, mikä paransi sellaisten parametrien arvoja kuin kokonaiskolesteroli, LDL, HDL ja triglyseridit.
Toinen mekanismi on se, että sydän- ja verisuonitautia sairastavilla ihmisillä on usein määritelmän mukaan epänormaali lipidiprofiili. Tällaista ei esiinny yhtä paljon terveillä ja fyysisesti aktiivisilla ihmisillä.
Esimerkiksi eräässä tutkimuksessa terveillä, nuorilla ja koulutetuilla naisilla KD-ruokavalio ei parantanut lipidiprofiileja. Kirjoittajat havaitsivat päinvastoin lipidiprofiilien heikkenemistä, mikä on toisaalta ristiriidassa useiden muiden tutkimusten kanssa, joissa ketogeeninen ruokavalio alensi sydän- ja verisuonitautien riskitekijöitä sekä ylipainoisilla että normaalipainoisilla potilailla.
Toinen argumentti ketogeenisen ruokavalion suuremmille hyödyille sydän- ja verisuonitautia sairastavilla tai riskiryhmään kuuluvilla ihmisillä on nykyisen ruokavalion koostumus.
Näiden ihmisten ruokavalion koostumus on usein sopimaton, erityisesti monien runsaasti prosessoitujen tuotteiden sisällön osalta. Länsimainen ruokavalio pahentaa sydän- ja verisuonitautien riskitekijöitä ja lisää siten sairastumisriskiä. Siirtyminen vähän prosessoituun tai prosessoimattomaan ruokavalioon (jonka yleensä tulisi olla ketogeeninen ruokavalio) laskee usein tätä riskiä.
Esimerkiksi tutkimus, jossa verrattiin prosessoimattoman ketogeenisen ruokavalion omaksumista länsimaisen ravitsemusmallin jatkamiseen. Ketogeeniseen ruokavalioon siirtyneet naiset paransivat merkittävästi yleistä terveydentilaansa ja sydän- ja verisuonitautien riskitekijöitä.
Toinen tärkeä mekanismi on se, että terveillä ihmisillä ketoaineiden vaikutus ei välttämättä ole yhtä merkittävää sydämen toimintaan, koska, kuten on toistuvasti osoitettu, sydänsolut lisäävät ketoaineiden ottoa vain heikentyneen aineenvaihdunnan yhteydessä, mitä esiintyy sydän- ja verisuonitautia sairastavilla ihmisillä [146,147,150,151,152,153,163].
Eräs vaikuttava mekanismi voi olla vaikutus itse verisuonten endoteeliin. Terveillä ihmisillä, joilla ei ole ongelmia endoteelin tulehduksen kanssa, on myös vaikea määrittää muun muassa ketoaineiden mahdollisia hyötyjä. Sydän- ja verisuonitautia sairastavat potilaat kamppailevat usein kroonisen endoteelin tulehduksen kanssa, jota tutkimusten mukaan voidaan vähentää nostamalla ketoaineiden määrää ketogeenisellä ruokavaliolla saavutettavalle tasolle [97,155].
Endoteelin tulehdukseen vaikuttavien tekijöiden, kuten glukoosin, glykoituneen hemoglobiinin ja insuliinipitoisuuksien vähentäminen osoittaa eroja ruokavalion vaikutuksista sydän- ja verisuonitautia sairastavilla ja terveillä ihmisillä.
Kirjoittajat: Damian Dyńka , Katarzyna Kowalcze , Anna Charuta , Agnieszka Paziewska ,*
Alkuperäinen artikkeli: https://pmc.ncbi.nlm.nih.gov/articles/PMC10421332/
Käännös & editointi: Sami Raja-Halli
Lähdeluettelo
176.Galley H.F., Webster N.R. Physiology of the endothelium. Br. J. Anaesth. 2004;93:105–113. doi: 10.1093/bja/aeh163. [DOI] [PubMed] [Google Scholar]
177.Nappi F., Fiore A., Masiglat J., Cavuoti T., Romandini M., Nappi P., Avtaar Singh S.S., Couetil J.-P. Endothelium-Derived Relaxing Factors and Endothelial Function: A Systematic Review. Biomedicines. 2022;10:2884. doi: 10.3390/biomedicines10112884. [DOI] [PMC free article] [PubMed] [Google Scholar]
178.Weis E.M., Puchalska P., Nelson A.B., Taylor J., Moll I., Hasan S.S., Dewenter M., Hagenmüller M., Fleming T., Poschet G., et al. Ketone body oxidation increases cardiac endothelial cell proliferation. EMBO Mol. Med. 2022;14:e14753. doi: 10.15252/emmm.202114753. [DOI] [PMC free article] [PubMed] [Google Scholar]
179.Devaraj S., Cheung A.T., Jialal I., Griffen S.C., Nguyen D., Glaser N., Aoki T. Evidence of increased inflammation and microcirculatory abnormalities in patients with type 1 diabetes and their role inmicrovascular complications. Diabetes. 2007;56:2790–2796. doi: 10.2337/db07-0784. [DOI] [PMC free article] [PubMed] [Google Scholar]
180.White N.H. Diabetic ketoacidosis in children. Endocrinol. Metab. Clin. North Am. 2000;29:657–682. doi: 10.1016/S0889-8529(05)70158-4. [DOI] [PubMed] [Google Scholar]
181.Bialo S.R., Agrawal S., Boney C.M., Quintos J.B. Rare complications of pediatric diabetic ketoacidosis. World J. Diabetes. 2015;6:167–174. doi: 10.4239/wjd.v6.i1.167. [DOI] [PMC free article] [PubMed] [Google Scholar]
182.Ma D., Wang A.C., Parikh I., Green S.J., Hoffman J.D., Chlipala G., Murphy M.P., Sokola B.S., Bauer B., Hartz A.M.S., et al. Ketogenic diet enhances neurovascular function with altered gut microbiome in young healthy mice. Sci Rep. 2018;8:6670. doi: 10.1038/s41598-018-25190-5. [DOI] [PMC free article] [PubMed] [Google Scholar]
183.Mccarthy C.G., Chakraborty S., Schreckenberger Z., Wenceslau C.F., Joe B. β-hydroxybutyrate (βHOB) increases nitric oxide synthase activity in resistance arteries from dahl salt-sensitive rats. FASEB J. 2019;33:829. doi: 10.1096/fasebj.2019.33.1_supplement.829.1. [DOI] [Google Scholar]
184.Newman J.C., Covarrubias A.J., Zhao M., Yu X., Gut P., Ng C.P., Huang Y., Haldar S., Verdin E. Ketogenic Diet Reduces Midlife Mortality and Improves Memory in Aging Mice. Cell Metab. 2017;26:547–557.e8. doi: 10.1016/j.cmet.2017.08.004. [DOI] [PMC free article] [PubMed] [Google Scholar]
185.Han Y.M., Bedarida T., Ding Y., Somba B.K., Lu Q., Wang Q., Song P., Zou M.H. β-Hydroxybutyrate Prevents Vascular Senescence through hnRNP A1-Mediated Upregulation of Oct4. Mol Cell. 2018;71:1064–1078.e5. doi: 10.1016/j.molcel.2018.07.036. [DOI] [PMC free article] [PubMed] [Google Scholar]
186.Meroni E., Papini N., Criscuoli F., Casiraghi M.C., Massaccesi L., Basilico N., Erba D. Metabolic Responses in Endothelial Cells Following Exposure to Ketone Bodies. Nutrients. 2018;10:250. doi: 10.3390/nu10020250. [DOI] [PMC free article] [PubMed] [Google Scholar]
187.Pirola L., Balcerczyk A., Tothill R.W., Haviv I., Kaspi A., Lunke S., Ziemann M., Karagiannis T., Tonna S., Kowalczyk A., et al. Genome-wide analysis distinguishes hyperglycemia regulated epigenetic signatures of primary vascular cells. Genome Res. 2011;21:1601–1615. doi: 10.1101/gr.116095.110. [DOI] [PMC free article] [PubMed] [Google Scholar]
188.Coppola G., Natale F., Torino A., Capasso R., D’Aniello A., Pironti E., Santoro E., Calabrò R., Verrotti A. The impact of the ketogenic diet on arterial morphology and en-dothelial function in children and young adults with epilepsy: A case-control study. Seizure. 2014;23:260–265. doi: 10.1016/j.seizure.2013.12.002. [DOI] [PubMed] [Google Scholar]
189.Buscemi S., Verga S., Tranchina M.R., Cottone S., Cerasola G. Effects of hypocaloric very-low-carbohydrate diet vs. Mediterranean diet on endothelial function in obese women. Eur. J. Clin. Investig. 2009;39:339–347. doi: 10.1111/j.1365-2362.2009.02091.x. [DOI] [PubMed] [Google Scholar]
190.DeFronzo R.A. The effect of insulin on renal sodium metabolism. A review with clinical implications. Diabetologia. 1981;21:165–171. doi: 10.1007/BF00252649. [DOI] [PubMed] [Google Scholar]
191.Brands M.W. Role of Insulin-Mediated Antinatriuresis in Sodium Homeostasis and Hypertension. Hypertension. 2018;72:1255–1262. doi: 10.1161/HYPERTENSIONAHA.118.11728. [DOI] [PubMed] [Google Scholar]
192.Palmer B.F., Clegg D.J. Physiology and pathophysiology of potassium homeostasis. Adv. Physiol. Educ. 2016;40:480–490. doi: 10.1152/advan.00121.2016. [DOI] [PubMed] [Google Scholar]
193.Harvey C.J.D.C., Schofield G.M., Williden M. The use of nutritional supplements to induce ketosis and reduce symptomsassociated with keto-induction: A narrative review. PeerJ. 2018;6:e4488. doi: 10.7717/peerj.4488. [DOI] [PMC free article] [PubMed] [Google Scholar]
194.Zupec-Kania B., Zupanc M.L. Long-term management of the ketogenic diet: Seizure monitoring, nutrition, and supplementation. Epilepsia. 2008;49((Suppl. S8)):23–26. doi: 10.1111/j.1528-1167.2008.01827.x. [DOI] [PubMed] [Google Scholar]
195.Cordain L. Nutritional Deficiencies of Ketogenic Diets. 2018. [(accessed on 23 July 2023)]. Available online: https://www.researchgate.net/publication/332098774_Nutritional_Deficiencies_of_Ketogenic_Diets?channel=doi&linkId=5c9f99e2a6fdccd46045868c&showFulltext=true. License CC BY-NC-ND 4.0.
196.Iqbal S., Klammer N., Ekmekcioglu C. The Effect of Electrolytes on Blood Pressure: A Brief Summary of Meta-Analyses. Nutrients. 2019;11:1362. doi: 10.3390/nu11061362. [DOI] [PMC free article] [PubMed] [Google Scholar]
197.Gallo G., Volpe M., Savoia C. Endothelial Dysfunction in Hypertension: Current Concepts and Clinical Implications. Front. Med. 2021;8:798958. doi: 10.3389/fmed.2021.798958. [DOI] [PMC free article] [PubMed] [Google Scholar]
198.Kostov K. The Causal Relationship between Endothelin-1 and Hypertension: Focusing on Endothelial Dysfunction, Arterial Stiffness, Vascular Remodeling, and Blood Pressure Regulation. Life. 2021;11:986. doi: 10.3390/life11090986. [DOI] [PMC free article] [PubMed] [Google Scholar]
199.Polito R., Messina G., Valenzano A., Scarinci A., Villano I., Monda M., Cibelli G., Porro C., Pisanelli D., Monda V., et al. The Role of Very Low Calorie Ketogenic Diet in Sympathetic Activation through Cortisol Secretion in Male Obese Population. J. Clin. Med. 2021;10:4230. doi: 10.3390/jcm10184230. [DOI] [PMC free article] [PubMed] [Google Scholar]
200.Polito R., Valenzano A., Monda V., Cibelli G., Monda M., Messina G., Villano I., Messina A. Heart Rate Variability and Sympathetic Activity Is Modulated by Very Low-Calorie Ketogenic Diet. Int. J. Environ. Res. Public Health. 2022;19:2253. doi: 10.3390/ijerph19042253. [DOI] [PMC free article] [PubMed] [Google Scholar]
201.Barrea L., Verde L., Camajani E., Šojat A.S., Marina L., Savastano S., Colao A., Caprio M., Muscogiuri G. Effects of very low-calorie ketogenic diet on hypothalamic–pituitary–adrenal axis and renin–angiotensin–aldosterone system. J. Endocrinol. Investig. 2023;46:1509–1520. doi: 10.1007/s40618-023-02068-6. [DOI] [PMC free article] [PubMed] [Google Scholar]
202.Belany P., Kackley M.L., Zhao S., Kluwe B., Buga A., Crabtree C.D., Nedungadi D., Kline D., Brock G., Simonetti O.P., et al. Effects of Hypocaloric Low-Fat, Ketogenic, and Ketogenic and Ketone Supplement Diets on Aldosterone and Renin. J. Clin. Endocrinol. Metab. 2023;108:1727–1739. doi: 10.1210/clinem/dgad009. [DOI] [PMC free article] [PubMed] [Google Scholar]
203.Di Raimondo D., Buscemi S., Musiari G., Rizzo G., Pirera E., Corleo D., Pinto A., Tuttolomondo A. Ketogenic Diet, Physical Activity, and Hypertension—A Narrative Review. Nutrients. 2021;13:2567. doi: 10.3390/nu13082567. [DOI] [PMC free article] [PubMed] [Google Scholar]
204.Williams B., Mancia G., Spiering W., Agabiti Rosei E., Azizi M., Burnier M., Clement D., Coca A., De Simone G., Dominiczak A., et al. 2018 Practice Guidelines for the management of arterial hypertension of the European Society of Hypertension and the European Society of Cardiology: ESH/ESC Tas k Force for the Management of Arterial Hypertension. J. Hypertens. 2018;36:2284–2309. doi: 10.1097/HJH.0000000000001961. [DOI] [PubMed] [Google Scholar]
205.Di Raimondo D., Musiari G., Miceli G., Arnao V., Pinto A. Preventive and Therapeutic Role of Muscle Contraction against Chronic Diseases. Curr. Pharm. Des. 2016;22:4686–4699. doi: 10.2174/1381612822666160510125011. [DOI] [PubMed] [Google Scholar]
206.Barrea L., Verde L., Santangeli P., Lucà S., Docimo A., Savastano S., Colao A., Muscogiuri G. Very low-calorie ketogenic diet (VLCKD): An antihypertensive nutritional approach. J. Transl. Med. 2023;21:128. doi: 10.1186/s12967-023-03956-4. [DOI] [PMC free article] [PubMed] [Google Scholar]
207.Rinaldi R., De Nucci S., Castellana F., Di Chito M., Giannuzzi V., Shahini E., Zupo R., Lampignano L., Piazzolla G., Triggiani V., et al. The Effects of Eight Weeks’ Very Low-Calorie Ketogenic Diet (VLCKD) on Liver Health in Subjects Affected by Overweight and Obesity. Nutrients. 2023;15:825. doi: 10.3390/nu15040825. [DOI] [PMC free article] [PubMed] [Google Scholar]
208.Yancy W.S., Jr., Westman E.C., McDuffie J.R., Grambow S.C., Jeffreys A.S., Bolton J., Chalecki A., Oddone E.Z. A randomized trial of a low-carbohydrate diet vs orlistat plus a low-fat diet for weight loss. Arch. Intern. Med. 2010;170:136–145. doi: 10.1001/archinternmed.2009.492. Erratum in JAMA Intern. Med. 2015, 175, 470. [DOI] [PubMed] [Google Scholar]
209.Foster G.D., Wyatt H.R., Hill J.O., Makris A.P., Rosenbaum D.L., Brill C., Stein R.I., Mohammed B.S., Miller B., Rader D.J., et al. Weight and metabolic outcomes after 2 years on a low-carbohydrate versus low-fat diet: A randomized trial. Ann. Intern. Med. 2010;153:147–157. doi: 10.7326/0003-4819-153-3-201008030-00005. [DOI] [PMC free article] [PubMed] [Google Scholar]
210.Samaha F.F., Iqbal N., Seshadri P., Chicano K.L., Daily D.A., McGrory J., Williams T., Williams M., Gracely E.J., Stern L. A low-carbohydrate as compared with a low-fat diet in severe obesity. N. Engl. J. Med. 2003;348:2074–2081. doi: 10.1056/NEJMoa022637. [DOI] [PubMed] [Google Scholar]
211.Tzenios N., Lewis E.D., Crowley D.C., Chahine M., Evans M. Examining the Efficacy of a Very-Low-Carbohydrate Ketogenic Diet on Cardiovascular Health in Adults with Mildly Elevated Low-Density Lipoprotein Cholesterol in an Open-Label Pilot Study. Metab. Syndr. Relat. Disord. 2022;20:94–103. doi: 10.1089/met.2021.0042. [DOI] [PMC free article] [PubMed] [Google Scholar]
212.Bueno N., De Melo I., De Oliveira S., Da Rocha Ataide T. Very-low-carbohydrate ketogenic diet v. low-fat diet for long-term weight loss: A meta-analysis of randomised controlled trials. Br. J. Nutr. 2013;110:1178–1187. doi: 10.1017/S0007114513000548. [DOI] [PubMed] [Google Scholar]
213.Markovikj G., Knights V., Kljusurić J.G. Ketogenic Diet Applied in Weight Reduction of Overweight and Obese Individuals with Progress Prediction by Use of the Modified Wishnofsky Equation. Nutrients. 2023;15:927. doi: 10.3390/nu15040927. [DOI] [PMC free article] [PubMed] [Google Scholar]
214.Muscogiuri G., Barrea L., Laudisio D., Pugliese G., Salzano C., Savastano S., Colao A. The management of very low-calorie ketogenic diet in obesity outpatient clinic: A practical guide. J. Transl. Med. 2019;17:356. doi: 10.1186/s12967-019-2104-z. [DOI] [PMC free article] [PubMed] [Google Scholar]
215.Powell-Wiley T.M., Poirier P., Burke L.E., Després J.P., Gordon-Larsen P., Lavie C.J., Lear S.A., Ndumele C.E., Neeland I.J., Sanders P., et al. American Heart Association Council on Lifestyle and Cardiometabolic Health; Council on Cardiovascular and Stroke Nursing; Council on Clinical Cardiology; Council on Epidemiology and Prevention; and Stroke Council. Obesity and Cardiovascular Disease: A Scientific Statement from the American Heart Association. Circulation. 2021;143:e984–e1010. doi: 10.1161/CIR.0000000000000973. [DOI] [PMC free article] [PubMed] [Google Scholar]

















 Lähde: https://www.hindawi.com/journals/jnme/2018/7195760/
Lähde: https://www.hindawi.com/journals/jnme/2018/7195760/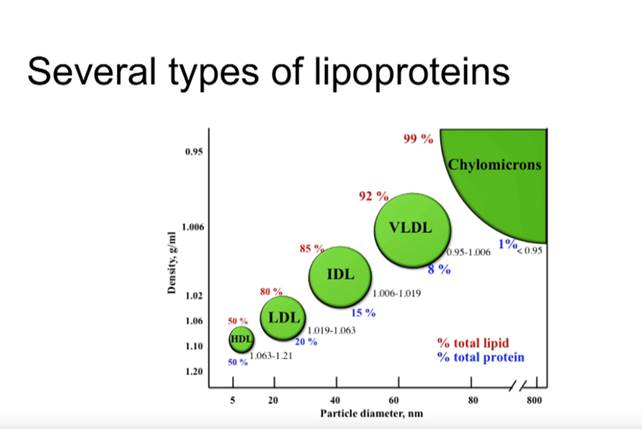

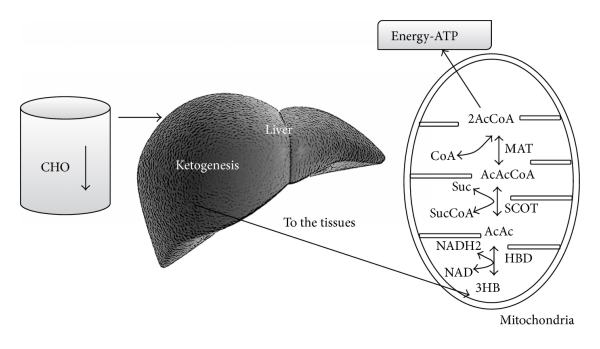 Keskushermostossa glukoosia tarvitaan energia lähteeksi, sekä tuottamaan pyruvaatteja, jotka voidaan edelleen muuntaa oksaloasetaatiksi.
Keskushermostossa glukoosia tarvitaan energia lähteeksi, sekä tuottamaan pyruvaatteja, jotka voidaan edelleen muuntaa oksaloasetaatiksi.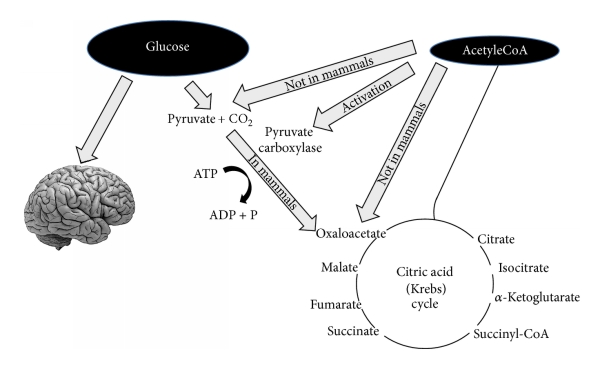












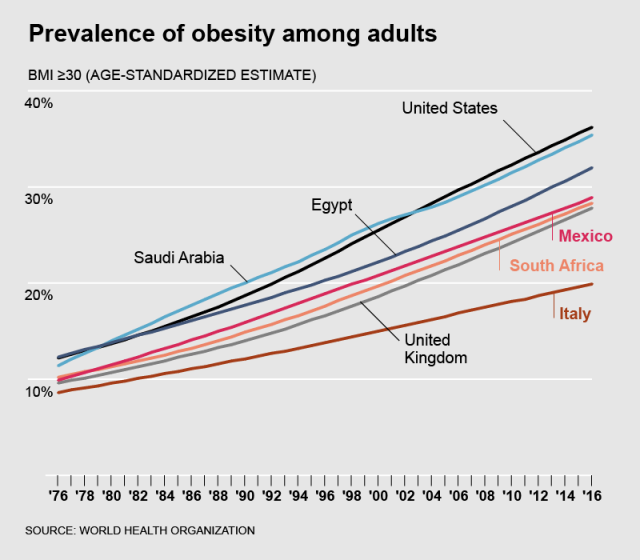








 Lihavuuden yleistyminen
Lihavuuden yleistyminen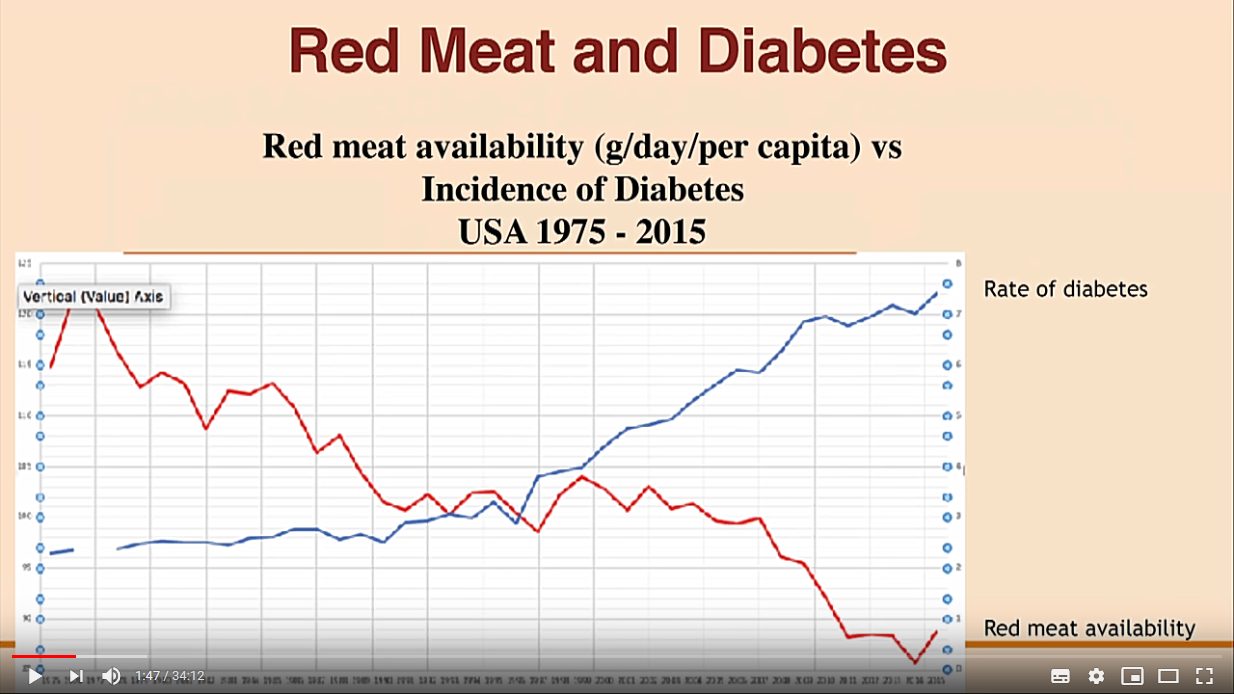

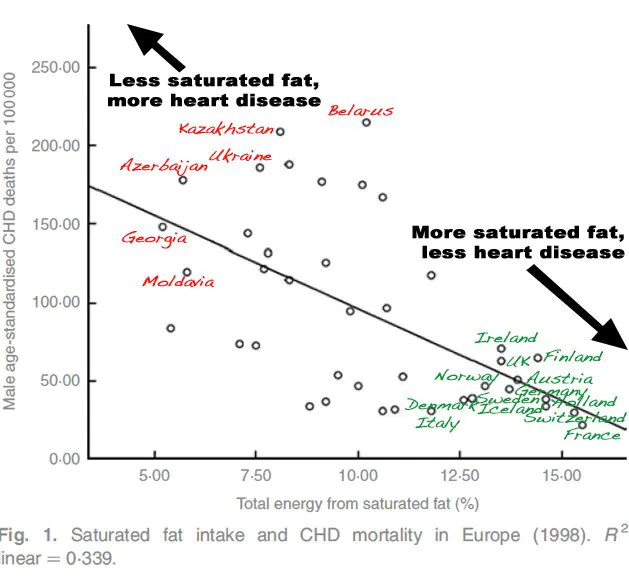
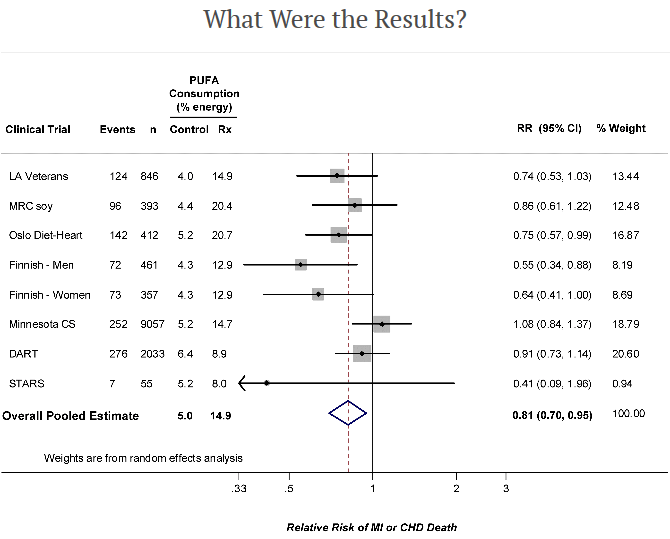
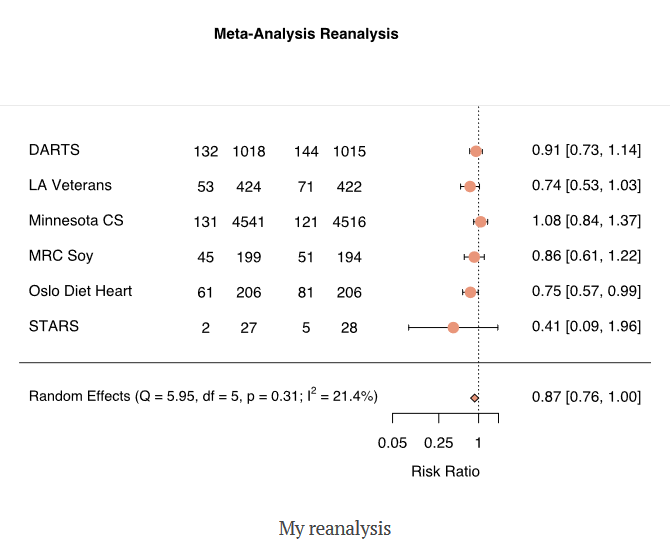
 60– ja 70-luvuilla rasvojen terveysvaikutuksista tehtiin kiinnostavia kontrolloituja satunnaistettuja tutkimuksia (CRT). Nämä tutkimukset eivät kuitenkaan mahtuneet vallitsevaan hypoteesiin kovien rasvojen haitallisuudesta, joten ne niiden annettiin unohtua.
60– ja 70-luvuilla rasvojen terveysvaikutuksista tehtiin kiinnostavia kontrolloituja satunnaistettuja tutkimuksia (CRT). Nämä tutkimukset eivät kuitenkaan mahtuneet vallitsevaan hypoteesiin kovien rasvojen haitallisuudesta, joten ne niiden annettiin unohtua.



